
历久弥坚,TOPAZ-1研究4年OS更新结果助力BTC患者长期生存
胆道恶性肿瘤(BTC)是一类呈高度异质性的肿瘤,其起病隐匿,多数患者确诊时已处于晚期,失去根治性手术治疗机会,预后较差。长年以来,晚期BTC的一线标准治疗方案为吉西他滨 +顺铂
+顺铂 (GC),但患者获益有限,生存不足一年。直至近年来程序性死亡蛋白1/程序性死亡配体1(PD-1/PD-L1)抑制剂等免疫检查点抑制剂的快速发展为肿瘤治疗带来了全新突破,尤其是III期TOPAZ-1、KEYNOTE-966等研究的成功打破了化疗瓶颈,为患者带来了显著的生存获益提升,开启了BTC免疫治疗新时代。
(GC),但患者获益有限,生存不足一年。直至近年来程序性死亡蛋白1/程序性死亡配体1(PD-1/PD-L1)抑制剂等免疫检查点抑制剂的快速发展为肿瘤治疗带来了全新突破,尤其是III期TOPAZ-1、KEYNOTE-966等研究的成功打破了化疗瓶颈,为患者带来了显著的生存获益提升,开启了BTC免疫治疗新时代。
打破十余年治疗瓶颈,
TOPAZ-1研究改写晚期BTC治疗格局
TOPAZ-1研究是十余年来晚期BTC一线免疫治疗首个取得阳性结果的全球、多中心、III期临床研究,旨在探索度伐利尤单抗 联合GC化疗方案相较于安慰剂联合GC化疗的疗效和安全性。研究共纳入685例患者,按1:1随机分配至度伐利尤单抗联合GC组(n=341)或安慰剂联合GC组(n=344)。主要研究终点是总生存期(OS),次要研究终点包括无进展生存期(PFS)、客观缓解率(ORR)、缓解持续时间(DoR)和安全性1。
联合GC化疗方案相较于安慰剂联合GC化疗的疗效和安全性。研究共纳入685例患者,按1:1随机分配至度伐利尤单抗联合GC组(n=341)或安慰剂联合GC组(n=344)。主要研究终点是总生存期(OS),次要研究终点包括无进展生存期(PFS)、客观缓解率(ORR)、缓解持续时间(DoR)和安全性1。
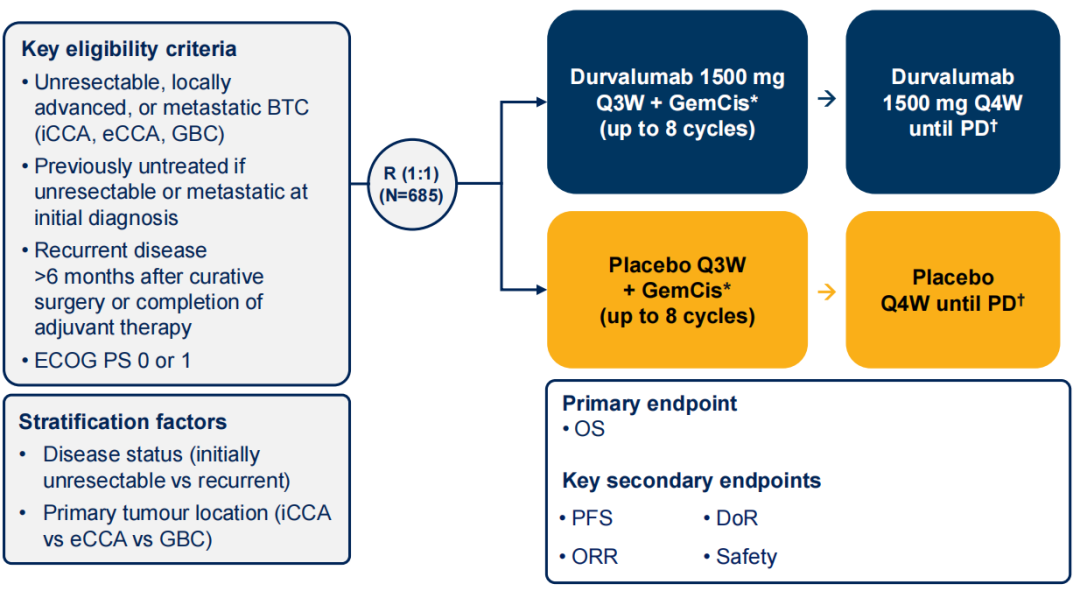
图1 TOPAZ-1研究设计
该研究初次公布的数据显示度伐利尤单抗联合GC化疗方案相较安慰剂联合化疗可显著改善患者的OS(12.8个月 vs 11.5个月,HR=0.80)、PFS(7.2个月 vs 5.7个月,HR=0.75)和ORR(26.7% vs 18.7%),且安全性良好1。继续随访6.5个月后,两组更新的OS数据分别为12.9个月 vs 11.3个月(HR=0.76),2年OS率提升了近一倍(23.6% vs 11.5%)2。基于上述研究结果,CSCO、NCCN等国内外权威指南均推荐度伐利尤单抗联合吉西他滨+化疗作为局部晚期或转移性BTC的一线治疗优选方案。
TOPAZ-1研究中位随访达41.3个月时,度伐利尤单抗联合GC组仍维持显著OS获益,其中位OS为12.9个月,安慰剂联合GC组为11.3个月,HR值进一步降低至0.74。而且度伐利尤单抗联合GC组的3年OS率为14.6%,较安慰剂联合GC组的6.9%翻倍。值得注意的是,在达到疾病控制的患者(566/685例,82.6%)中,度伐利尤单抗联合GC组的3年OS率高达17.0%,而安慰剂联合GC组仅为7.6%3。
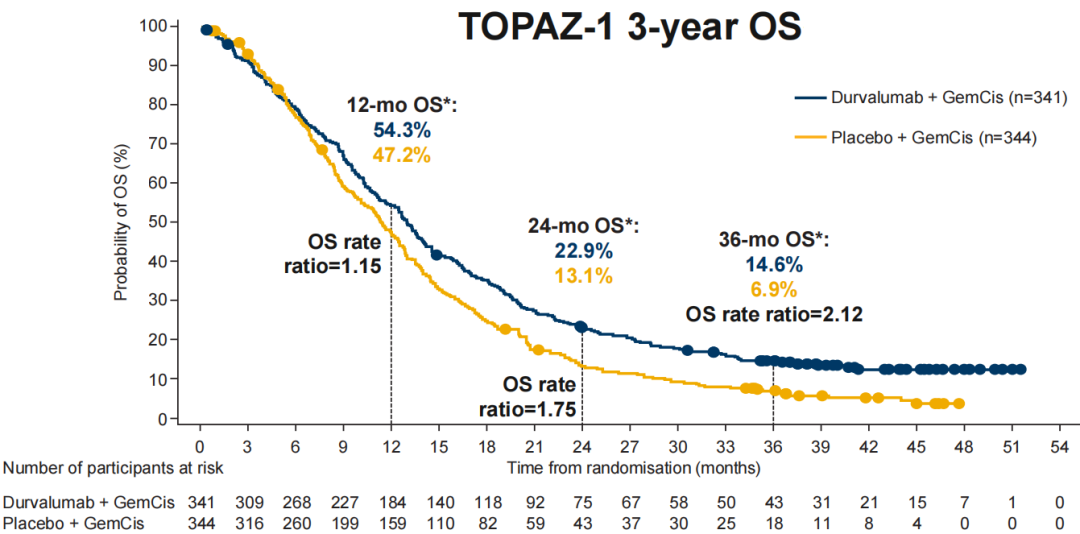
图2 TOPAZ-1研究的3年OS率结果
此外,该研究对长生存患者(eLTS,即随机化后存活≥30个月的全分析集中的受试者)的特征和结果进行了评估和分析。结果显示,所有临床相关亚组中均可见eLTS患者。全分析集(FAS)中,12.8%(88/685例)的患者为eLTS,其中度伐利尤单抗联合GC组(17.0%)的比例高于安慰剂联合GC组(8.7%)。此外,无论患者后续是否接受抗肿瘤治疗,相较安慰剂联合GC,度伐利尤单抗联合GC方案均能改善OS。安全性方面,在eLTS中,两组间的严重不良事件(SAE)发生率相当(32.8% vs 36.7),且低于FAS(44.8% vs 44.4%)3。
基于3年的持续随访数据,度伐利尤单抗联合GC方案的长期生存获益得到进一步确认,特别是在实现疾病控制的患者群体中表现尤为突出。研究同时表明,eLTS患者广泛存在于不同临床特征的亚组人群中,充分证实了该方案在晚期BTC治疗中的普适性,有望为不同人群带来长生存希望。
4年随访数据揭示免疫联合方案OS获益持续扩大,长期生存逐步成为现实
2026年欧洲肝脏研究学会肝癌峰会(EASL LCS)会议上,TOPAZ-1研究重磅更新了超4年随访的疗效和安全性数据。本次分析的数据截止日期(DCO)为2025年2月28日,即最后一名患者入组约48个月后。截至该节点,度伐利尤单抗联合GC组的中位随访时间已达到56.9个月,安慰剂联合GC组为50.7个月4。
随着随访时间的延长,免疫联合治疗方案的生存获益进一步凸显。度伐利尤单抗联合GC组的中位OS达13.0个月,仍显著优于安慰剂联合GC组的11.4个月(HR=0.75)。从最初的0.80,到如今的0.75,OS HR值的逐步下降和持续稳定,清晰勾勒出免疫治疗所特有的“长拖尾效应”,提示更多晚期BTC患者正迈入长期生存的行列。此外,度伐利尤单抗联合GC组的4年OS率达到11.8%,而安慰剂联合GC组仅为4.3%,这一数据意味着在接受免疫联合方案治疗的患者中,超过十分之一实现了长期生存4。
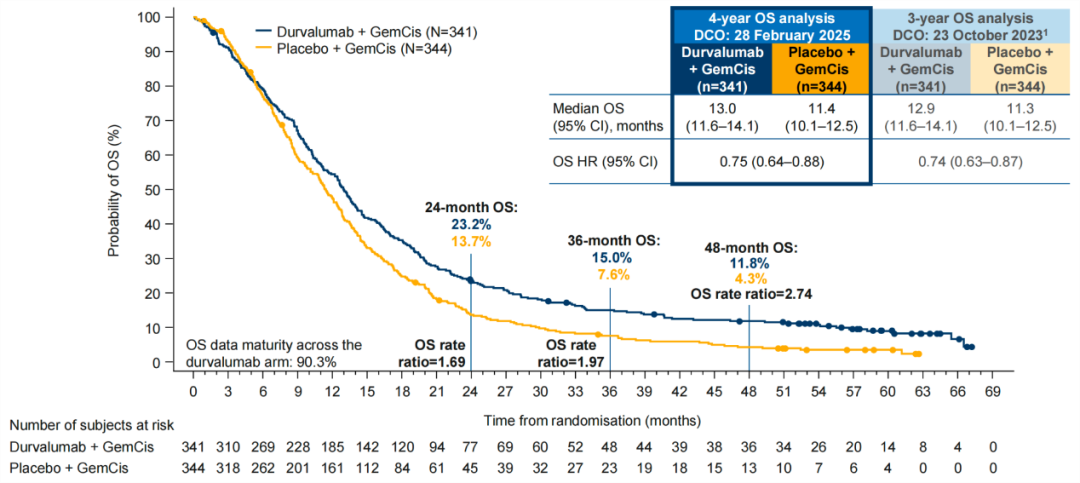
图3 TOPAZ-1研究的更新OS、4年OS率结果
此外,研究分析显示,在3年至4年的随访区间内,两组患者后续接受抗肿瘤治疗的比例未见明显变化,整体保持平衡,后续治疗仍以细胞毒化疗为主。
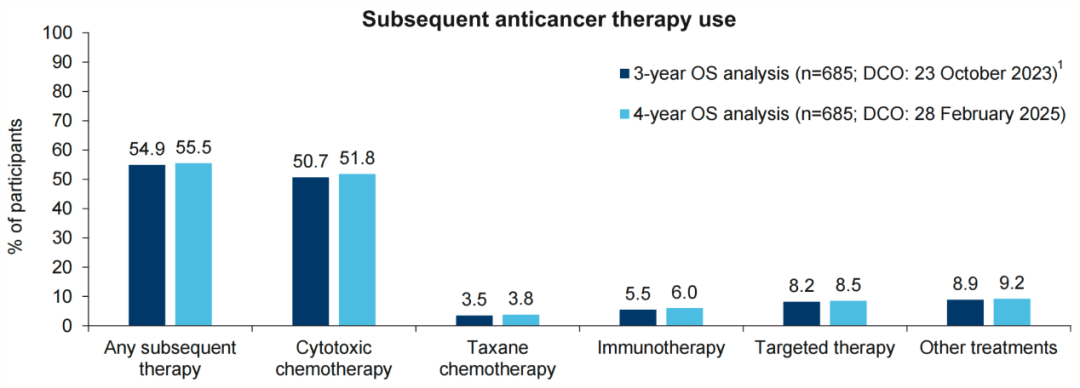
图4 DCO时患者接受后续治疗情况
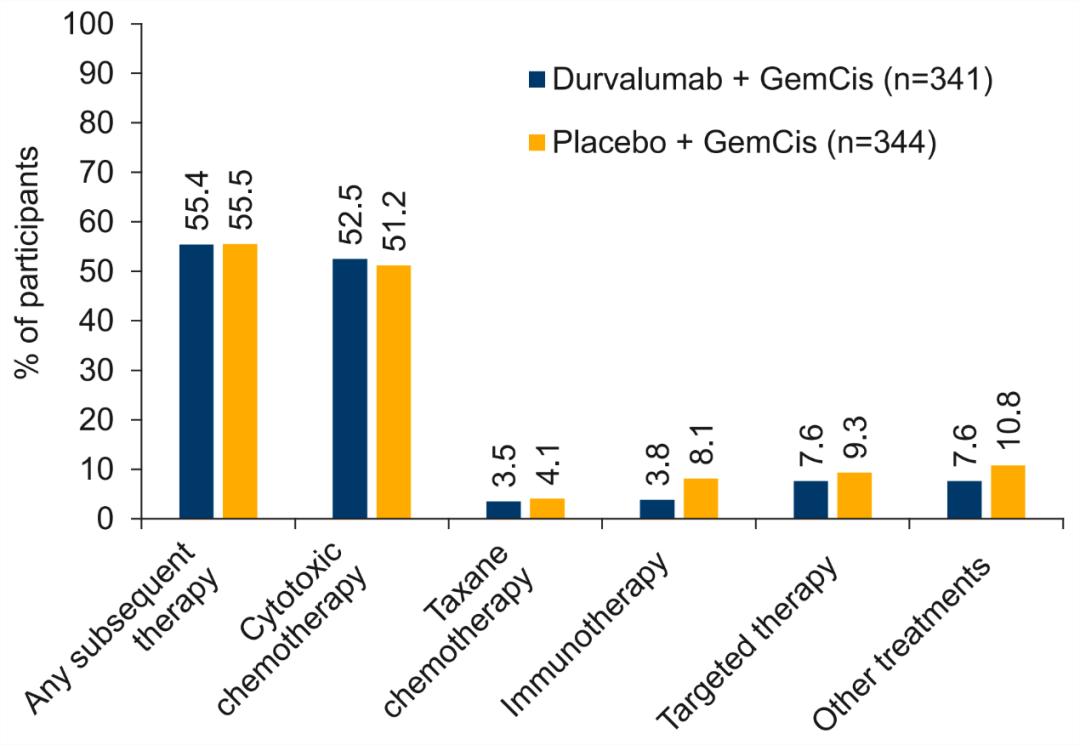
图5 DCO时患者接受后续治疗情况
安全性方面,本次长期随访未发现新的安全性信号,也未出现潜在的严重不良反应。与3年数据截止时相比,度伐利尤单抗联合GC组的安全谱保持稳定,与安慰剂联合GC组亦无明显差异。值得注意的是,截至数据截止日,度伐利尤单抗联合GC组仍有7例患者继续接受度伐利尤单抗联合GC治疗,而安慰剂联合GC组已无患者继续治疗,这一差异从侧面印证了该免疫联合方案的长期耐受性和临床可行性4。
同时,TOPAZ-1研究也存在着一定局限性,如所有探索性分析均为事后分析,未进行正式的统计学检验;随访约3年时,仍存活的患者数量较少,因此将eLTS的阈值设定为30个月,以确保此项事后分析包含足够数量的患者以进行有意义的比较。此外,研究样本量较小,无法对度伐利尤单抗长期获益的潜在预后或预测生物标志物进行研究,该领域仍需进一步探索。
小结
TOPAZ-1研究是首个报告免疫联合化疗方案治疗晚期BTC患者4年OS数据的随机对照III期研究。经过长达4年的持续随访,该研究再次证实,度伐利尤单抗联合GC方案能为患者带来持久且具有临床价值的生存改善。度伐利尤单抗联合GC组的4年OS率相较安慰剂联合GC组实现近3倍提升,OS HR稳步下降至0.75,且在长期观察中未发现新的安全性信号。此次长期随访结果的公布,意味着未来将有更多晚期BTC患者有望迈入长期生存队列。
上述成果不仅进一步巩固了度伐利尤单抗联合GC方案作为晚期BTC一线治疗核心方案的地位,也为推动晚期BTC治疗目标从短期控制向长期生存跨越提供了有力证据,有望持续惠及全球患者。
本材料由阿斯利康提供,仅供医疗卫生专业人士参考,不可用于推广目的。
审批号:CN-179546
有效期:2027.03.08

