
乳腺癌复发监测新范式:非侵入性生物标志物的临床进展
前言
乳腺癌 作为全球女性健康的主要威胁之一,其复发问题始终是肿瘤学领域的重大挑战。据临床数据显示,约25%-30%的早期乳腺癌患者会出现疾病复发,且部分会进展为不可治愈的转移性疾病,成为导致长期死亡和发病的关键因素。传统的复发监测手段以影像学检查和血清肿瘤标志物
作为全球女性健康的主要威胁之一,其复发问题始终是肿瘤学领域的重大挑战。据临床数据显示,约25%-30%的早期乳腺癌患者会出现疾病复发,且部分会进展为不可治愈的转移性疾病,成为导致长期死亡和发病的关键因素。传统的复发监测手段以影像学检查和血清肿瘤标志物 为主,但这些方法存在局限性:影像学检查成本高昂、可及性有限;血清标志物灵敏度和特异性不足,并且在早期复发检测中表现不佳,常无法及时发现亚临床转移。因此,开发非侵入性、高灵敏度、高特异性的监测手段,对于实现乳腺癌复发的早期干预和改善预后具有重要意义。
为主,但这些方法存在局限性:影像学检查成本高昂、可及性有限;血清标志物灵敏度和特异性不足,并且在早期复发检测中表现不佳,常无法及时发现亚临床转移。因此,开发非侵入性、高灵敏度、高特异性的监测手段,对于实现乳腺癌复发的早期干预和改善预后具有重要意义。
近年来,非侵入性生物标志物的研究取得了重要进展,为乳腺癌复发监测带来了新的思路。这类生物标志物通过液体活检技术分析血液、尿液、唾液等体液中的循环肿瘤DNA(ctDNA)、循环肿瘤细胞(CTC)和外泌体等成分,无需侵入性操作即可实时反映肿瘤的分子动态和生物学状态,不仅克服了传统方法的缺陷,还能为个体化治疗提供精准指导。
ctDNA:精准捕捉分子复发信号的核心力量
ctDNA是肿瘤细胞凋亡或坏死过程中释放到外周血中的肿瘤特异性DNA片段,仅占游离DNA(cfDNA)的极小部分。ctDNA检测的优势在于能够精准捕捉肿瘤的分子特征,例如HR+/HER2-肿瘤中的PIK3CA和ESR1突变以及HER2扩增型肿瘤中的ERBB2特异性标志物等,为亚型导向的监测提供了可能。
CTC:反映肿瘤转移潜能的关键指标
CTC作为完整的肿瘤细胞,携带了肿瘤的表型和功能信息,其在血液中与肿瘤转移密切相关,是预测乳腺癌复发的重要指标。并且CTC的表型分析(如HER2、PD-L1表达)能够反映肿瘤异质性,为治疗方案调整提供依据,例如HER2阴性肿瘤中出现HER2阳性CTC可能提示治疗耐药,需调整治疗策略。
外泌体:承载肿瘤生物学信息的微型载体
外泌体是一类由肿瘤细胞释放的细胞外囊泡,包含了蛋白质、脂质、核酸等成分,能够反映肿瘤的生物学状态。目前已发现多种与乳腺癌复发相关的外泌体标志物,例如外泌体存活蛋白在乳腺癌患者中的浓度高于健康人群;hsa-miR-21-5p在乳腺癌患者中高表达,可有效区分健康人与癌症患者;而miR-92b-5p则为乳腺癌诊断提供了新的非侵入性选择。
多组学整合策略的兴起为乳腺癌复发监测提供了较为全面的视角。该方法融合基因组、转录组、蛋白质组和代谢组数据,通过机器学习框架捕捉复杂的分子模式和相关性,实现动态、个体化的监测。多组学数据的整合不仅提高了复发检测的灵敏度和特异性,还能为治疗靶点的发现提供依据,推动精准医疗的发展。
基因组学
基因组学聚焦DNA水平的改变,是多组学研究的基础。NGS技术的发展实现了快速、经济、高效的多基因测序,可同时检测多个与乳腺癌复发相关的基因突变,如TP53、PIK3CA、BRCA1/2、BARD1、BRIP1等。
转录组学
转录组学则关注基因表达水平,包括信使RNA和非编码RNA。研究发现,miR-21、miR-155等RNA特征与乳腺癌进展和复发相关;一项针对136例患者的研究鉴定出2000多种与乳腺癌复发相关的RNA。这些RNA特征为揭示疾病复发的分子机制和开发治疗靶点提供了重要线索。
蛋白质组学和代谢组学
蛋白质组学通过质谱技术识别调控免疫抑制和血管生成的特异性蛋白标志物,其为理解肿瘤的功能状态和复发机制提供了直接依据;而代谢组学则通过利用GC-MS、LC-MS、NMR光谱等技术分析生物体液(尿液、血清、血浆、唾液)或组织中的代谢物变化,揭示肿瘤相关的代谢通路紊乱。例如当糖酵解通路上调时,代谢物水平的动态变化能够反映肿瘤生理状态和微环境改变,可作为复发监测的敏感指标。
值得一提的是,与分子标志物相比,代谢组学标志物能更早地反映治疗反应和复发趋势,但易受饮食、合并症等非肿瘤因素影响。因此在实际应用中,整合这两种检测方式可发挥它们的互补优势:分子标志物检测能以高特异性确认肿瘤特异性事件,而代谢组学检测结果则能为肿瘤复发或治疗反应提供早期预警。
生物标志物检测技术的革新为乳腺癌复发精准监测提供了关键支撑,各类技术的突破提升了非侵入性生物标志物的检测灵敏度、特异性和临床实用性,为发现复发信号、动态监测肿瘤状态提供了有力工具。
ctDNA检测技术
ctDNA检测技术包括Droplet Digital PCR(ddPCR)和下一代测序(NGS),这两种技术均具备高灵敏度,能够捕捉到血液中微量的肿瘤特异性DNA片段,检测下限可低至等位基因频率0.1%以下,并且使分子复发的检测中位数比影像学进展提前10-12个月。其中ddPCR凭借成本适中、检测周期短的优势,更适合临床常规监测场景,可快速提供明确的检测结果;NGS则能全面覆盖肿瘤的突变谱,一次性检测多个基因的多种遗传改变,为精准分型和治疗靶点筛选提供丰富信息,已成为精准肿瘤学中复发监测的标准技术之一。
CTC分离与分析技术
微流控设备的研发提升了CTC的分离效率,这类平台可基于细胞大小、免疫亲和性或密度对CTC进行精准分选。捕获后的CTC可通过单细胞测序、表型分析等技术,获取其分子特征和功能信息,例如检测CTC表面EMT标志物水平,为判断肿瘤转移潜能、评估治疗耐药性提供依据,助力个性化治疗方案的调整。
外泌体检测技术
外泌体的高效分离与成分分析得益于纳米技术的应用。纳米颗粒传感器和生物工程平台的发展,增强了外泌体分离的灵敏度和纯度。通过这些技术,可精准提取外泌体中的蛋白质、miRNA等生物标志物,明确其与乳腺癌复发的关联,为复发风险评估和动态监测提供新的视角。但目前外泌体检测技术仍缺乏统一的标准化流程,限制了其临床转化。
新兴检测技术
除了上述检测技术外,可穿戴设备和即时检测(POCT)新技术的发展,为乳腺癌复发监测开辟了新方向。这类技术通过整合生物标志物检测与数据分析,实时反映肿瘤动态。例如目前正在研发的可穿戴传感器,能够检测间质液中的ctDNA或外泌体RNA,实现无创、连续的复发监测。然而这些新兴技术面临成本较高、检测稳定性待验证等问题,尚未进入大规模临床应用阶段。
非侵入性生物标志物在乳腺癌复发监测中的临床价值已通过多项临床研究逐步验证,这些研究涵盖干预性试验、观察性研究等多种类型,聚焦生物标志物指导治疗策略、风险分层、早期检测等核心目标。例如有研究表明,在常规ctDNA监测中,部分患者的ctDNA阳性信号早于影像学检查,在早期治疗干预方面具有重要意义。
此外,多项临床研究正在验证非侵入性生物标志物的临床价值。Ⅱ期DARE试验(NCT04567420)纳入100例早期乳腺癌患者,探索ctDNA指导的辅助治疗升降级策略;c-TRAKTN试验(NCT03145961)针对208例术后三阴性乳腺癌患者,评估ctDNA检测在治疗指导中的作用;TRAK-ER试验(NCT04985266)则纳入1100例患者,通过ctDNA检测分层复发风险并个性化监测方案。这些试验的结果将为非侵入性生物标志物的临床应用提供高级别证据支持。
表1:非侵入性生物标志物检测和监测乳腺癌的区别
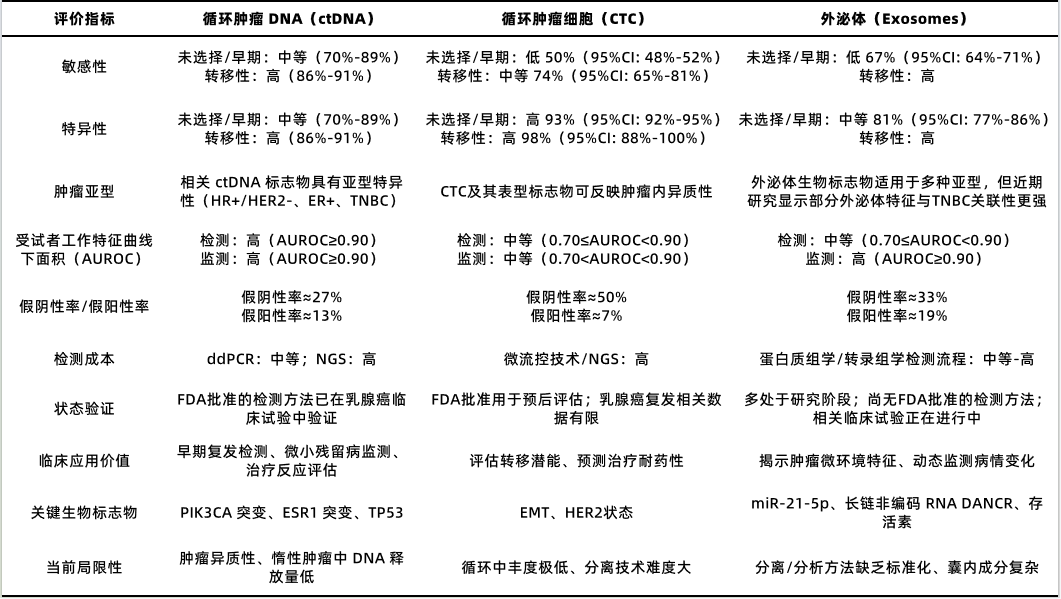
总结
综上所述,非侵入性生物标志物(ctDNA、CTC、外泌体)结合液体活检技术,突破了传统监测方法的局限,尤其在监测疾病复发或进展、治疗反应评估以及识别靶向突变以指导治疗方面表现突出,这类生物标志物比传统方法更灵敏,且能实时反映肿瘤行为动态。并且检测技术的进步(包括ddPCR、NGS和微流控平台)使其能够用于复发的个体化动态监测。
然而,非侵入性生物标志物的应用仍存在亟待解决的问题,包括生物学变异性、技术局限性、成本压力以及可及性差异等系统性障碍。这些问题需要通过研发创新与专业协作共同解决。此外,还需开展严谨的验证研究并建立标准化流程,以确立这些技术在不同人群和医疗系统中的可信度与适用性。
审批编号:CN-179606
有效期至:2027-03-09
本文由阿斯利康提供,仅供医疗卫生专业人士参考,不可用于推广目的。
