溯经典,愈新生丨金锋、胡夕春教授:纵观乳腺癌治疗演进历程,共绘个体化治疗蓝图
导读:
三月芳华,三八国际妇女节如期而至。女性健康是全社会共同关注的重要议题,而乳腺癌 作为威胁全球女性健康与生命安全的头号恶性肿瘤,其诊疗创新与规范化发展,始终是医学界聚焦的核心课题。回溯乳腺癌治疗的发展脉络,从传统化疗、内分泌治疗,到靶向药物精准治疗,这一演进历程正深刻重塑着临床实践,极大地改善了患者的生存与生活质量。其中,诸多经典治疗方案历经时间沉淀,始终是乳腺癌治疗体系中屹立不倒的坚实基石。在此背景下,医脉通诚挚邀请中国医科大学附属第一医院金锋
作为威胁全球女性健康与生命安全的头号恶性肿瘤,其诊疗创新与规范化发展,始终是医学界聚焦的核心课题。回溯乳腺癌治疗的发展脉络,从传统化疗、内分泌治疗,到靶向药物精准治疗,这一演进历程正深刻重塑着临床实践,极大地改善了患者的生存与生活质量。其中,诸多经典治疗方案历经时间沉淀,始终是乳腺癌治疗体系中屹立不倒的坚实基石。在此背景下,医脉通诚挚邀请中国医科大学附属第一医院金锋 教授、复旦大学附属肿瘤医院胡夕春
教授、复旦大学附属肿瘤医院胡夕春 教授聚焦乳腺癌领域关键治疗策略的演变,系统回顾经典治疗方案的价值,并展望未来的发展趋势,以期为乳腺癌治疗的前行之路点亮新的思路。
教授聚焦乳腺癌领域关键治疗策略的演变,系统回顾经典治疗方案的价值,并展望未来的发展趋势,以期为乳腺癌治疗的前行之路点亮新的思路。
巾帼安康 ——三八妇女节专家寄语
——三八妇女节专家寄语
Q1:春风送暖,巾帼安康,在三八国际妇女节这个致敬女性、关爱女性健康的美好节日,诚邀两位教授结合深耕乳腺诊疗领域的初心与临床经验,为广大女性朋友送上节日的美好寄语,分享守护乳腺健康的暖心建议与感悟?
金锋教授
中国医科大学附属第一医院
胡夕春教授
复旦大学附属肿瘤医院
溯本求源——化疗时代的演进与蒽环类药物角色的变迁
Q2:化疗是乳腺癌中的传统治疗方式,其中以蒽环类药物为基础的化疗方案应用历史悠久、临床获益明确。在乳腺癌治疗迈向精准化、个体化的当下,能否请您结合当前乳腺癌领域的化疗演进趋势,谈谈蒽环类药物在其中的地位与价值?
金锋教授
中国医科大学附属第一医院
精进不止——HR+乳腺癌的个体化决策
Q3:HR+/HER2-乳腺癌是乳腺癌中占比最高的亚型,以内分泌治疗为核心的治疗策略已成为该类患者的治疗基石。对于HR+早期乳腺癌患者,请您结合相关研究,谈谈应如何优化这类人群的辅助内分泌治疗策略,以实现患者获益最大化?
胡夕春教授
复旦大学附属肿瘤医院
Q4:在晚期HR+乳腺癌领域,CDK4/6抑制剂联合内分泌治疗已确立为一线标准治疗方案。目前国内已有多种CDK4/6抑制剂可供选择,临床医生应综合考量哪些因素,以进行个体化治疗决策?
金锋教授
中国医科大学附属第一医院
拥抱变革——ADC时代的突破与未来
Q5:除HR+乳腺癌外,HER2阳性乳腺癌作为一类特殊的亚型,同样备受关注。作为首个获批用于乳腺癌治疗的ADC药物,T-DM1开创了HER2阳性乳腺癌治疗新格局。请您谈谈T-DM1的独特结构与作用机制优势,对后续ADC药物的研发路径产生了哪些深远影响?
胡夕春教授
复旦大学附属肿瘤医院
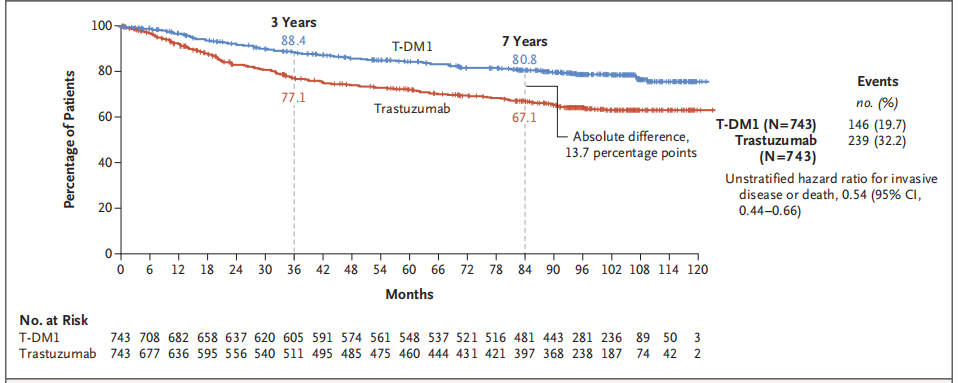
Q6:在HER2阳性早期乳腺癌治疗中,新辅助治疗已成为重要治疗手段。但临床中部分患者经新辅助治疗后仍残存侵袭性病灶,这类患者复发风险较高、治疗难度较大,请问针对这类患者,后续辅助治疗的核心思路及关键循证证据有哪些?
金锋教授
中国医科大学附属第一医院
Q7:从化疗、内分泌到以ADC药物为代表的靶向治疗的升级迭代,乳腺癌已呈现慢病化发展趋势。在此背景下,您认为未来乳腺癌治疗的整体发展方向是什么?如何进一步完善个体化治疗策略,更好地惠及广大乳腺癌患者?
胡夕春教授
复旦大学附属肿瘤医院
专家简介
胡夕春教授
复旦大学附属肿瘤医院教授 博导
ESMO乳腺癌Faculty Member 国际ABC 5-7 panelist
中华医学会肿瘤分会肿瘤内科专家委员会副主任委员
中国抗癌协会多原发和不明原发肿瘤专委会荣誉主委
中国抗癌协会临床化疗专委会副主委
中国抗癌协会分子靶向专委会副主委
中国研究型医院学会乳腺专业委员会副主委
上海市医师协会肿瘤分会副会长
上海市抗癌协会常务理事
上海抗癌协会肿瘤药物临床研究专业委员会主任委员
上海抗癌协会癌症康复和姑息治疗委员会前任主任委员
国家食品药品监督管理总局审评中心审评专家
发表论著300多篇,包括Lancet Onco等 主编《肿瘤内科方案的药物不良反应及对策》和《肿瘤科常见诊疗问题问答-胡夕春医生查房实录》等 主持十三五“重大新药创制”科技重大专项等
获上海市领军人才、中国抗癌协会科技奖二等奖、全国妇幼健康科学技术奖一等奖和上海市医学科技进步奖一等奖等
金锋 教授
二级教授 主任医师 博士生导师
中国医科大学附属第一医院乳腺外科
辽宁省抗癌协会乳腺癌专业委员会主任委员
辽宁省医学会乳腺外科分会主任委员
中华医学会肿瘤分会乳腺肿瘤学组名誉副组长
中国抗癌协会乳腺癌专业委员会副主任委员
中国临床肿瘤学会
CSCO-BC常务委员
中华医学会外科分会乳腺外科学组委员
中国医师学会外科分会乳腺外科专家组副组长
北京乳腺病防治学会外科专委会副主任委员
辽宁医学会外科分会乳腺外科学组组长
* 目前唯一:截至2026年3月8日。
编辑:Phoebe
审校:Ninian
排版:Seren
执行:Ocean
本平台旨在为医疗卫生专业人士传递更多医学信息。本平台发布的内容,不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议。如该等信息被用于了解医学信息以外的目的,本平台不承担相关责任。本平台对发布的内容,并不代表同意其描述和观点。若涉及版权问题,烦请权利人与我们联系,我们将尽快处理。