
图话消化|基于富勒烯的氨基纳米平台使VEGFR2靶向抗血管生成和肿瘤免疫治疗具有协同作用
背
景
补
充
病理性血管生成在为肿瘤提供氧气和营养的同时,也促进了免疫抑制性肿瘤微环境(TME)的形成,加剧了免疫逃逸,从而严重制约了多种癌症疗法的疗效。血管内皮生长因子A(VEGF-A)及其主要受体VEGFR2(激酶插入结构域受体,KDR)在肿瘤中常常过度表达,是关键的治疗靶点。VEGFR2在结直肠癌 中高度表达,但其抑制剂常面临耐药性及免疫调节作用不明确的问题。如何将候选药物高效、特异地递送到肿瘤部位,同时保证其稳定性和安全性,是纳米医学领域的核心挑战。
中高度表达,但其抑制剂常面临耐药性及免疫调节作用不明确的问题。如何将候选药物高效、特异地递送到肿瘤部位,同时保证其稳定性和安全性,是纳米医学领域的核心挑战。
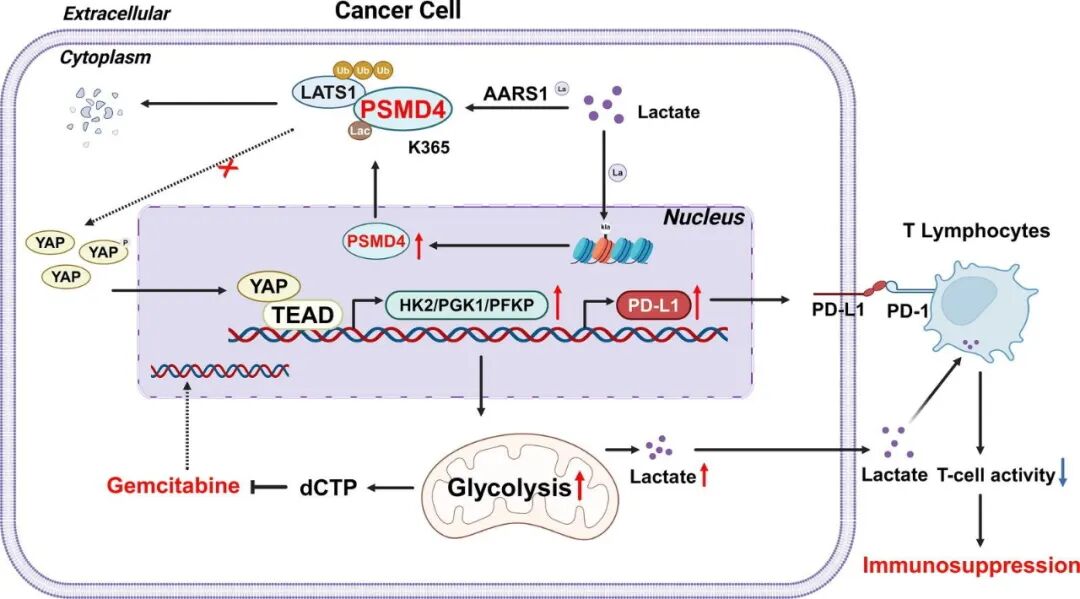
通过表型筛选,研究者鉴定出富勒烯衍生物四[4-(氨基)哌啶-1-基]C60 环氧化物(TAPC)能有效抑制血管生成。
TAPC能靶向VEGFR2,降低其表达并抑制肿瘤和内皮细胞中的PI3K-AKT信号。
为实现靶向递送,研究者将TAPC封装于PLGA纳米颗粒中,并用同源肿瘤细胞膜进行包被,制备了肿瘤细胞膜包被纳米颗粒(TAPC@CNPs)。
TAPC@CNPs 显著抑制肿瘤生长并降低血管生成标志物,包括 VEGFR2 和 CD31。此外,治疗降低了调控 T 细胞水平,增加了 T 细胞的浸润和激活,表明抗肿瘤免疫力增强。
研究结论
本研究证实TAPC是高效的VEGFR2靶向抑制剂,其经同源肿瘤细胞膜包裹的纳米颗粒(TAPC@CNPs)递送后,稳定性与肿瘤靶向性大幅提升,可同时抑制肿瘤血管生成、重塑肿瘤免疫微环境,为攻克癌症治疗中血管生成与免疫抑制双重难题提供了新型纳米材料策略。
END

参考文献:
Jiawei Huo, et al. Aminated fullerene-based nanoplatform enables synergistic VEGFR2-targeted anti-angiogenesis and tumor immunotherapy, Bioactive Materials, Volume 62,2026, Pages248-262, ISSN 2452-199X. https://doi.org/10.1016/j.bioactmat.2026.03.016.
编辑:Ivyke
审核:Aurora
排版:Ivyke
执行:Aurora
 ,助力中国临床决策”是平台的使命。医脉通旗下拥有「临床指南」「用药参考」「医学文献王」「医知源」「e研通」「e脉播」等系列产品,全面满足医学工作者临床决策、获取新知及提升科研效率等方面的需求。
,助力中国临床决策”是平台的使命。医脉通旗下拥有「临床指南」「用药参考」「医学文献王」「医知源」「e研通」「e脉播」等系列产品,全面满足医学工作者临床决策、获取新知及提升科研效率等方面的需求。