
重磅!乙肝治愈新药要来了,在研乙肝新药Bepirovirsen(GSK836)中国申请上市|肝注「药」闻
2026 年 3 月 17 日,国家药品监督管理局药品审评中心(CDE)发布最新公示,葛兰素史克(GSK)研发的慢性乙型肝炎治疗新药贝普若韦生注射液(Bepirovirsen,研发代号 GSK836) 纳入拟优先评审品种名单。
若公示无异议,该药物将进入加速审批通道,我国慢乙肝患者距离获得功能性治愈的创新药又近了一步。
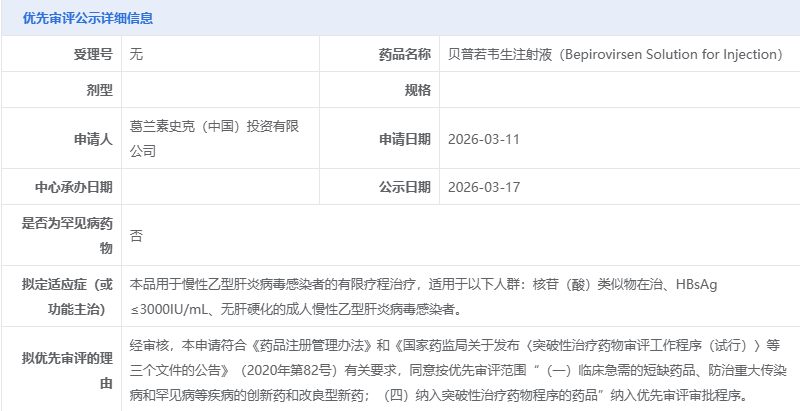
此次 GSK836 的上市申请于 2026 年 3 月 11 日提交,拟定适应症为慢性乙型肝炎病毒 感染者的有限疗程治疗,适用人群明确为核苷(酸)类似物在治、乙肝表面抗原(HBsAg)≤3000 IU/mL、无肝硬化
感染者的有限疗程治疗,适用人群明确为核苷(酸)类似物在治、乙肝表面抗原(HBsAg)≤3000 IU/mL、无肝硬化 的成人慢乙肝感染者。
的成人慢乙肝感染者。
国家药品监督管理局药品审评中心指出,该药因符合 “防治重大传染病的创新药” 及 “纳入突破性治疗药物程序” 相关要求,获准进入优先审评,按照国内审评规则,若无意外该药有望于 2026 年内在外我国获批上市。
此前,该药已在日本提交上市申请,预计最快9月在日本获批上市
此前,2026 年 2 月 26 日,GSK836 已向日本厚生劳动省递交上市申请,且因 2024 年 8 月获日本 SENKU(先驱)资格认定,享受审批加速政策,预计最快 2026 年 9 月在日本获批上市。
GSK836 作为一款反义寡核苷酸药物,它区别于传统核苷(酸)类似物仅能抑制病毒复制的局限,通过抑制乙型肝炎病毒DNA的复制,进而抑制血液中乙型肝炎表面抗原 (HBsAg)水平,并刺激免疫系统产生持久应答,为实现功能性治愈奠定基础,打破慢乙肝 “终身服药” 的治疗困境。
(HBsAg)水平,并刺激免疫系统产生持久应答,为实现功能性治愈奠定基础,打破慢乙肝 “终身服药” 的治疗困境。
GSK836往期研究结果如何?
GSK836 的上市申请,依托于B-Well 1(NCT05630807)和 B-Well 2(NCT 05630820)两项全球多中心 III 期临床试验的积极数据,这两项研究共纳入 29 个国家的 1800 余名慢乙肝患者。
III 期临床试验采用每周一次 300mg 皮下注射 + 负荷剂量的治疗方案,总疗程 24 周,以 “停药后 24 周持续 HBsAg 阴转且 HBV DNA 检测不到” 作为功能性治愈的核心判定标准。
结果显示,该药与核苷(酸)类似物联合治疗的功能性治愈率显著高于核苷(酸)类似物单药治疗,基线 HBsAg≤1000 IU/ml 的患者疗效更突出,且药物安全性与耐受性良好,相关详细数据将于 2026 年学术会议公布。
GSK836 在我国拟纳入优先审评,无疑是具有里程碑意义的好消息,为我国乙肝患者追求功能性治愈带来新的治疗方案和选择。
来源:肝博士
 ,助力中国临床决策”是平台的使命。医脉通旗下拥有「临床指南」「用药参考」「医学文献王」「医知源」「e研通」「e脉播」等系列产品,全面满足医学工作者临床决策、获取新知及提升科研效率等方面的需求。
,助力中国临床决策”是平台的使命。医脉通旗下拥有「临床指南」「用药参考」「医学文献王」「医知源」「e研通」「e脉播」等系列产品,全面满足医学工作者临床决策、获取新知及提升科研效率等方面的需求。本平台旨在为医疗卫生专业人士传递更多医学信息。本平台发布的内容,不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议。如该等信息被用于了解医学信息以外的目的,本平台不承担相关责任。本平台对发布的内容,并不代表同意其描述和观点。若涉及版权问题,烦请权利人与我们联系,我们将尽快处理。
