
Military Medical Research | 重塑抗体表位,P2-1肽段通过调控HMGB1-pCTS-L轴协同治疗脓毒症与类风湿关节炎
Metadata Card
文献题目:Repurposing a detrimental antibody epitope as targeted therapeutics for sepsis and rheumatoid arthritis
发表期刊:Military Medical Research
发表时间:26.2.17
影响因子:22.9(中科院1区)
通讯作者/单位:Hai-Chao Wang @ The Feinstein Institutes for Medical Research
一句话总结:研究者将一种能加重脓毒症 的抗四连蛋白(TN)抗体表位改造为P2-1肽段,通过精准阻断HMGB1诱导的pCTS-L分泌,实现了对脓毒症和关节炎的跨疾病治疗。
的抗四连蛋白(TN)抗体表位改造为P2-1肽段,通过精准阻断HMGB1诱导的pCTS-L分泌,实现了对脓毒症和关节炎的跨疾病治疗。
Graphical Abstract

Abstract
背景:脓毒症和类风湿性关节炎 (RA)是不同但机制相关的疾病,通常由失调的炎症反应驱动。在这里,我们探索了一个违反直觉的假设,即来自有害的抗四连蛋白(TN)抗体(mAb9)的表位可能具有不可预见的治疗潜力。
(RA)是不同但机制相关的疾病,通常由失调的炎症反应驱动。在这里,我们探索了一个违反直觉的假设,即来自有害的抗四连蛋白(TN)抗体(mAb9)的表位可能具有不可预见的治疗潜力。
方法:通过将mAb9的表位定位到P2(残基55-70),一个对TN的保护功能至关重要的区域,我们开发了P2-1,一种水溶性衍生物作为靶向治疗。然后,我们采用脓毒症(盲肠结扎和穿刺)和关节炎(胶原抗体诱导的关节炎)的动物模型,通过评估脓毒症存活率、关节炎严重程度、疼痛敏感性和关节组织组织学来评估P2、P2-1和组织蛋白酶原L(PCT-L)中和抗体的治疗效果。同时,我们利用表面等离子体共振(SPR)分析和计算模型来检查P2-1/高迁移率族盒1(HMGB1)的相互作用。最后,我们使用原代人外周血单核细胞(PBMCs)阐明了P2-1对HMGB1诱导的pCTS-L和其他细胞因子和趋化因子释放的影响。
结果:P2-1在脓毒症模型中显著提高存活率并减少全身炎症,在RA模型中减弱关节炎严重程度和疼痛敏感性,即使在疾病发作后进行治疗性给药也是如此。在机制上,P2-1表现出与HMGB1的高亲和力结合,并选择性抑制HMGB1诱导的组织蛋白酶L(Ctsl)mRNA上调和人类免疫细胞的pCTS-L分泌,关键是不干扰其他HMGB1诱导的细胞因子和趋化因子。我们通过证明中和抗体赋予有效的抗关节炎作用,减少关节炎症、疼痛和结构损伤,进一步验证了PCT-L作为治疗靶点。
结论:我们的发现引入了一种范式转变的药物发现策略,将有害抗体作用的见解转化为HMGB1-pCTS-L轴的靶向治疗。这种方法不仅递送P2-1作为有效疗法,而且还将PCT-L确立为炎性疾病如脓毒症和RA中的关键介质。
Background & Problem
背景:脓毒症是急性炎症导致的生命威胁,占全球死亡人数的20%;类风湿关节炎(RA)则是慢性的自身免疫病。两者虽临床表现迥异,但都存在共同的免疫病理机制:炎症介质(如TNF、IL-6)和损伤相关分子模式(DAMPs,如HMGB1)的失调释放。
痛点:
1.临床转化困境:脓毒症的大量临床试验均告失败;
2.现有RA疗法不足:虽然抗TNF疗法(如英夫利昔单抗)是基石,但仍有部分患者无效,且会增加感染风险及产生药物耐受;
3.四连蛋白(TN)的双刃剑作用:研究发现,针对TN不同表位的抗体,有的能救命,有的却能致死(如抗体mAb9),这种“有害”表位背后的机制此前尚未被转化为治疗机会。
Methodology
策略:研究团队采用了“逆向工程”策略,将有害抗体mAb9识别的P2表位合成肽段,并改造为稳定性更好的P2-1,作为“诱饵(Decoy)”竞争性阻断病理过程。
逻辑:
1. 表位映射:锁定有害抗体的作用位点;
2. 药物开发:优化肽段P2-1的水溶性和抗氧化性;
3. 疗效验证:在CLP诱导的脓毒症模型和CAIA诱导的关节炎模型中评估P2-1;
4. 机制解析:通过表面等离振子共振(SPR)、分子对接、RNA-seq和人PBMC培养,探索其对HMGB1-pCTS-L轴的精准调控。
Key Results & Interpretation
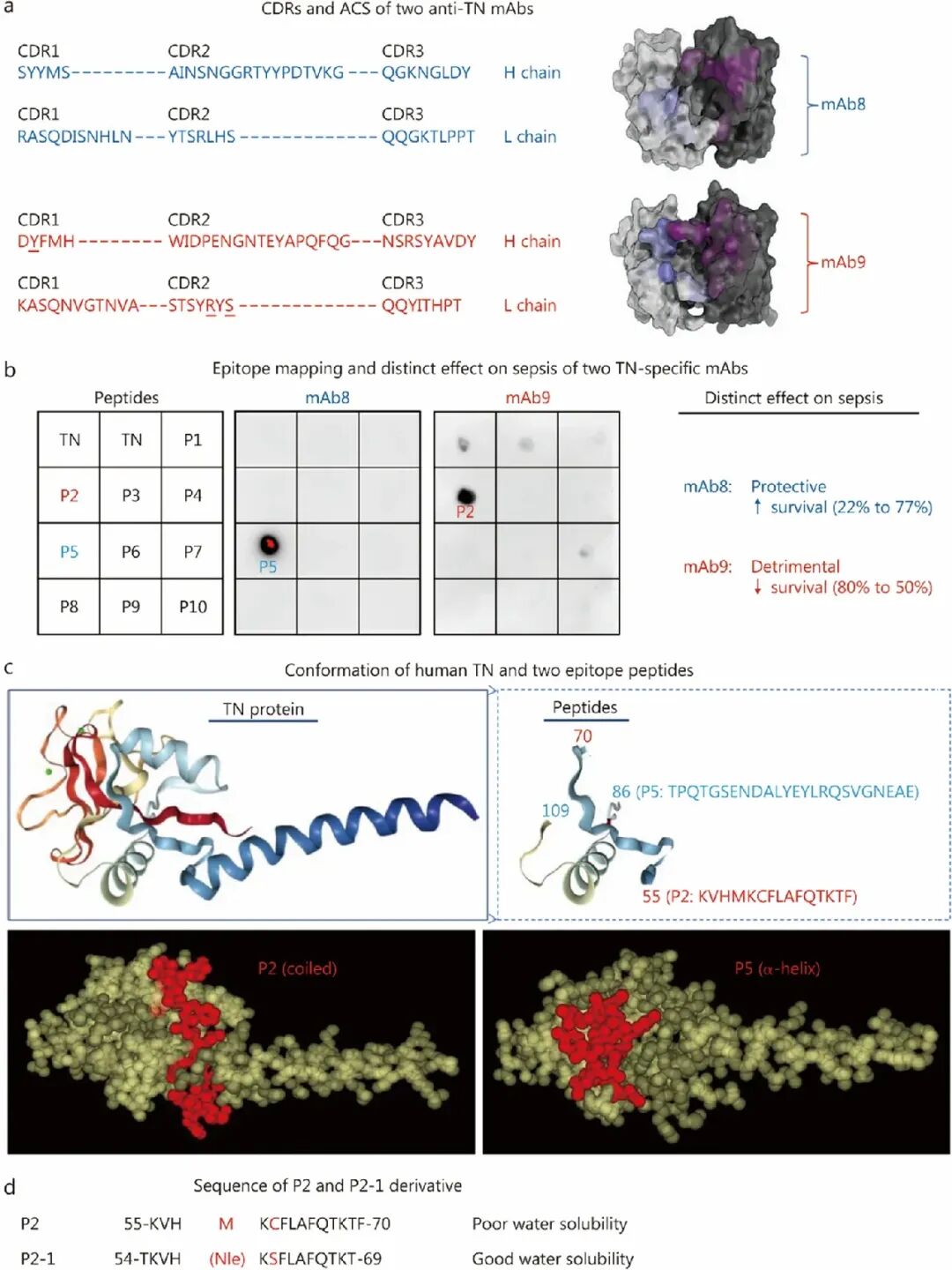
[1A]:通过计算建模预测了两款抗四连蛋白(TN)单克隆抗体的抗原接触结构(ACS),发现保护性抗体 mAb8 呈“洞穴状”结构,而有害抗体 mAb9 呈“沟壑状”结构。
[1B]:系统性点印迹(Dot-blot)实验证实 ,mAb8 靶向 P5 肽段,而有害抗体 mAb9 专门识别 P2 肽段(残基 55-70。
[1C]:结构模型显示 P2 和 P5 是 TN 蛋白表面空间分离且可接触的表位 ,其中 P2 表位在 3D 空间中呈卷曲状。
[1D]:为了提升临床适用性,研究者对 P2 进行了工程化改造:去除 C 端的苯丙氨酸并引入 N 端的苏氨酸以提高水溶性 ,同时用去甲亮氨酸(Nle)和丝氨酸 (S)替换易氧化的氨基酸
(S)替换易氧化的氨基酸 ,最终获得水溶性良好的 P2-1 肽段。
,最终获得水溶性良好的 P2-1 肽段。
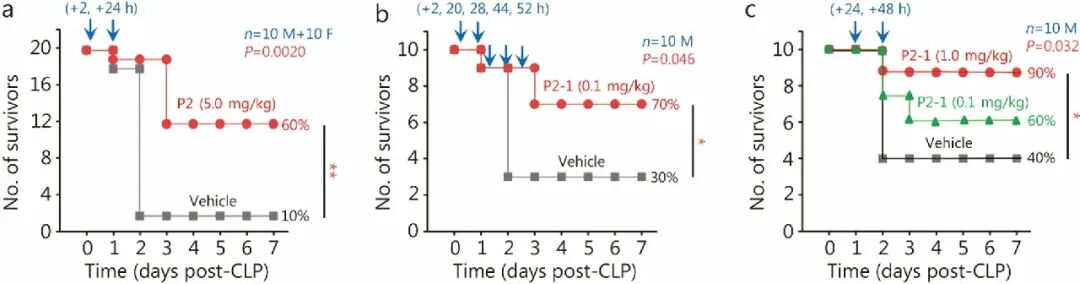
Fig2 [A-B]:在 CLP 脓毒症模型中,重复给予 P2 肽段显著提高了雌雄小鼠的存活率;而低剂量(0.1 mg/kg)的 P2-1 在多个时间点给药同样表现出强效保护作用。
Fig2 [C]:临床转化价值极高的延迟给药实验显示,即便在术后 24 h 和 48 h 才开始干预,1.0 mg/kg 的 P2-1 仍能将存活率从 40% 提升至 90%。
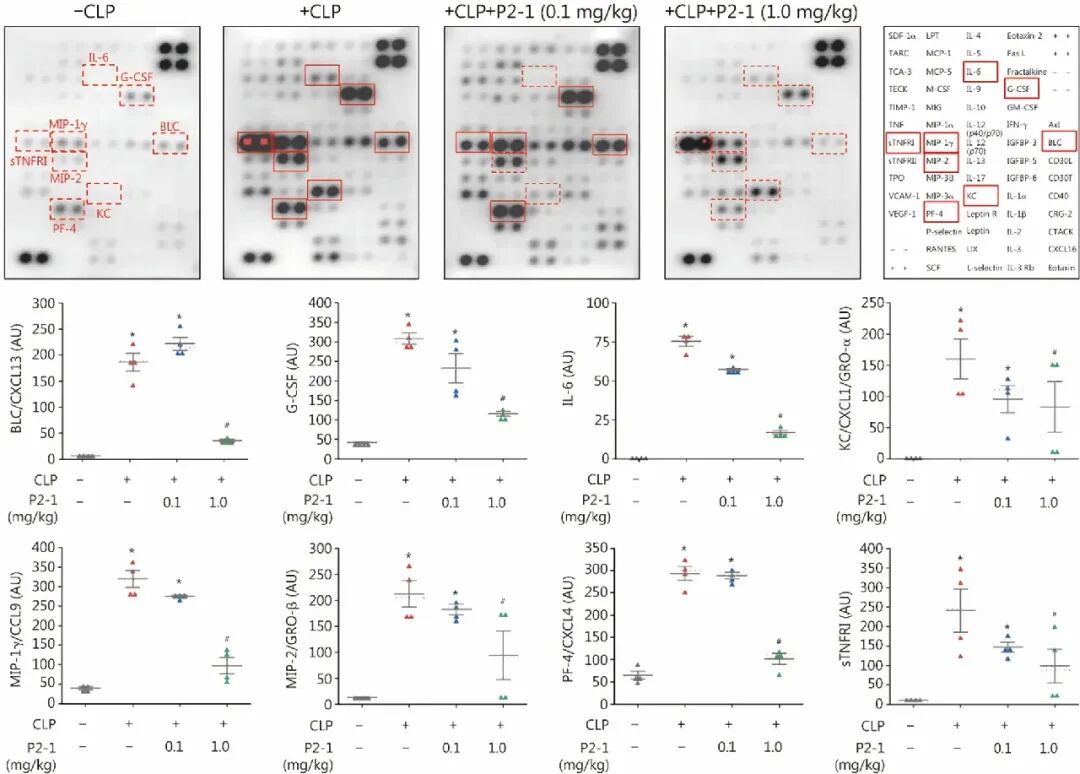
Fig3:细胞因子抗体阵列结果显示,P2-1 处理显著降低了脓毒症诱导的血清促炎介质积累 ,包括 BLC/CXCL13、G-CSF、IL-6、KC、MIP-1γ、MIP-2、PF-4 和 sTNFRI。
发现点3:P2-1 缓解类风湿关节炎的临床进展及局部关节疼痛
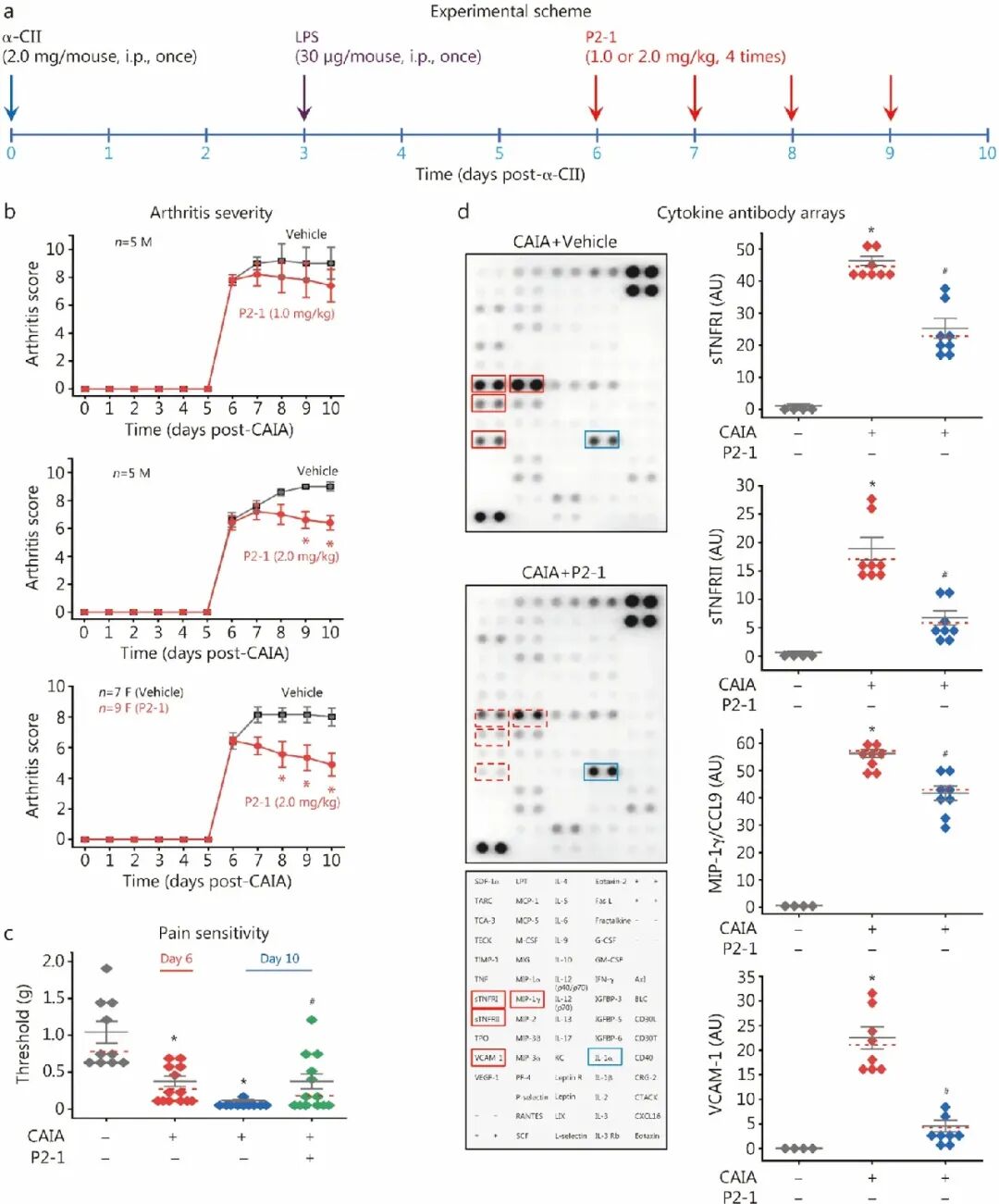
[4A-B]:在疾病建立后的第 6 天开始给药,P2-1 剂量依赖性地减轻了雄性和雌性小鼠的关节炎评分。
[4C]:通过 Von Frey 细丝测试发现,P2-1 显著提升了 CAIA 小鼠受损的机械 withdrawal 阈值,表明其能有效缓解关节相关的炎性疼痛。
[4D]:关节组织裂解液分析证实,P2-1 显著降低了局部 sTNFRI、sTNFRII、MIP-1γ 以及血管细胞黏附分子-1(VCAM-1)的水平。
发现点4:P2-1 与 HMGB1 高亲和力结合并精准阻断 RAGE 介导的内吞
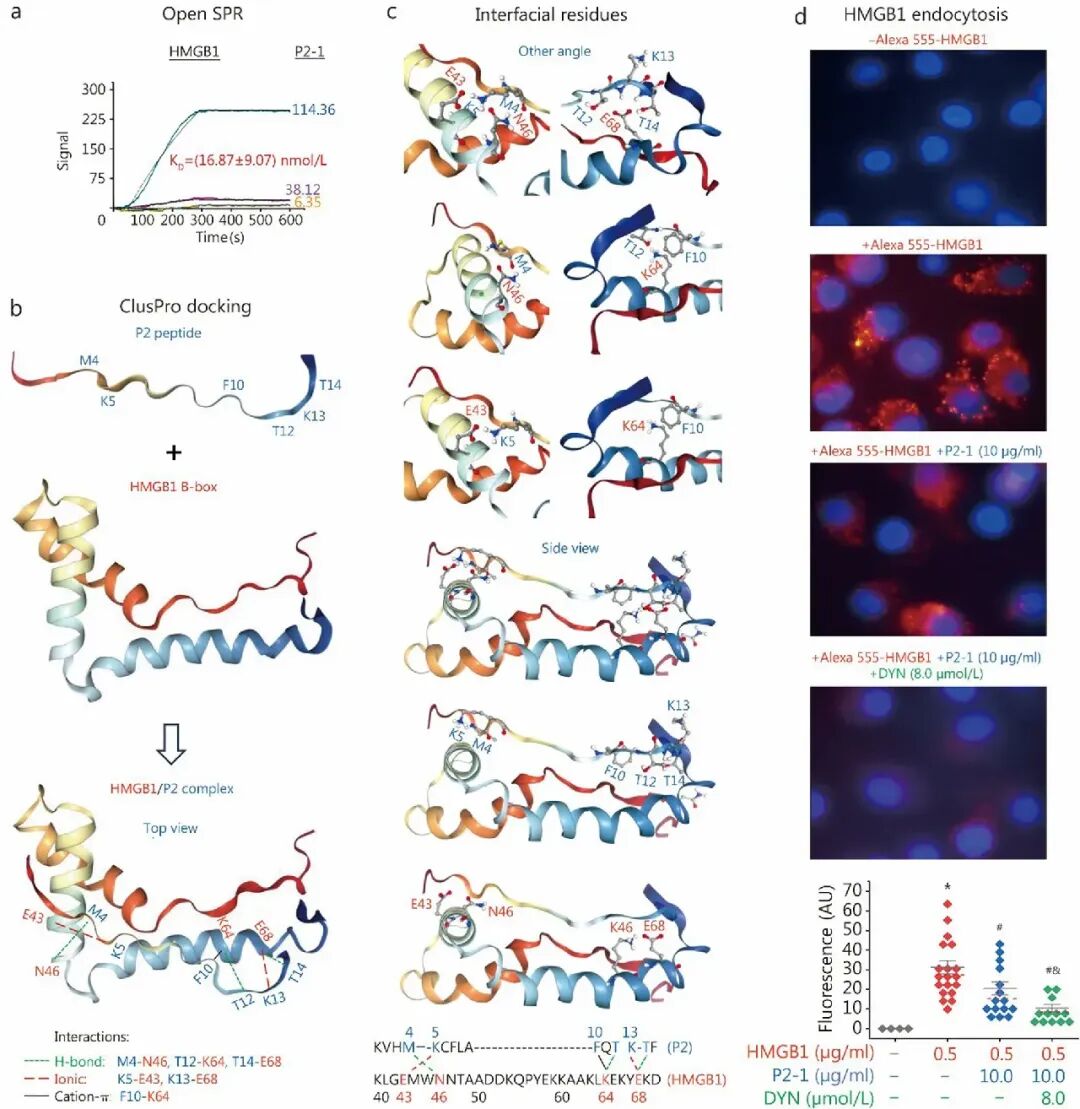
[5A]:表面等离振子共振(SPR)实验测得 P2-1 与 HMGB1 的平衡解离常数(KD)约为 16.87±9.07 nmol/L,证实了两者的高亲和力结合。
[5B-C]:ClusPro 对接模型显示,P2-1 结合在 HMGB1 的 B-box 区域 ,涉及 E43、N46、K64 和 E68 等核心残基 。该结合位点与 RAGE 结合域重叠,但避开了 TLR4 结合域。
[5D]:荧光成像显示,P2-1 处理显著抑制了人巨噬细胞对 Alexa 555 标记的 HMGB1 的摄取,这种抑制作用可被内吞抑制剂 dynasore 进一步增强。
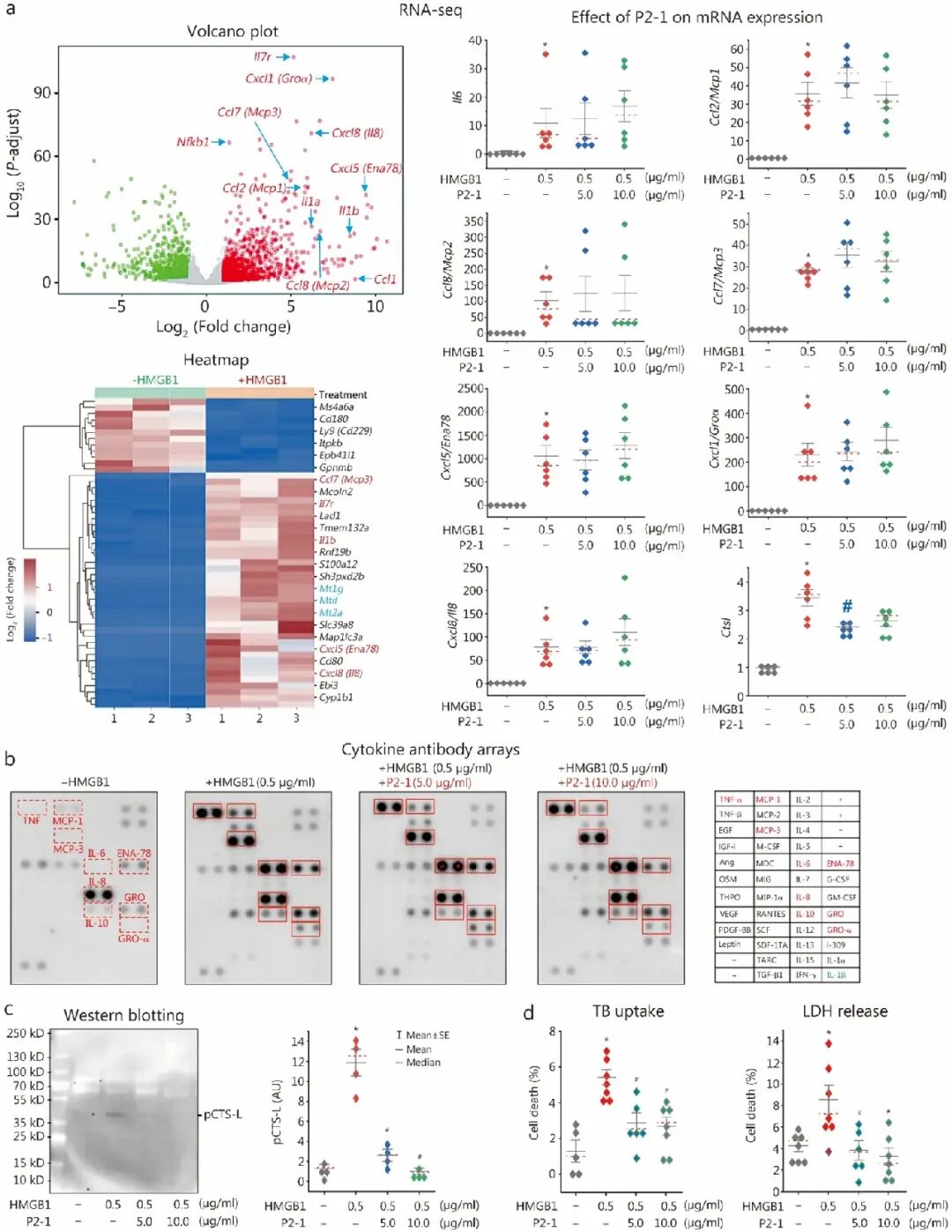
[6A]:RNA-seq 火山图和热图显示,HMGB1 诱导了大量基因表达,但 P2-1 并未广泛逆转这些变化;关键的是,P2-1 显著降低了 Ctsl mRNA 的上调(从 3.4 倍降至 2.4 倍)。
[6B]:细胞因子阵列证实,P2-1 并不抑制 HMGB1 诱导的 TNF、IL-6、IL-8、MCP-1 等常规因子的分泌。
[6C]:Western Blot 结果表现出惊人的特异性:P2-1 呈剂量依赖性地完全阻断了 HMGB1 诱导的组织蛋白酶 L 前体(pCTS-L)的分泌。
[6D]:TB 摄取和 LDH 释放实验证明,P2-1 能显著抑制 HMGB1 诱导的巨噬细胞焦亡,从而保护免疫细胞功能。
发现点6:中和 pCTS-L 可显著减轻关节炎症并逆转骨/软骨侵蚀
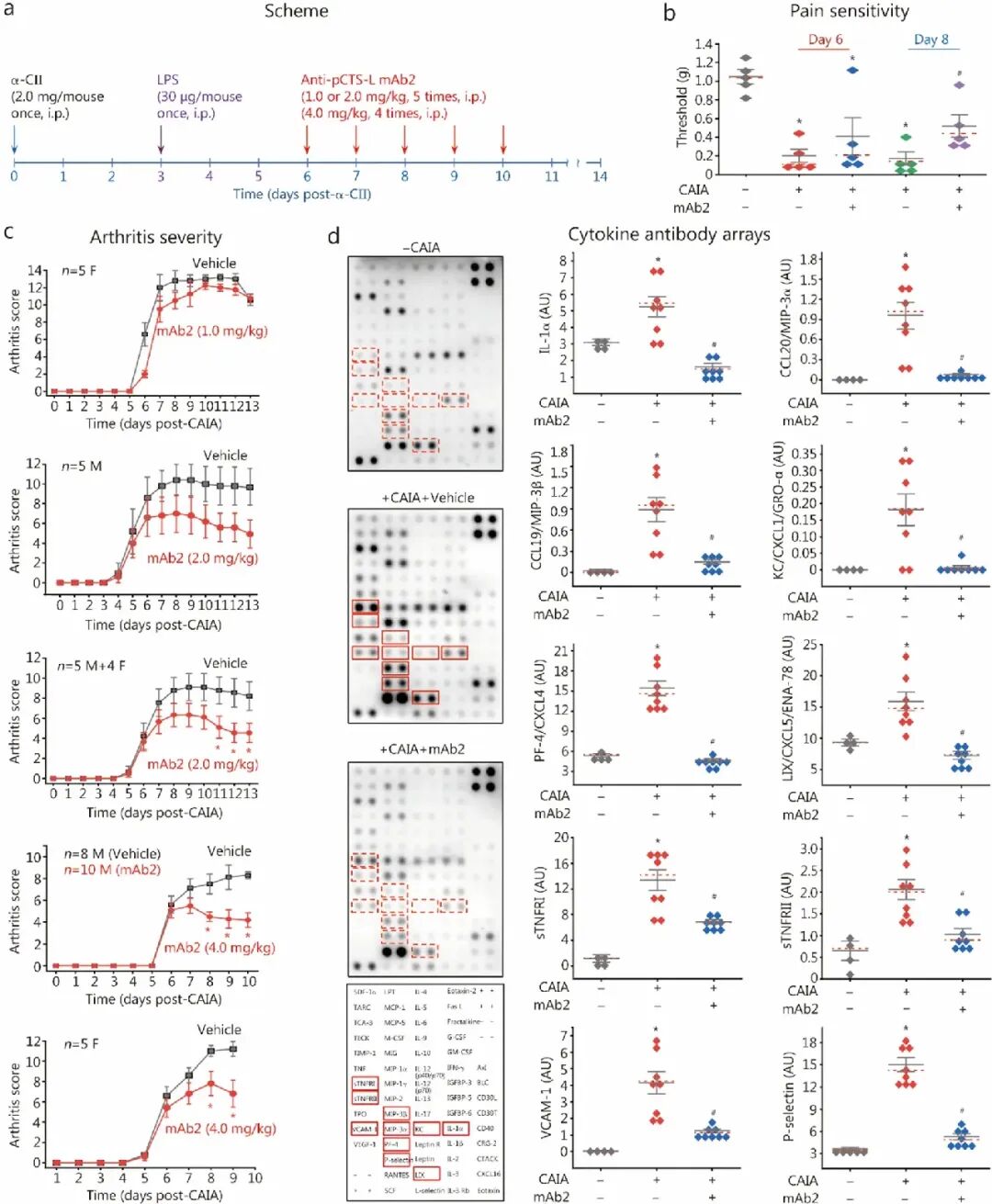
Fig7 [B-C]:给予 pCTS-L 中和抗体 mAb2 显著恢复了 CAIA 小鼠的痛觉 阈值,并大幅降低了关节炎临床评分。
阈值,并大幅降低了关节炎临床评分。
Fig7 [D]:mAb2 治疗降低了关节局部多种趋化因子(如 CCL20/MIP-3α、LIX/CXCL5)和黏附分子(P-selectin、VCAM-1)的表达。
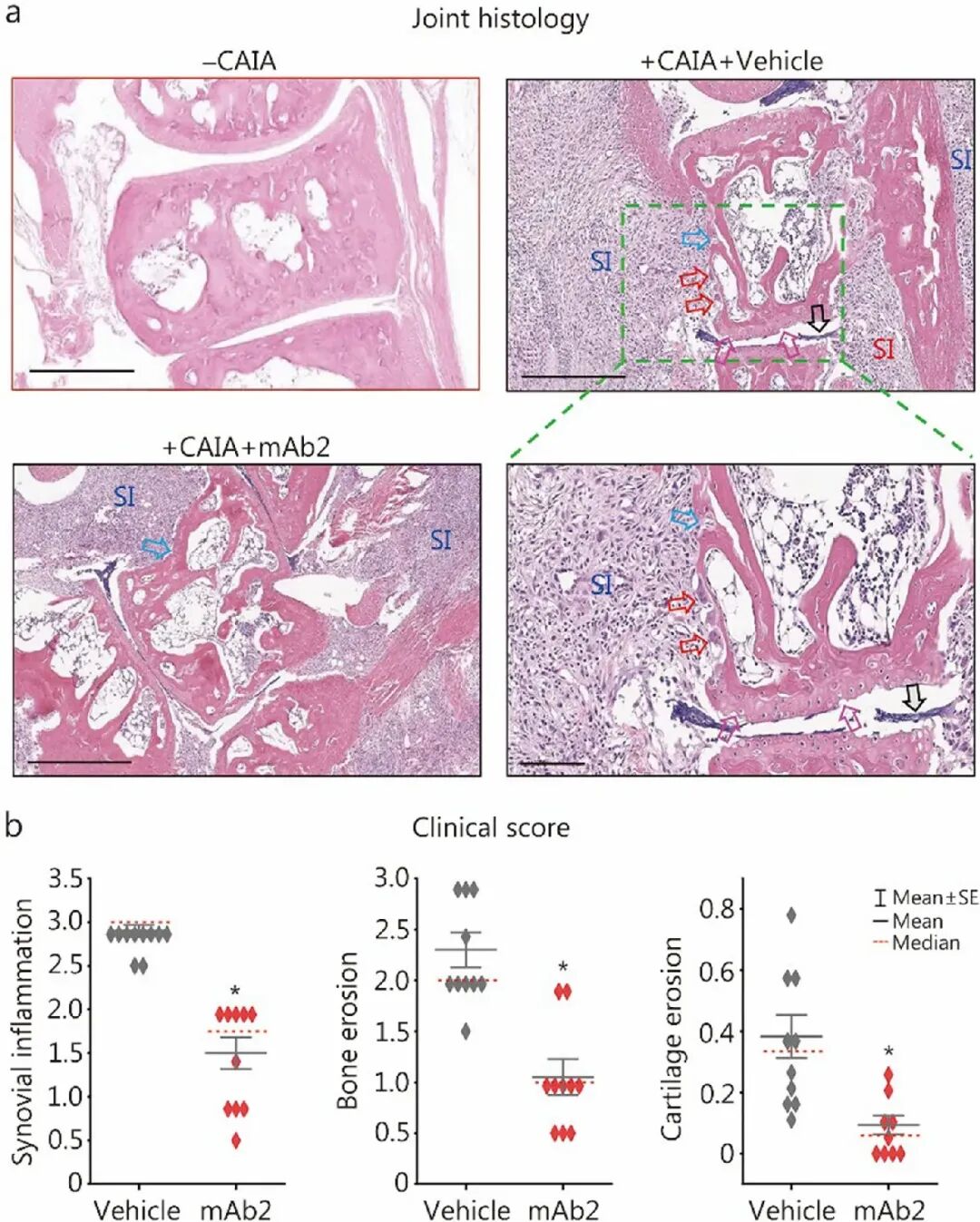
Fig8 [A]:H&E 染色显示,模型组存在严重的滑膜增生、炎性细胞浸润及侵略性“血管翳(pannus)”结构;而 mAb2 治疗组的关节结构完整,骨表面破骨细胞聚集(红箭)和骨侵蚀(蓝箭)显著减少。
Fig8 [B]:临床评分定量分析证实,mAb2 在滑膜炎症、骨侵蚀及软骨侵蚀三个维度上均达到了统计学显著的改善效果。
Innovation & Takeaway
✨ 创新点
1. 首次将导致脓毒症恶化的抗体表位“废物利用”,设计成高效治疗肽;
2. 发现了HMGB1-pCTS-L这一全新的病理轴心,并证明其在急慢性炎症中具有普适性;
3. P2-1具有“病理激活”特性,仅在HMGB1释放的炎症部位起效,且不干扰基础免疫(TLR4轴),安全性优于传统免疫抑制剂。
✨ 科研启示
实验中观察到的“有害”现象往往隐藏着更深层次的机制。对致死抗体表位的深入解析,可以转化为极其精准的Decoy分子。
✨ 临床/应用价值
pCTS-L作为脓毒症的晚期介质及RA的致病因子,其靶点价值已被充分肯定。P2-1肽段有望成为下一代兼顾疗效与安全性的炎症调节药物。目前已有相关专利布局,值得产业界关注。
局限性
首先,主要的治疗证据,特别是脓毒症和关节炎的生存/改善数据,完全依赖于高度标准化的盲肠结扎穿刺(CLP)和胶原抗体诱导型关节炎(CAIA)小鼠模型,这些模型无法完全模拟人类相关疾病极其复杂的病理生理异质性,因此临床转化存在不确定性。
作为一种小分子肽段,P2-1可能面临体内代谢稳定性差、半衰期短以及潜在的免疫原性问题,这可能限制其作为临床药物的可行性,除非进行进一步的配方优化或结构改造。
虽然研究强调了P2-1的高度选择性(只抑制pCTS-L而不影响其他因子),但在脓毒症这种由于多重炎症因子风暴导致的多器官衰竭复杂疾病中,仅拦截单一通路(HMGB1-pCTS-L轴)是否足以逆转病情,其疗效可能不及在小鼠模型中看到的那么显著。
医脉通是专业的在线医生平台,“感知世界医学脉搏,助力中国临床决策”是平台的使命。医脉通旗下拥有「临床指南」「用药参考」「医学文献王」「医知源」「e研通」「e脉播」等系列产品,全面满足医学工作者临床决策、获取新知及提升科研效率等方面的需求。
