
重磅!7.2mg司美格鲁肽获FDA批准上市,平均狂甩21%体重,但有一点需要特别留意
2026年3月19日,美国食品药品监督管理局(FDA)正式批准诺和诺德(Novo Nordisk)公司的新型高剂量司美格鲁肽 注射液(Wegovy HD,7.2 mg)上市,结合低热量饮食和增加体力活动,帮助肥胖成年患者实现并维持体重减轻。前提是患者已经能够耐受2.4 mg剂量的Wegovy至少4周,并且在临床上具有进一步减重的需求。同时需警惕:皮肤感觉异常(Dysesthesia)风险激增。
注射液(Wegovy HD,7.2 mg)上市,结合低热量饮食和增加体力活动,帮助肥胖成年患者实现并维持体重减轻。前提是患者已经能够耐受2.4 mg剂量的Wegovy至少4周,并且在临床上具有进一步减重的需求。同时需警惕:皮肤感觉异常(Dysesthesia)风险激增。

STEP UP试验数据分析 Wegovy HD的获批主要基于名为“STEP UP”的3b期随机、双盲、安慰剂对照临床试验结果。该试验共纳入1,407名无糖尿病 的肥胖成年患者(BMI≥30 kg/m²),在生活方式干预的基础上,对比了每周一次7.2 mg司美格鲁肽、2.4 mg司美格鲁肽与安慰剂的疗效差异。
的肥胖成年患者(BMI≥30 kg/m²),在生活方式干预的基础上,对比了每周一次7.2 mg司美格鲁肽、2.4 mg司美格鲁肽与安慰剂的疗效差异。

随访72周后的数据显示,Wegovy HD(7.2 mg)在减重效果上展现出显著优势:
平均体重降幅:在假设所有患者均坚持治疗的理想情况(疗效评估值,Efficacy estimand)下,7.2 mg组的平均体重降幅高达约21%(20.7%),而2.4 mg组为约18%(17.5%),安慰剂组仅为约2%(2.4%)。即使在包含所有患者实际治疗情况(治疗方案评估值)的分析中,7.2 mg组也达到了约19%(18.8%)的减重效果。
深度减重达标率:在7.2 mg组中,高达31.2%的患者实现了25%或以上的体重减轻,这意味着一个200多斤的人,平均能减掉50斤左右;而2.4 mg组这一比例为15.3%,安慰剂组为0。
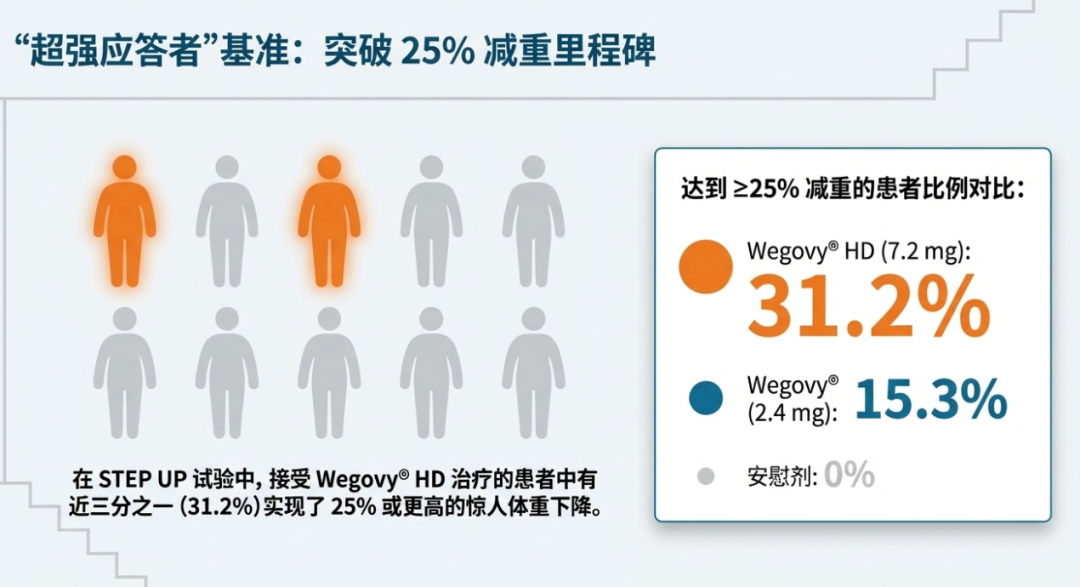
图 实现体重减轻≥25%的比例
随着药物剂量的提升,其安全性图谱也出现了一些值得关注的变化。
Wegovy HD最常见的不良反应依然包括恶心、呕吐 、便秘
、便秘 、腹痛、疲劳和脱发等。 然而,感觉异常(Dysesthesia)这一不良事件的发生率在高剂量组中明显升高。
、腹痛、疲劳和脱发等。 然而,感觉异常(Dysesthesia)这一不良事件的发生率在高剂量组中明显升高。
临床数据显示,高达22%接受Wegovy HD治疗的患者报告了皮肤感觉改变的临床症状(如皮肤敏感、感觉过敏、感觉异常和感觉麻木等),这一发生率显著高于2.4 mg组的6%和安慰剂组的0.3%。
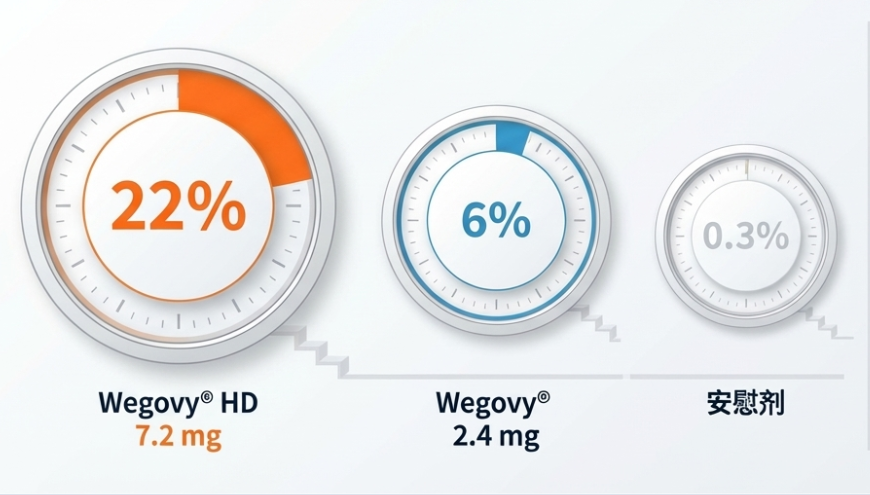
图 皮肤感觉异常事件发生率
此外,基于动物模型研究,该药物依然带有关于潜在甲状腺C细胞肿瘤(包括甲状腺髓样癌,MTC)的黑框警告,具有此类疾病个人或家族史的患者禁用此药。
肥胖被医疗界广泛认为是一种需要长期管理的复杂、慢性及进行性疾病,受遗传、生物学和环境等多种因素驱动,而非单纯的“意志力薄弱”问题。阿拉巴马大学伯明翰分校糖尿病研究中心主任W. Timothy Garvey博士指出,Wegovy HD为肥胖管理提供了一个重要的新工具,其展现出的突破性减重效果有望重塑医疗专业人员对患者临床结局的期望。
据悉,该高剂量注射液将于今年4月通过全美超过7万家药房及相关渠道正式供应,为遭遇减重瓶颈的肥胖患者提供更为强效的干预手段。
参考文献
本视频/资讯/文章的内容不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议。医脉通是专业的在线医生平台,“感知世界医学脉搏 ,助力中国临床决策”是平台的使命。医脉通旗下拥有「临床指南」「用药参考」「医学文献王」「医知源」「e研通」「e脉播」等系列产品,全面满足医学工作者临床决策、获取新知及提升科研效率等方面的需求。
,助力中国临床决策”是平台的使命。医脉通旗下拥有「临床指南」「用药参考」「医学文献王」「医知源」「e研通」「e脉播」等系列产品,全面满足医学工作者临床决策、获取新知及提升科研效率等方面的需求。
