
魏蕊教授:胰岛局部GLP-1系统——血糖稳态调控的核心靶点与机制解析 | 2026北大论坛分享会(昆明站)
2026年3月14日,由《中国糖尿病杂志》和云南省药学会共同主办的“2026北大糖尿病论坛学术分享会暨多民族代谢疾病研究交流会(第二季)”在昆明隆重举行。本次会议秉承“科学至上,学术独立”的宗旨,汇聚多民族地区的糖尿病领域专家,围绕代谢疾病研究前沿、多民族人群特点及胰高糖素样肽-1(GLP-1)类药物应用等热点议题展开深入交流,为推动我国糖尿病防治事业发展注入新动力。

在本次大会上,北京大学第三医院魏蕊教授以《胰岛局部GLP-1系统在血糖稳态调控中的作用》为题发表精彩学术演讲,魏蕊教授从基础研究角度揭示了胰岛内源性GLP-1系统的重要功能,为理解GLP-1类药物的作用机制提供了新视角。会后,魏蕊教授接受医脉通专访,就相关议题分享了深入见解。
(一)胰岛素单药治疗1型糖尿病 的不足
的不足
1921年,胰岛素的发现开启了糖尿病治疗的新纪元,被誉为“糖尿病领域的伟大发现”(图1)。

图1 糖尿病领域的伟大发现——胰岛素
然而,胰岛素单药治疗对于1型糖尿病(T1D)患者而言并非完美。即使接受胰岛素治疗,T1D患者的血糖仍然较健康个体有较大波动,且美国大型登记研究(n=16,061)显示,不同年龄段T1D患者的糖化血红蛋白 达标率均较低,仅14%~30%,以上均提示机体内存在其他激素参与了糖尿病的发生发展。
达标率均较低,仅14%~30%,以上均提示机体内存在其他激素参与了糖尿病的发生发展。
(二)胰高糖素参与糖尿病的发生发展
胰岛α细胞约占小鼠胰岛细胞的15%~20%,人类胰岛中α细胞占比更高,约为30%~50%,其分泌的胰高糖素(Glucagon)是调控血糖的重要机制之一。胰高糖素参与糖尿病进展:T1D儿童发病5年内胰高糖素水平升高与高血糖 密切相关;胰高糖素受体(GCGR)敲除可避免链脲佐菌素(STZ,特异性破坏β细胞)诱导的T1D,证实GCGR参与T1D的进展(图2)。
密切相关;胰高糖素受体(GCGR)敲除可避免链脲佐菌素(STZ,特异性破坏β细胞)诱导的T1D,证实GCGR参与T1D的进展(图2)。
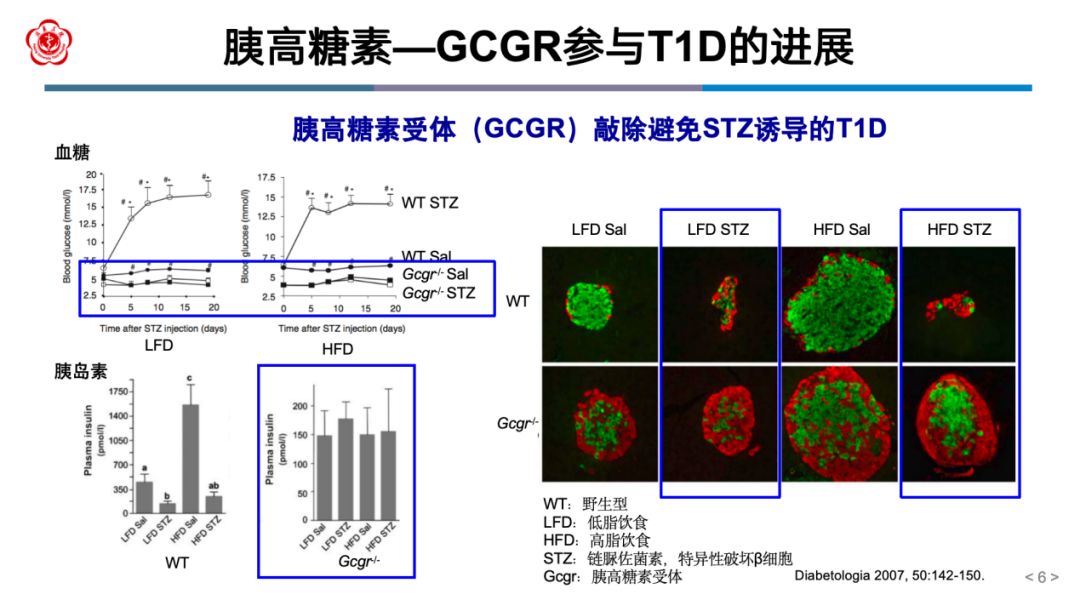
图2 胰高糖素—GCGR参与T1D的进展
(三)胰高糖素中心论与双激素调控学说
美国科学院院士Roger H. Unger提出的“胰高糖素中心论”,以及后续学术界逐渐认可胰岛素与胰高糖素的“双激素调控学说”,明确了胰高糖素在糖尿病发生发展中的重要地位。
(四)阻断GCGR降低糖尿病模型小鼠与患者的血糖
动物实验 证实,GCGR单克隆抗体可降低多种模型小鼠的血糖水平(图3)。I期和II期临床研究已证实,GCGR单抗在减少T1D患者胰岛素用量的同时,还能降低平均血糖和糖化血红蛋白水平。
证实,GCGR单克隆抗体可降低多种模型小鼠的血糖水平(图3)。I期和II期临床研究已证实,GCGR单抗在减少T1D患者胰岛素用量的同时,还能降低平均血糖和糖化血红蛋白水平。
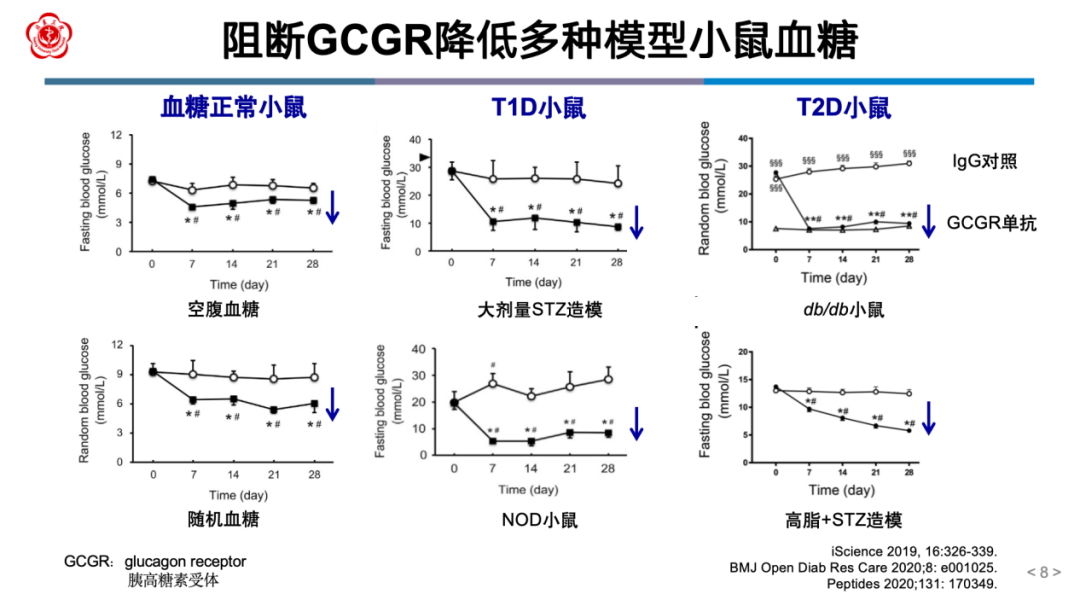
图3 阻断GCGR降低多种模型小鼠血糖
(五)阻断GCGR促进胰岛β细胞再生
进一步研究表明,阻断GCGR可增加T1D和T2D小鼠的β细胞总量、胰岛数量及面积。此外,一项研究评估了GCGR单抗在T1D啮齿动物中维持血糖稳态的潜力。研究发现,在经过4周的GCGR抗体治疗后停药4周,小鼠的血糖持续保持低水平,胰岛素持续保持高水平。此外,停药后仍能维持胰岛β细胞总量,具备葡萄糖 和精氨酸
和精氨酸 刺激的促胰岛素分泌能力,表明阻断GCGR后再生的β细胞是有功能的(图4)。
刺激的促胰岛素分泌能力,表明阻断GCGR后再生的β细胞是有功能的(图4)。
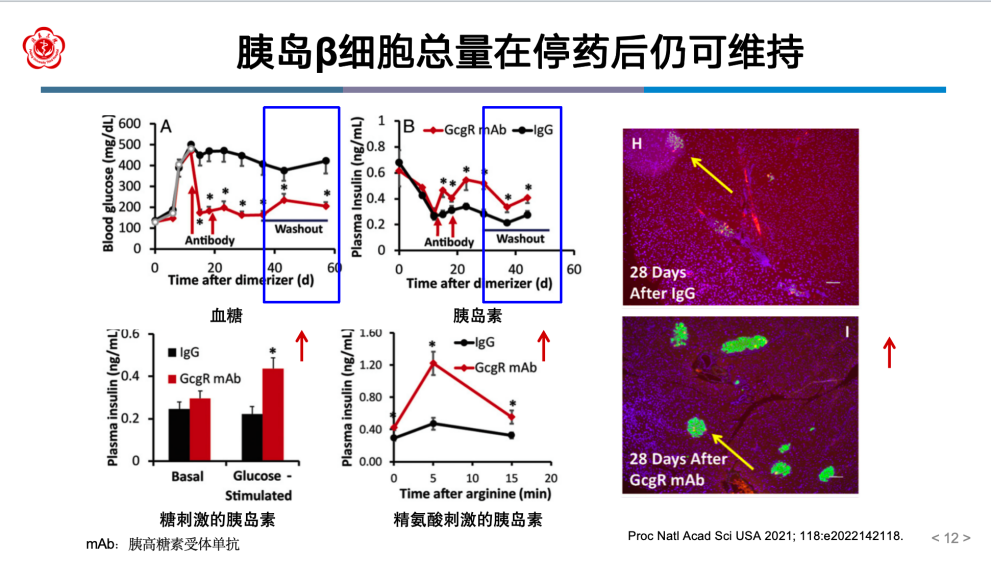
图4 胰岛β细胞总量在停药后仍可维持
综上,阻断GCGR可降低多种T1D和T2D模型动物及患者的血糖,同时促进糖尿病胰岛β细胞的再生,是糖尿病治疗的重要策略,而其促进β细胞再生的潜在机制,成为后续研究的核心方向。
(一)GLP-1的作用优势
进一步研究表明,阻断GCGR可增加循环GLP-1水平、肠道GLP-1生成和分泌。研究者对GLP-1与GCGR信号之间的调控关系进行了深入分析,若敲除GLP-1R,GCGR单抗的降糖与β细胞保护作用消失,提示GLP-1是介导GCGR阻断发挥降糖作用及促进β细胞再生的关键效应分子。
GLP-1对胰岛β细胞具有多重保护效应,主要体现在以下三个方面:一是改善β细胞功能,包括促进胰岛素基因表达和生物合成、促进胰岛素原 向胰岛素剪切、增强胰岛素分泌,提高葡萄糖刺激下的胰岛素释放效率;二是维持β细胞数量稳定,包括促进细胞增殖、促进干细胞分化、抑制凋亡与坏死等,从而保障胰岛β细胞池结构与功能的完整性(图5)。
向胰岛素剪切、增强胰岛素分泌,提高葡萄糖刺激下的胰岛素释放效率;二是维持β细胞数量稳定,包括促进细胞增殖、促进干细胞分化、抑制凋亡与坏死等,从而保障胰岛β细胞池结构与功能的完整性(图5)。
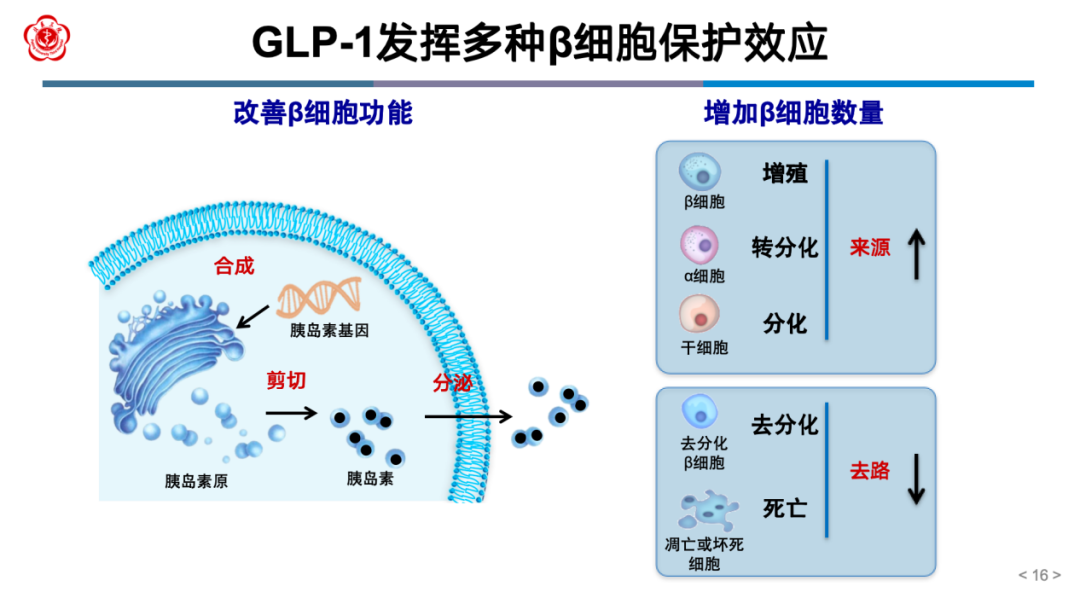
图5 GLP-1发挥多种β细胞保护效应
(二)GLP-1的天然局限
天然GLP-1在体内易被快速降解:二肽基肽酶4(DPP-4)在机体广泛表达,可快速切割GLP-1分子,导致GLP-1半衰期仅2-3分钟。肠道来源的GLP-1无法以高浓度持续直接作用于胰岛β细胞。这些事实提示,胰岛局部可能存在内源性GLP-1系统,该系统或许是血糖调控的核心所在。
(三)GLP-1的胰腺局部生成:α细胞为核心来源,多种降糖药物促进α细胞GLP-1生成
GLP-1的生成并非仅局限于肠道,近年来研究发现,胰岛α细胞是内源性GLP-1的核心产生部位之一(图6)。多种降糖药物可通过调控α细胞促进GLP-1的生成:
lGLP-1受体激动剂(GLP-1RA):研究证实,利拉鲁肽 可促进人胰岛和小鼠胰岛α细胞的GLP-1生成,增加胰岛GLP-1的表达与活性,提示临床常用GLP-1RA可能通过调节α细胞功能增强疗效。
可促进人胰岛和小鼠胰岛α细胞的GLP-1生成,增加胰岛GLP-1的表达与活性,提示临床常用GLP-1RA可能通过调节α细胞功能增强疗效。
lSGLT2抑制剂:研究证实,SGLT2抑制剂达格列净 能增加原代小鼠胰岛及α细胞系中GLP-1的含量与分泌。
能增加原代小鼠胰岛及α细胞系中GLP-1的含量与分泌。
(四)促进α细胞GLP-1生成的内、外源性策略
体内外的多种生理病理因素及干预手段亦可促进α细胞GLP-1生成(图6)。
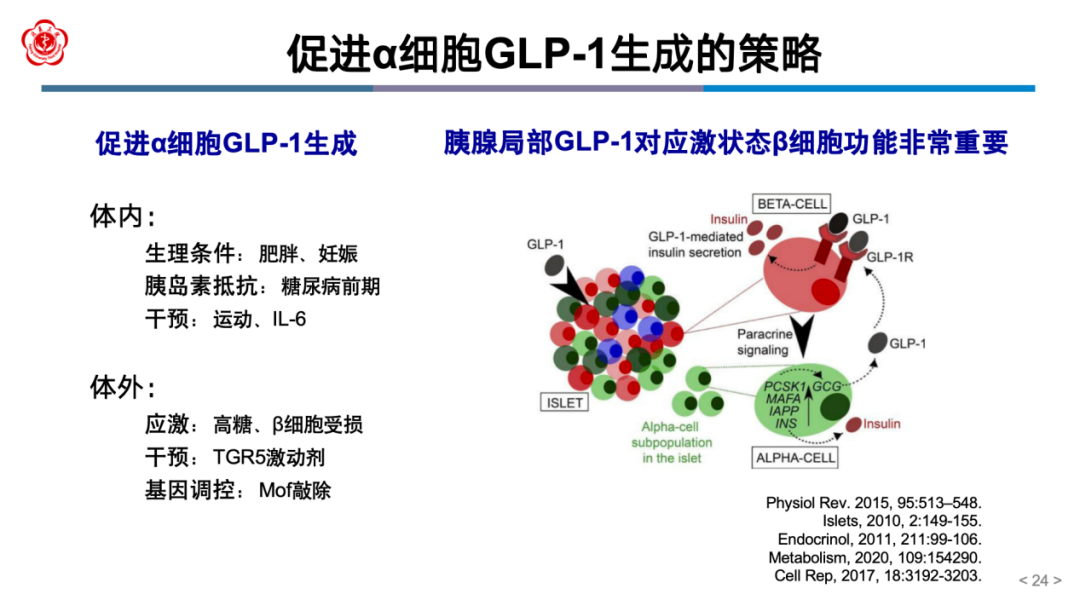
图6 促进α细胞GLP-1生成的策略
此外,胰高糖素除激活GCGR外,还可激活GLP-1受体,因此在胰岛局部存在胰高糖素/GLP-1两个配体对GLP-1受体的激活,两个通路参与胰岛再生和β细胞功能调控(图7)。胰岛局部GLP-1系统成为血糖稳态调控的核心环节,而调控α细胞GLP-1分泌的具体机制,成为进一步研究的重点。
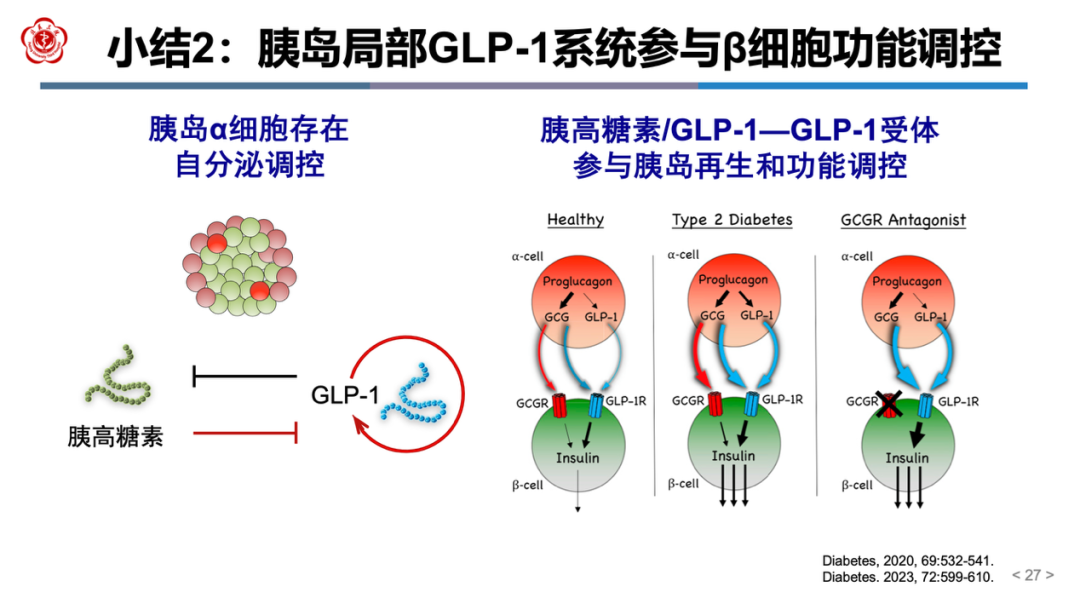
图7 胰岛局部GLP-1系统总结
(一)Fam3a在胰岛α细胞中的表达与功能
魏蕊教授团队的研究揭示了Fam3a的关键作用。首先,动物实验显示,在全身敲除Fam3a的小鼠中,小鼠胰腺和血浆中的活性GLP-1水平升高(图8)。其次,利用人类胰岛单细胞测序和转录组测序的数据库分析证实,人类α细胞中FAM3A与PCSK1(编码PC1/3,一种可将胰高糖素原剪切加工为活性GLP-1的关键酶)表达水平之间呈负相关,提示FAM3A下调可能促进人类α细胞产生GLP-1。
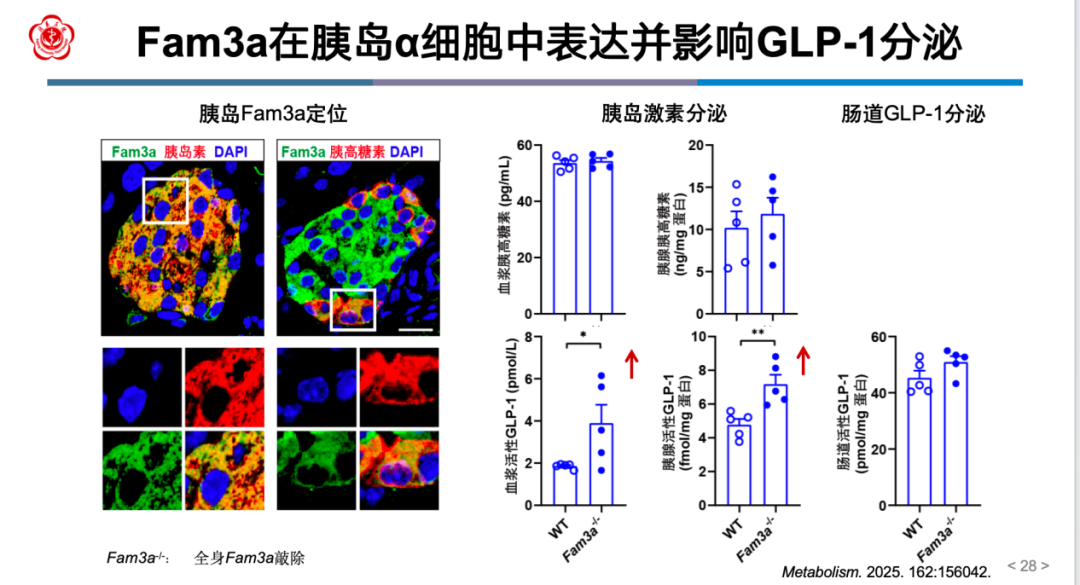
图8 Fam3a在胰岛α细胞中表达并影响GLP-1分泌
(二)Fam3a缺失改善β细胞功能与血糖稳态
随后,魏蕊教授团队通过构建胰岛α细胞特异性Fam3a敲除小鼠开展系列动物实验。结果显示,无论是在正常生理条件下,还是在高脂饮食和糖尿病两种代谢应激模型中,α细胞Fam3a缺失均可上调胰岛来源的GLP-1、增加血浆胰岛素水平(图9)。进一步添加GLP-1受体拮抗剂证实,α细胞来源的GLP-1通过旁分泌作用促进β细胞分泌胰岛素,进而在正常生理条件和代谢应激状态下改善葡萄糖代谢。
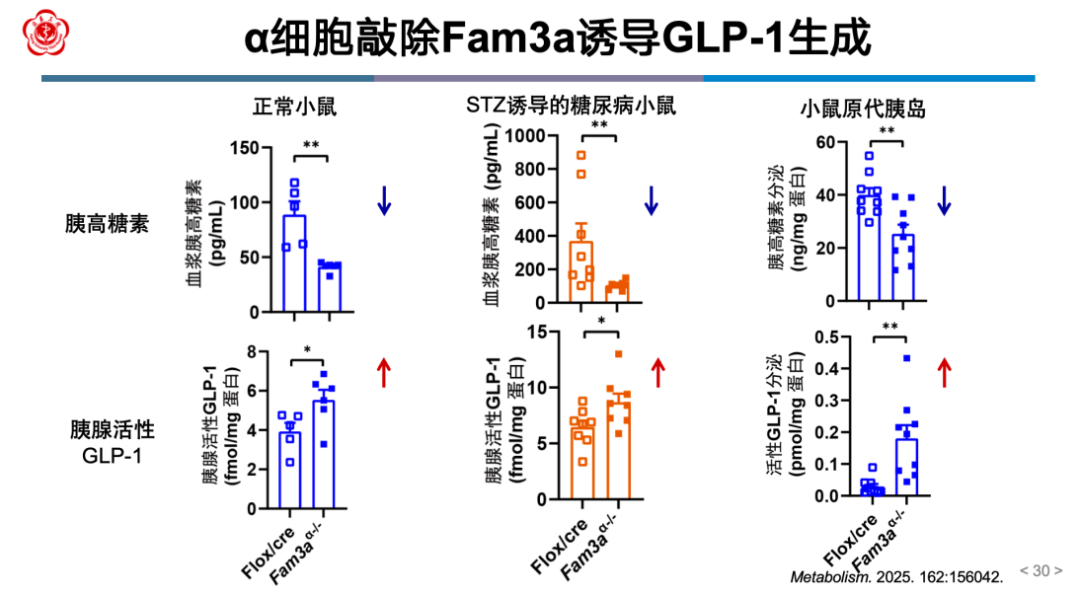
图9 α细胞敲除Fam3a诱导GLP-1生成
(三)Fam3a缺失促进α细胞产生GLP-1的机制
最后,为探究Fam3a缺失促进α细胞产生GLP-1的机制,魏蕊教授团队在胰岛α细胞中利用Fam3a基因过表达或敲减实验、转录组测序、免疫共沉淀、核转位检测、基因截短或点突变技术、双荧光素酶报告基因分析等一系列体外实验证实,Fam3a通过上调Nr4a2促进Foxa2核转位,Nr4a2与Foxa2两者形成蛋白复合体,作用于Pcsk1启动子的特定结合位点,从而抑制Pcsk1的转录活性。上述结果提示,在胰岛α细胞中,Fam3a通过Nr4a2-Foxa2-PC1/3轴调控α细胞来源的GLP-1产生,进而以旁分泌方式改善β细胞功能(图10)。
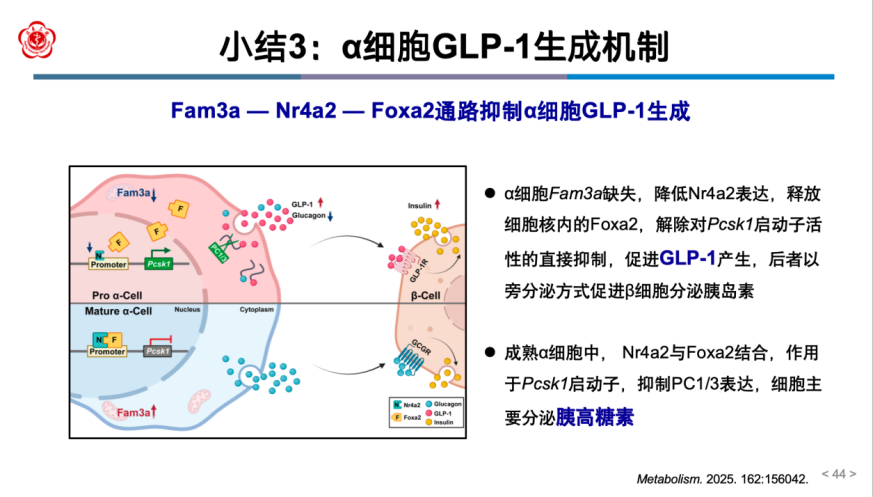
图10 α细胞GLP-1生成机制
胰高糖素的核心调控地位:胰高糖素是机体血糖调控的重要激素,阻断胰高糖素通路可降低多种T1D和T2D动物及患者的血糖,阻断胰高糖素受体还可促进胰岛β细胞再生,为糖尿病治疗提供了重要靶点。
胰岛α细胞的自分泌调控:胰岛α细胞存在激素分泌的自调控机制,GLP-1可正反馈促进自身分泌,胰高糖素受体阻断可促进GLP-1分泌,且胰高糖素/GLP-1可激活胰岛GLP-1受体,参与胰岛再生与β细胞功能调控。
α细胞GLP-1分泌的分子调控:Fam3a—Nr4a2—Foxa2通路是α细胞激素分泌的重要调控方式,为胰岛局部GLP-1系统的精准调控提供了分子基础。
魏蕊 教授
北京大学第三医院内分泌科研究员、博导、学术带头人后备人选
兼任中华医学会内分泌学分会青委、中国生物化学与分子生物学代谢分会青年副主委、北京医学会糖尿病学分会委员等
牵头科技创新2030青年科学家项目,主持国家自然科学基金(5项)等国家及省部级课题20余项
荣获北京市科技进步奖、中国胰岛素分泌研究新星奖等
申报国际/国家发明专利5项,获得授权3项
以第一/通讯作者发表论文60余篇,其中在Diabetes、Diabetologia、Molecular Cancer(IF=33.9,高被引)等SCI发表论文41篇
兼任Cardiovascular Diabetology副主编、Chronic Diseases and Translational Medicine编委、中国糖尿病杂志编委等
Cell Metabolism、Diabetologia、Signal Transduction and Targeted Therapy、Thyroid、中华糖尿病杂志等审稿专家
本视频/资讯/文章的内容不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议。医脉通是专业的在线医生平台,“感知世界医学脉搏,助力中国临床决策”是平台的使命。医脉通旗下拥有「临床指南」「用药参考」「医学文献王」「医知源」「e研通」「e脉播」等系列产品,全面满足医学工作者临床决策、获取新知及提升科研效率等方面的需求。

