
抗癌治疗中,用激素到底是好是坏?——重新审视肝癌免疫治疗中的“预防性激素”策略
前言
introduction
本专栏旨在汇聚国内外肝癌治疗领域的最新科研成果与临床实践,深度聚焦钇-90微球介入治疗这一前沿技术,为肝癌患者及医疗专业人士搭建一座信息交流的桥梁。


对于肝癌患者,免疫治疗(特别是“双免疫”组合)在带来更强疗效的同时,也伴随着更高的严重副作用风险。长期以来,医生们因担心影响疗效而不敢在免疫治疗前使用激素。但一项发表在Journal of Hepatology(IF:33)上的专家观点提出:是时候打破这个禁忌了[1]。本文将带您了解这一重要的理念转变。
01
肝细胞癌 是一种难治的肿瘤。近年来,以PD-1/PD-L1抑制剂为代表的免疫检查点抑制剂,尤其是联合使用CTLA-4抑制剂(如伊匹木单抗
是一种难治的肿瘤。近年来,以PD-1/PD-L1抑制剂为代表的免疫检查点抑制剂,尤其是联合使用CTLA-4抑制剂(如伊匹木单抗 )的“双免疫”疗法,显著提高了治疗效果,为许多无法手术的肝癌患者带来了新希望[2-4]。
)的“双免疫”疗法,显著提高了治疗效果,为许多无法手术的肝癌患者带来了新希望[2-4]。
然而,希望伴随着风险,更强的疗效往往意味着更高的副作用风险。在肝癌患者中,由于很多人本身就有肝硬化 或肝功能储备不足,他们更难耐受严重的治疗相关不良事件,特别是免疫相关不良事件。
或肝功能储备不足,他们更难耐受严重的治疗相关不良事件,特别是免疫相关不良事件。
以“CheckMate 9DW”方案(伊匹木单抗联合纳武利尤单抗 )为例,其有效率高达36%,但严重的(3级及以上)治疗相关不良事件发生率也达到了41%[5]。这意味着超过三分之一的患者可能会遭遇需要住院甚至危及生命的副作用。相比之下,另一个“STRIDE”方案(tremelimumab联合durvalumab)的严重副作用较低(25.8%),但有效率也相对低一些(20.1%)[6]。
)为例,其有效率高达36%,但严重的(3级及以上)治疗相关不良事件发生率也达到了41%[5]。这意味着超过三分之一的患者可能会遭遇需要住院甚至危及生命的副作用。相比之下,另一个“STRIDE”方案(tremelimumab联合durvalumab)的严重副作用较低(25.8%),但有效率也相对低一些(20.1%)[6]。
这就给医生和患者出了一个难题:是选择更强效但风险更高的方案,还是选择相对安全但疗效稍逊的方案?有没有一种方法,能在不削弱疗效的前提下,有效预防或减轻这些严重的副作用呢?
02
皮质类固醇(通常简称为“激素”,如地塞米松 、泼尼松
、泼尼松 )是一种历史悠久的抗炎和免疫抑制药物。在传统化疗中,它常被用来预防过敏反应和呕吐
)是一种历史悠久的抗炎和免疫抑制药物。在传统化疗中,它常被用来预防过敏反应和呕吐 ,是肿瘤科的“老熟人”[7]。
,是肿瘤科的“老熟人”[7]。
然而,当免疫治疗时代来临时,激素的地位变得尴尬起来。因为免疫治疗的原理是“激活”患者自身的免疫系统去攻击肿瘤,而激素的作用是“抑制”免疫系统。因此,长期以来医学界有一个根深蒂固的教条:在免疫治疗中使用激素,会抑制抗肿瘤免疫力,导致治疗失败。这使得医生们对在免疫治疗期间使用激素,尤其是预防性使用,讳莫如深[8,9]。
03
这个看似合理的教条,正被越来越多的现实世界数据和科学研究挑战。
在肺癌 、头颈癌等多种癌症的治疗中,当免疫治疗联合化疗时,医生们为了预防化疗的副作用,会常规地给患者使用预防性激素[10-12]。大量的观察研究发现,这些短期使用的激素,不仅没有削弱免疫治疗的疗效,反而可能降低了严重的免疫相关副作用的发生率[13,14]。这形成了一个有趣的局面:在“免疫+化疗”中可以用激素,在“单独免疫”或“双免疫”中却不敢用。
、头颈癌等多种癌症的治疗中,当免疫治疗联合化疗时,医生们为了预防化疗的副作用,会常规地给患者使用预防性激素[10-12]。大量的观察研究发现,这些短期使用的激素,不仅没有削弱免疫治疗的疗效,反而可能降低了严重的免疫相关副作用的发生率[13,14]。这形成了一个有趣的局面:在“免疫+化疗”中可以用激素,在“单独免疫”或“双免疫”中却不敢用。
来自台湾大学的研究团队在肝癌小鼠模型中进行了严谨的实验。他们发现,在给小鼠使用“双免疫”治疗前,先注射预防性的地塞米松(一种激素),并没有影响免疫疗法的抗肿瘤效果[6,16]。肿瘤没有被“保护”起来,反而得到了同样的控制。更深入的分析显示,激素并没有抑制住那些能杀伤肿瘤的“高亲和力”T细胞,它只是选择性地抑制了一些可能引起副作用的“低亲和力”或自身反应性T细胞[18]。
为什么激素能抑制副作用,却不影响疗效?科学家们提出了一种“差异化敏感性”的理论[18-21]:
· 引起副作用的“坏T细胞”:
这类T细胞对肿瘤的杀伤力不强,但容易被我们自身的正常组织误认为是“敌人”而发起攻击,从而导致免疫相关副作用。它们对激素非常敏感,容易被抑制[18]。
· 杀伤肿瘤的“好T细胞”:
这类T细胞能够精准识别并强力杀伤肿瘤细胞,是免疫治疗起效的核心。它们对激素有更强的抵抗力,能够在短期激素暴露下“幸存”下来,继续执行任务[19,20]。
因此,短期、预防性地使用激素,就像是在免疫系统发动总攻前,先精确地“缴械”了那些可能制造混乱的“暴徒”,而保留了真正能打仗的“精锐部队”[21]。
04
专家们认为,并非所有患者都需要,但以下“高风险”人群可能是预防性激素策略的最大受益者[22]:
· 使用高风险方案的患者:特别是那些包含高剂量CTLA-4抑制剂(如伊匹木单抗3mg/kg)的治疗方案[2,3]。
· 身体脆弱的患者:例如年龄较大、体力状况较差(ECOG评分高)、肝功能储备不佳或合并多种严重疾病的患者。他们可能无法耐受一次严重的免疫相关副作用。
· 特殊情况患者:如患有需要控制的自身免疫性疾病(如类风湿关节炎 、银屑病
、银屑病 ),或之前因严重副作用中断过免疫治疗、现在考虑再次用药的患者[26]。
),或之前因严重副作用中断过免疫治疗、现在考虑再次用药的患者[26]。
05
文章提出了几种参考现有临床实践的策略,既简单易行,又具有科学依据(图1)[23-25]:
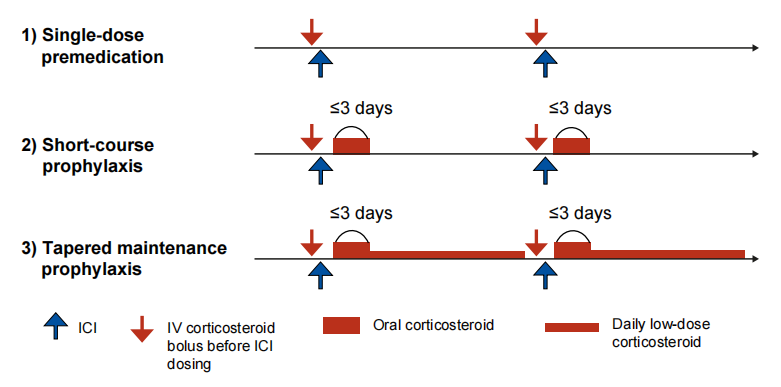
图1
1) 单次给药预处理:在每次输注免疫药物前,通过静脉注射一次中等剂量的激素(如地塞米松8-40mg)。这主要用于预防即刻的输液反应,也可能有助于抑制早期免疫风暴。
2) 短期疗程预防:在免疫治疗后,口服低剂量激素,持续不超过3天。这是从肺癌“免疫+化疗”方案中借鉴的经验,也是最有可能被采纳的策略之一[13,14]。
3) 低剂量维持预防:对于经过筛选的极高风险患者,在治疗后持续使用低剂量激素维持整个治疗周期。
这些策略成本低廉,操作简单,是每一位肿瘤科医生都熟悉的基本技能。
06
尽管证据令人鼓舞,但要将其正式写入临床指南,还需要更严谨的临床试验来证实[7,8]。
专家们呼吁开展一项随机、双盲、安慰剂对照的临床试验。研究将招募上述“高风险”患者,一组在接受“双免疫”治疗前接受短期激素预防,另一组接受安慰剂。主要观察目标是严重副作用的发生率和客观缓解率,同时还会加入深入的免疫学分析,以找到最适合从该策略中获益的人群[16]。
07
长期以来“激素会破坏免疫治疗”的教条正在被颠覆。最新的科学证据和临床观察表明,审慎、短期、预防性地使用皮质类固醇,可能是一种兼顾疗效与安全的巧妙策略[6,16-18]。它有望在不降低抗肿瘤效果的前提下,显著提升高风险肝癌患者对强效免疫治疗的耐受性。
当然,这并不意味着可以随意使用激素。关键在于“预防性”、“短期”和“高风险人群”。我们期待未来有更多高质量的研究,为这一策略提供坚实的证据,从而让更多肝癌患者能够安全、有效地从免疫治疗中获益。
(注: 本文基于2026年发表于权威期刊的专家观点文章撰写,旨在传递最新医学理念,不构成具体的医疗建议。所有治疗决策应由患者与其主治医生在充分沟通后共同制定。)
专家简介
韩国宏教授
• 主任医师、教授、博士生导师
• 国际门静脉高压最权威Baveno Ⅶ 专家组成员、科学委员会委员
• 亚太原发性肝癌理事会理事(APPLE Council Member)
• 中国抗癌协会第九届理事会理事
• 中国非公立医疗机构协会介入医学分会会长
• 中国抗癌协会-中西医整合肝癌专委会主委
• 中国抗癌协会-选择性内照射整合专业委员会主委
• 中国抗癌协会-整合肝癌专委会和肿瘤肝病学专委会副主委
• 中国研究型医院学会-介入专委会副主委
• 卫健委原发性肝癌诊疗指南专委会介入治疗组副组长(2011版、2017版、2019版、2022版和2024版)
• 2023-2025年入选全球2%顶尖科学家,2021年入选全球学者库
• 2020-2024年连续5年入选“ 中国高被引学者 ”
• 2020年中国消化病领域学术影响力排名TOP 100 中位列第六
• 2017年以第一完成人获军队科技进步一等奖
• 2016年作为主要成员获国家科学进步奖创新团队奖
• 2011年以来作为第一或通讯作者在Nat Rev Gastro Hepatol、Ann Oncol、Lancet Gastro Hepatol、Gastroenterology、J Hepatol、Gut、Radiology等权威杂志发表SCI同行评议论文167篇。他引12456余次,H指数53
作者简介
白苇
• 西安国际医学中心医院钇90治疗中心主任
• 中国研究型医院学会介入医学专业委员会青年委员会常务委员
• 中国医师协会介入医师分会肿瘤介入专委会委员
• 中华医学会放射学分会介入学组青年委员会委员
• 中国抗癌协会肿瘤介入学委员会化疗与免疫治疗专家委员会委员
• 中国抗癌协会诊疗一体化专业委员会委员
• 中国临床肿瘤学会(CSCO)胆道肿瘤专业委员会委员
• 陕西省抗癌协会第一届肿瘤消融治疗专委会常务委员
• 陕西省非公立医疗机构协会核医学专委会常务委员
• 主要负责肝恶性肿瘤的钇90内照射治疗、介入及靶免治疗;肝胆胰恶性肿瘤的介入联合系统治疗
• 在J Heptol、Liver Cancer、IJC等期刊发表SCI同行评议论文20余篇,其中第一/共同第一作者8篇,单篇影响因子最高30.08
来源:肝癌在线
执行:Aurora


