
前腺探泌|OS金标准不可撼动,从2026 EAU/NCCN指南证据看mHSPC治疗终点选择

替代终点需要验证,总生存期的延长才是评价抗肿瘤药物临床价值的金标准[1,2]
单从肿瘤临床治疗的角度来说,患者的总生存期(OS)延长才是评价抗肿瘤药物临床价值的金标准。然而,随着当前医疗水平的进展,肿瘤患者整体生存时间已经在不断延长,这可能导致在抗肿瘤药物临床研究中仅通过OS来评估疗效越来越难。因此,越来越多的临床研究已经采用了替代终点来进行疗效评估。不同的研究终点具有不同的功能和特点,需要结合所研究的疾病特征、药物作用机制和该临床试验的阶段合理地选择与运用[1]。而在mHSPC领域,应如何选择合适的临床终点?
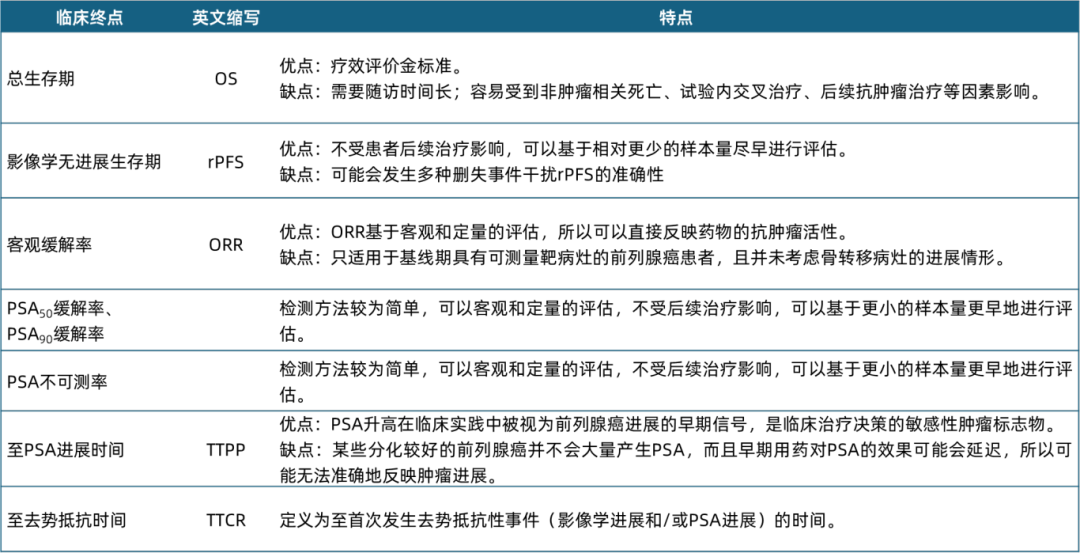
当前,在mHSPC的临床研究中,越来越多的采用OS和影像学无进展生存期(rPFS)作为研究终点支持注册。此外,客观缓解率(ORR)、前列腺特异性抗原 (PSA)动力学、至去势抵抗时间(TTCR)/进展至去势抵抗性前列腺癌(CRPC)时间和至首次后续治疗时间(TFST)等临床终点也可为疗效评估提供重要参考依据(表 1)[2,3]。
(PSA)动力学、至去势抵抗时间(TTCR)/进展至去势抵抗性前列腺癌(CRPC)时间和至首次后续治疗时间(TFST)等临床终点也可为疗效评估提供重要参考依据(表 1)[2,3]。
表 1常用mHSPC疗效评估临床终点选择(部分)[2]


OS显著获益支持EAU与NCCN指南强推荐/优先推荐恩扎卢胺 二联方案
二联方案
2026年3月,EAU前列腺癌指南更新,对mHSPC一线治疗推荐进行了修订。当前雄激素受体通路抑制剂(ARPI)二联方案在EAU指南中有两种推荐等级,一是强推荐雄激素剥夺治疗(ADT) + 恩扎卢胺/阿比特龙 /阿帕他胺
/阿帕他胺 /瑞维鲁胺
/瑞维鲁胺 的二联方案,二是弱推荐ADT + 达罗他胺
的二联方案,二是弱推荐ADT + 达罗他胺 的二联方案(表 2)[4]。
的二联方案(表 2)[4]。
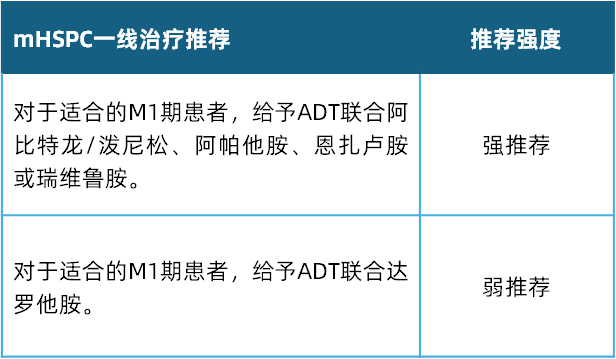
表 2 2026 EAU前列腺癌指南mHSPC一线治疗推荐(部分)
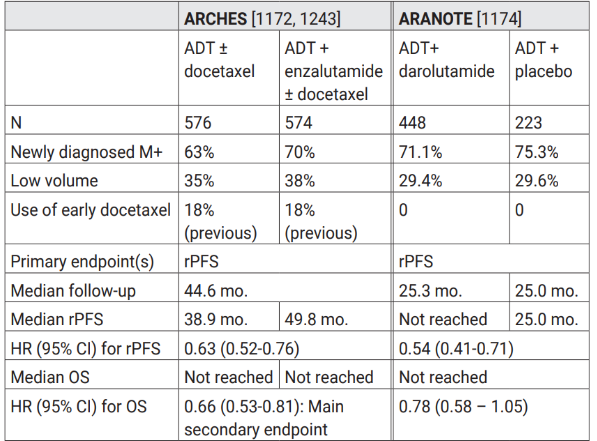
以恩扎卢胺二联方案和达罗他胺二联方案为例,EAU指南对二者的推荐基于ENZAMET、ARCHES和ARANOTE研究结果。EAU指南将ARCHES和ARANOTE研究主要结果汇总在一个表格中(表 3),两个研究均以rPFS为主要终点,且OS数据均未成熟*#[4]。
表 3 2026 EAU前列腺癌指南引用的ARCHES和ARANOTE研究结果*#[4]
* EAU指南引用的并非两个研究的更长随访的更新数据,从解读指南的角度出发,本文与之保持一致。
# 非头对头研究,数据无法直接对比,请谨慎解读。
在临床药物审评时,在理想条件下,如果rPFS和OS均达到了预设的主要研究终点,那么以该数据支持产品注册是最为稳妥的。但在现实中,如果选择OS作为唯一主要终点计算样本量,那么可能会需要比较大的样本量,最终将导致临床研究实施难度加大。因此,研究者一直需要除OS之外的其他替换性研究终点来加速药物开发。尤其是在前列腺癌的药物研究中,这种需求显得更加迫切。目前,在考虑临床研究数据支持药品注册时,已经可以选择rPFS作为主要终点[3]。但应当注意的是,在选择rPFS来评价药物疗效时仍需关注能否真正延长OS[2]。
在ARCHES研究中,约36%的患者为低瘤负荷,约25%曾接受过局部治疗,18%的患者曾接受过多西他赛 治疗。与对照组相比,接受恩扎卢胺 + ADT治疗的患者中位rPFS显著延长(HR = 0.39,95% CI 0.3 ~ 0.5)。在预设的最终分析中,关键次要终点OS也得到显著延长(HR = 0.66;95% CI 0.53 ~ 0.81),并且可以继续维持rPFS的显著获益(HR = 0.63,95% CI 0.52 ~ 0.76)*[4]。
治疗。与对照组相比,接受恩扎卢胺 + ADT治疗的患者中位rPFS显著延长(HR = 0.39,95% CI 0.3 ~ 0.5)。在预设的最终分析中,关键次要终点OS也得到显著延长(HR = 0.66;95% CI 0.53 ~ 0.81),并且可以继续维持rPFS的显著获益(HR = 0.63,95% CI 0.52 ~ 0.76)*[4]。
在ARANOTE研究中,与对照组相比,接受达罗他胺 + ADT治疗的患者可显著延长中位rPFS(HR = 0.54,95% CI 0.41 ~ 0.71),且在高瘤负荷与低瘤负荷等各亚组中获益一致。最终分析显示OS无统计学差异(HR = 0.81,95% CI 0.59 ~ 1.12)*[4]。
2026v5版NCCN前列腺癌指南在讨论部分中指出:“专家委员会将达罗他胺 + ADT列为低瘤负荷与高瘤负荷mHSPC的治疗选择。由于该双联疗法尚未证实OS获益,目前不作为1类推荐方案”[5]。在具体的推荐中,无论mHSPC患者肿瘤负荷高低,均将恩扎卢胺/阿比特龙/阿帕他胺二联方案列为优先推荐(1类),将达罗他胺二联方案列为其他推荐(2B)类(图 1)[5]。


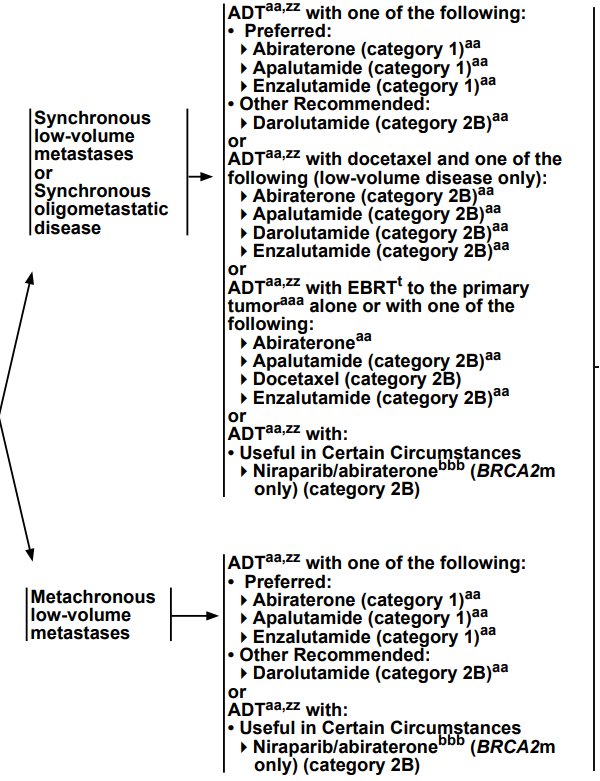

图 1 2026v5版NCCN前列腺癌指南mHSPC治疗推荐(部分)



稳健的OS数据是恩扎卢胺二联方案长期生存获益的有力佐证
在恩扎卢胺二联方案注册时,全球ARCHES研究并未获得成熟的OS数据,支持注册的主要是依据积极的rPFS结果。当时,其在中国获批也综合考虑了多方面因素。
首先,恩扎卢胺是全球首个研发上市的ARPI,其疗效已在AFFIRM、PREVAIL和PROSPER多项III期临床试验中得到充分验证,已证实恩扎卢胺可显著延长转移性去势抵抗性前列腺癌(mCRPC)及非转移性去势抵抗性前列腺癌(nmCRPC)患者的OS,有效性明确[3]。
其次,mHSPC与mCRPC和nmCRPC同样依赖雄激素信号通路,结合当时ARCHES研究已公布的数据,两组患者的rPFS HR为0.39,该数据与同类药物具有可比性。基于此,审评中认为恩扎卢胺应用于mHSPC患者时,有较大概率可使患者在OS方面获得获益,因此,现有优异的rPFS数据可作为其获批mHSPC适应证的重要支撑依据[3]。
2021年,ARCHES研究公布了最终OS分析数据,证实了恩扎卢胺二联方案的长期生存获益,两组间HR为0.66(95% CI 0.53 ~ 0.81,P < 0.0001)[6]。2025年,ARCHES研究更新了中位61.4个月(约5年)随访结果,体现了恩扎卢胺二联方案稳健的长期OS获益,5年生存率为66%(vs. 安慰剂 + ADT 53%),两组间HR为0.70(95% CI: 0.58 ~ 0.85,P < 0.001),使患者死亡风险降低了30%,进一步确认了恩扎卢胺的疗效[7]。
总体而言,mHSPC患者生存期相对较长,有PSA标志物等疾病特征,在临床研究中可选择的疗效性终点多样。在此背景下,合理选择替代性终点可提高研发效率,但仍需关注临床获益的稳健程度以及转化为OS获益的趋势。根据治疗方案在临床研究中表现出的rPFS差异的OS趋势,并结合其他前期终点数据,全面、科学地评估药物疗效,共同支持临床决策。
* EAU指南引用的并非两个研究的更长随访的更新数据,从解读指南的角度出发,本文与之保持一致。

参考文献
[1] 宋媛媛, 唐凌 , 夏琳, 等. 在抗肿瘤药物临床试验中运用替代终点的审评考量[J/OL]. 中华肿瘤杂志, 2022, 44(11): 1155-1159. DOI:10.3760/cma.j.cn112152-20210913-00697.
, 夏琳, 等. 在抗肿瘤药物临床试验中运用替代终点的审评考量[J/OL]. 中华肿瘤杂志, 2022, 44(11): 1155-1159. DOI:10.3760/cma.j.cn112152-20210913-00697.
[2] 国家药品监督管理局药品审评中心. 《晚期前列腺癌临床试验终点技术指导原则》[EB/OL]. [2026-03-19]. https://www.cde.org.cn/main/att/download/f896f2327b9291c82d16d00b2585bfb1.
[3] 仝昕, 吕俊, 郝瑞敏 , 等. 转移性激素敏感性前列腺癌临床研究终点的审评考虑[J/OL]. 中国临床药理学杂志, 2023, 39(6)[2026-03-19]. https://doi.org/10.13699/j.cnki.1001-6821.2023.06.030. DOI:10.13699/j.cnki.1001-6821.2023.06.030.
, 等. 转移性激素敏感性前列腺癌临床研究终点的审评考虑[J/OL]. 中国临床药理学杂志, 2023, 39(6)[2026-03-19]. https://doi.org/10.13699/j.cnki.1001-6821.2023.06.030. DOI:10.13699/j.cnki.1001-6821.2023.06.030.
[4] CORNFORD P, TILKI D, VAN DEN BERGH R C N, et al. EAU-EANM-ESTRO-ESUR-SIOG Guidelines on Prostate Cancer[EB/OL]. 2026[2026-03-14]. https://d56bochluxqnz.cloudfront.net/documents/full-guideline/EAU-EANM-ESTRO-ESUR-ISUP-SIOG-Guidelines-on-Prostate-Cancer-2026_2026-03-14-104356_ixav.pdf
[5] National Comprehensive Cancer Network. Prostate Cancer (Version 5.2026)[EB/OL]. 2026[2026-01-23]. https://www.nccn.org/professionals/physician_gls/pdf/prostate.pdf.
[6] ARMSTRONG A J, IGUCHI T, AZAD A A, et al. LBA25 Final overall survival (OS) analysis from ARCHES: A phase III, randomized, double-blind, placebo (PBO)-controlled study of enzalutamide (ENZA) + androgen deprivation therapy (ADT) in men with metastatic hormone-sensitive prostate cancer (mHSPC)[J/OL]. Abstract Book of the ESMO Congress 2021, 16 – 21 September 2021, 2021, 32: S1300-S1301. DOI:10.1016/j.annonc.2021.08.2101.
[7] ARMSTRONG A J, PETRYLAK D P, SHORE N D, et al. ARCHES: 5-year follow-up overall survival (OS) analysis of enzalutamide (ENZA) plus androgen-deprivation therapy (ADT) in patients (pts) with metastatic hormone-sensitive prostate cancer (mHSPC).[J/OL]. Journal of Clinical Oncology, 2025, 43(16_suppl): 5005-5005. DOI:10.1200/JCO.2025.43.16_suppl.5005.
MAT-CN-XTD-2026-00056
Preparation date: 2026-03-16
仅供医疗卫生专业人士阅读
