
邵春红教授 | 精准调控!从国内外指南更新看失眠诊疗新发展

随着对失眠病理机制的深入研究,国内外失眠诊疗指南/共识持续迭代更新,共同推动失眠管理向更科学、更精准的方向迈进。在这一进程中,新一代抗失眠药物——双食欲素受体拮抗剂(DORAs)的崛起,标志着失眠治疗从传统“广泛镇静”迈入“精准调节”的全新阶段。本文围绕国内外权威指南的核心变迁要点,剖析失眠诊疗领域新发展,以期为失眠临床实践提供参考。


当前,国内外权威指南的迭代可归纳为三个维度的核心升级:
➤ 1.诊断标准更新:重视日间功能损害,并明确失眠是一种独立疾病,需单独治疗方案
失眠诊断方面,国内外指南的核心更新要点包括:
1)将日间功能损害纳入失眠障碍诊断的必要条件之一:《国际疾病分类第11版(ICD-11)》及《2023版欧洲失眠指南》等明确强调,失眠诊断必须同时满足"夜间睡眠困难"与"至少一项日间症状(如疲劳、认知障碍、情绪紊乱等)"1-3。《中国失眠障碍诊断和治疗指南(2025)》同样将"影响日常生活"作为失眠诊断的必需维度4。
2)放弃原发性/继发性二分法,确立失眠独立疾病地位:各指南均认识到失眠不仅是其他疾病的伴随症状,更是需要单独干预的独立疾病实体1-5。如《2024加拿大失眠管理共识》指出,失眠应作为独立的疾病进行诊断,即使伴随合并症,失眠也需要单独的治疗方案6。
表1 国内外失眠指南的诊断标准1-4
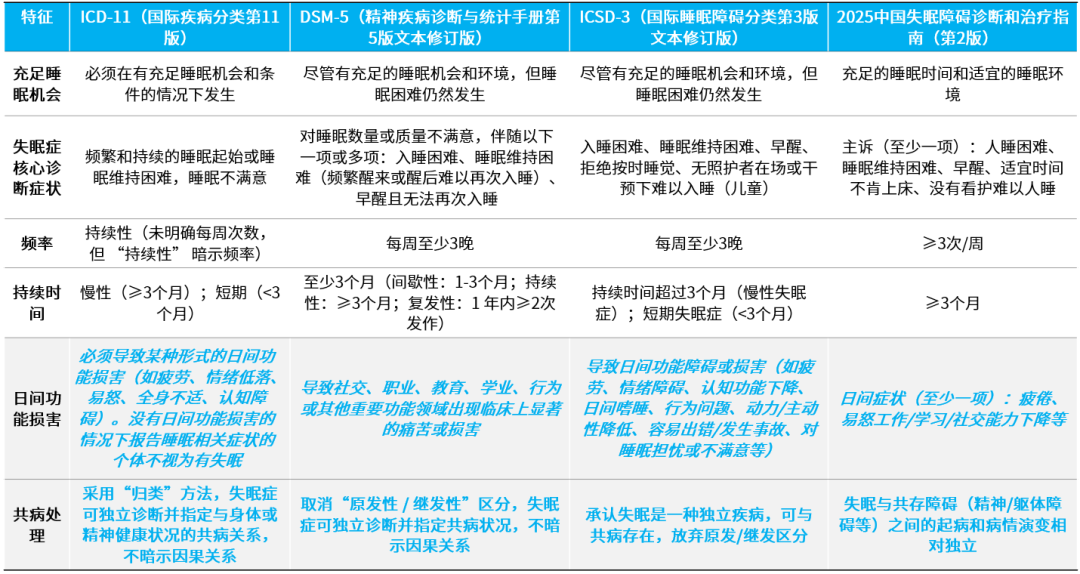
表2 国内外失眠指南中的失眠治疗目标4,5,7,8

自1998年食欲素被发现,到2014年首个DORA获批上市,失眠治疗实现革命性突破,其治疗理念逐渐从传统“强制镇静(GABA机制)”转向DORAs的“精准调节(抑制促觉醒信号)”。其中,以达利雷生为代表的DORAs已成为国内外各指南推荐的新一线失眠治疗药物1,4,6,8-10。但需明确的是,《2023欧洲失眠指南》等权威指南仍表示认知行为治疗(CBT-I)是所有成年失眠患者的首选一线治疗(A级证据,Ⅰ级推荐)1,4,6,8-10。
表3 国内外失眠指南中的DORAs类药物治疗推荐意见1,4,6,8-10
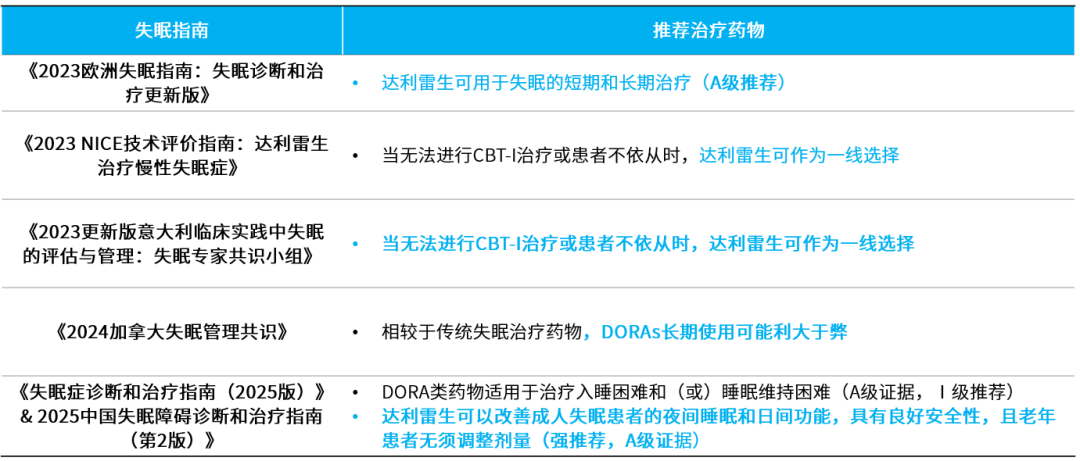
值得注意的是,达利雷生是目前最新欧洲指南推荐的唯一能改善日间功能的DORA1。


DORAs类药物之所以能逐渐成为国内外指南力荐的新一线失眠治疗药物,主要源于:
1)传统镇静催眠药存在诸多负面效应。研究显示,传统镇静催眠药物——苯二氮䓬受体激动剂(BZRAs)长期使用不仅会干扰睡眠结构,还会导致跌倒、痴呆、滥用等风险增加,并带来次日残留效应/日间嗜睡症状11-14,尚不能满足失眠患者的临床治疗需求。
2)DORAs类药物具有不同传统镇静催眠药的创新机制和疗效优势。DORAs类药物通过拮抗食欲素1受体(OX1R)和食欲素2受体(OX2R),以生理方式促进睡眠,有效改善睡眠的启动和维持,且具有维持正常睡眠结构、次日残留效应低、依赖性风险小的显著优势15,弥补了传统镇静催眠药的治疗空白,也全面契合了失眠诊疗的最新需求,以达利雷生为例:
➤ 机制创新:达利雷生对OX1R和OX2R具有同等较强亲和力,可通过阻断食欲素系统,抑制过度觉醒状态,在促进睡眠、改善睡眠维持的同时,不改变各睡眠阶段的时间占比,实现精准调控16,17。此外,达利雷生的8小时终末半衰期,更符合人体正常睡眠周期,可有效避免次日残留18。
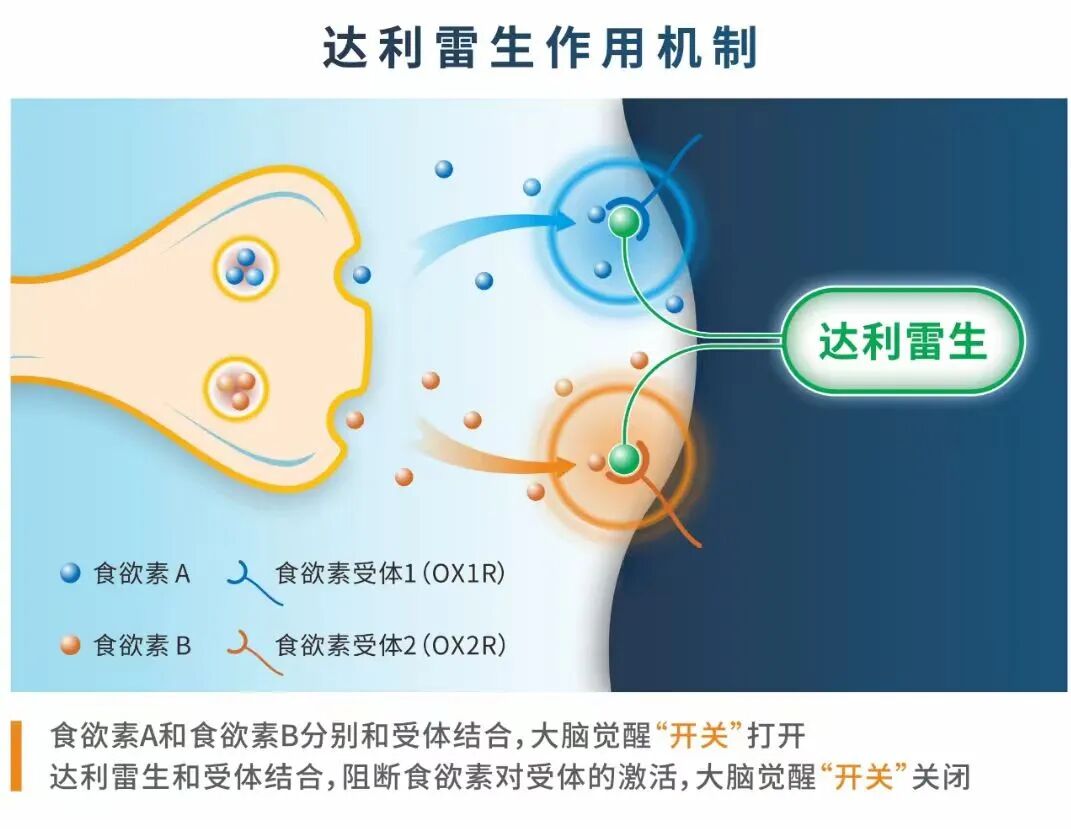
➤ 昼夜兼顾:达利雷生的国际多中心、随机、双盲、安慰剂对照Ⅲ期研究显示,与安慰剂相比,达利雷生50mg治疗3个月时,患者入睡后觉醒时间(WASO)较基线显著降低、持续睡眠潜伏期(LPS)较基线显著缩短、自我报告的总睡眠时间(TST)较基线显著增加;此外,失眠日间症状及影响问卷量表(IDSIQ)总分及各领域评分显著改善,其中,思睡域和情绪域的改善具有临床意义,且该治疗获益从第1周即显现19。随后的国际Ⅲ期扩展研究显示,达利雷生治疗1年可持续改善夜间睡眠和日间功能20。
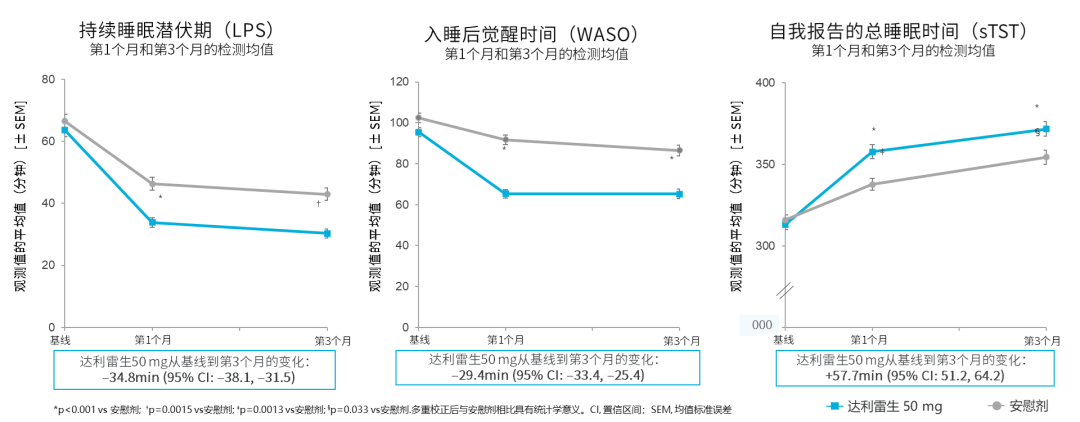
图2 达利雷生50mg显著缩短入睡时间并改善睡眠维持
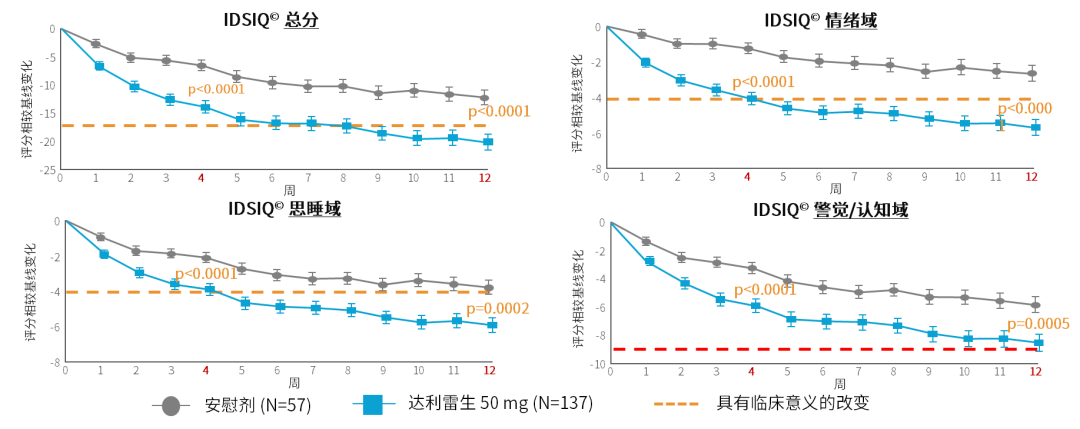
➤ 安全性良好:国际Ⅲ期研究显示,达利雷生50mg治疗3个月整体安全性良好,不良事件发生率与安慰剂相当(38% vs. 34%),因不良事件导致停药比例低于安慰剂,且嗜睡(2% vs. 2%)发生率与安慰剂相同,跌倒(<1% vs. 3%)发生率甚至低于安慰剂19。其国际Ⅲ期扩展也研究显示,达利雷生长期耐受性良好,治疗期间未出现新的安全事件信号;长期给药后,直接停药未产生戒断相关体征或症状,也未观察到任何反跳弹性失眠20。
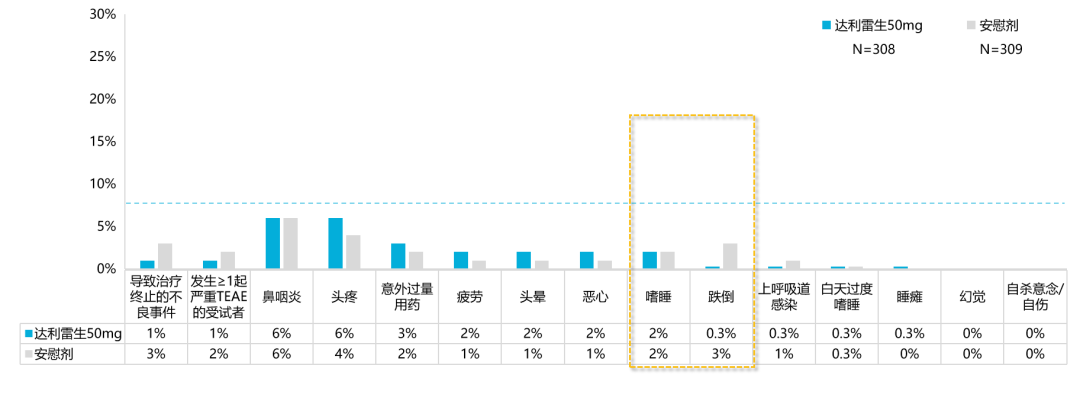
图4 达利雷生50mg治疗3个月的跌倒发生率较安慰剂低
➤ 适用于复杂患者:2025年意大利《达利雷生临床实践应用共识》指出,达利雷生在特殊患者群体,如老年人及合并症(包括神经退行性疾病与认知障碍、失眠合并睡眠呼吸暂停、精神疾病与情绪障碍、癫痫综合征及不宁腿综合征)患者中兼具疗效和安全性,是治疗失眠的一种新的、且极具潜力的选择21。
专家点评
从明确失眠独立疾病地位、并将日间功能损害纳入核心诊断标准,到构建“夜间睡眠+日间功能”双改善的综合治疗目标,再到治疗理念从传统“广泛镇静”转向DORAs的“精准调节”,失眠管理正步入“精准与系统化”的全新时代。其中,以达利雷生为代表的DORAs类药物,凭借其创新机制、兼顾“昼夜改善”的双重获益、以及良好安全性,逐渐成为国内外指南一致推荐的一线治疗药物,为失眠患者带来了更契合临床需求的治疗方案。
值得关注的是,食欲素系统的调控作用并非局限于睡眠-觉醒周期,越来越多证据表明,其在认知与情感等高级脑功能调控中也同样扮演着核心角色22。如在情绪与记忆方面,食欲素通过作用于杏仁核(AMY)(情绪加工核心区)中的OX1R,促进恐惧记忆形成和应激反应增强;同时,也广泛投射至前额叶皮层(PFC),参与调节焦虑与抑郁相关行为22,23。目前,已有研究显示DORAs类药物在改善重度抑郁症患者睡眠参数方面具有潜力24,期待未来,随着机制与临床研究的进一步深入,DORAs类药物能进一步突破单一失眠治疗的范畴,为失眠与精神等疾病的共病管理开辟新路径!
邵春红 教授
复旦大学附属华山医院
复旦大学附属华山医院精神医学科 副主任(主持工作)
美国Purdue大学认知心理学博士后
完成哈佛医学院临床研究学者培训项目
中华医学会精神医学分会委员
中国中西医结合学会心身专委会 常委、副主任委员
上海市中西医结合学会心身专委会 主任委员
上海市医学会精神医学专委会 委员
上海市医学会心身医学专委会 委员
上海市医师协会精神科医师分会 委员
中国CBT专业组织CBT培训师
参考文献



