
HER2低表达状态与接受CDK4/6抑制剂治疗的转移性乳腺癌患者生存的关联:系统评价与Meta分析

前言
细胞周期蛋白依赖性激酶(CDK)4/6抑制剂显著改变了激素受体阳性/人表皮生长因子受体2阴性(HR+/HER2-)转移性乳腺癌 (MBC)的治疗格局,其联合内分泌治疗已成为一线和二线治疗的标准方案,可改善患者的无进展生存期(PFS)和总生存期(OS)。然而,并非所有患者都能从该治疗中获得一致获益,约15%的患者即使接受一线治疗仍出现病情进展,因此亟需明确可预测长期获益和早期进展的生物标志物。多项研究提示HER2低表达疾病患者可能存在疗效降低的情况,本研究通过系统评价和Meta分析,评估MBC患者HER2低表达与CDK4/6抑制剂治疗疗效结局的关联。
(MBC)的治疗格局,其联合内分泌治疗已成为一线和二线治疗的标准方案,可改善患者的无进展生存期(PFS)和总生存期(OS)。然而,并非所有患者都能从该治疗中获得一致获益,约15%的患者即使接受一线治疗仍出现病情进展,因此亟需明确可预测长期获益和早期进展的生物标志物。多项研究提示HER2低表达疾病患者可能存在疗效降低的情况,本研究通过系统评价和Meta分析,评估MBC患者HER2低表达与CDK4/6抑制剂治疗疗效结局的关联。
研究背景
ErbB2受体家族在内分泌治疗耐药中起关键作用,针对该通路的靶向治疗已在HER2阳性乳腺癌领域应用逾二十年。HER2阳性肿瘤定义为IHC 3+或IHC 2+/ISH+,而IHC 1+或IHC 2+/ISH-的肿瘤HER2表达水平较低,且此类肿瘤可能通过新型抗HER2抗体偶联药物实现靶向治疗,因此“HER2低表达乳腺癌”这一新亚型应运而生。
然而,HER2低表达对患者生存的影响尚未明确,且可能影响包括CDK4/6抑制剂在内的抗内分泌药物疗效,但现有研究在设计、人群、样本量及结局指标等方面存在差异,因此需通过系统评价和Meta分析明确其预后作用。
研究方法
本研究检索PubMed、Web of Science和Scopus数据库,收集从建库至2023年8月8日发表的相关研究,纳入接受CDK4/6抑制剂治疗的MBC患者,且按HER2表达状态报告生存结局的研究。提取内容包括第一作者姓名、发表年份、患者总数、OS或PFS的风险比(HR)及其95%置信区间(CI),以及客观缓解率(ORR),采用纽卡斯尔-渥太华量表评估研究质量和偏倚风险。
Meta分析采用固定效应模型的通用逆方差法,以HR及95%双侧CI作为主要汇总指标,通过I²统计量报告异质性,使用Review Manager 5.4软件进行分析,P<0.05为差异有统计学意义。研究的主要终点是评估HR+乳腺癌患者中HER2低表达与CDK4/6抑制剂治疗后PFS的关联,次要终点是根据HER2表达(HER2低表达与HER2 0表达)评估OS和ORR的关联,并按治疗线进行PFS亚组分析。
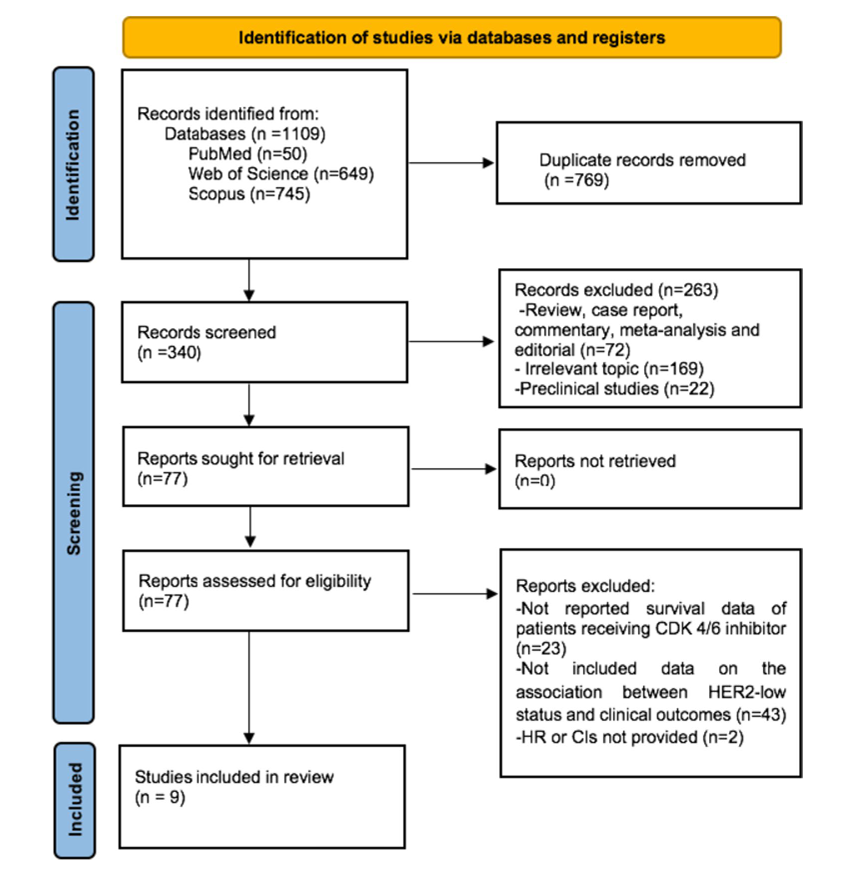
图1.研究方法1
研究结果
(一)研究特征
纳入9项研究共2705例患者,其中4项为一线治疗队列,5项为包含不同治疗线的混合队列。其中5项为多中心研究,4项报告了单中心数据。8项为回顾性研究,仅1项包含前瞻性记录数据的队列。所有研究均纳入了芳香酶抑制剂或氟维司群 联合CDK4/6抑制剂治疗的患者。样本量在84至1084例之间,9项研究中有5项样本量不足200例。5项研究报告了PFS和OS结果,4项仅报告PFS结果。各研究中位随访时间为15-36个月。根据NOS标准评估,多数研究存在较低偏倚风险。
联合CDK4/6抑制剂治疗的患者。样本量在84至1084例之间,9项研究中有5项样本量不足200例。5项研究报告了PFS和OS结果,4项仅报告PFS结果。各研究中位随访时间为15-36个月。根据NOS标准评估,多数研究存在较低偏倚风险。
(二)HER2低表达状态与PFS的关联
9项研究中6项未发现HER2低表达状态与PFS相关。汇总分析显示,HER2低表达组疾病进展和/或死亡风险高于HER2 0表达组(HR:1.22,95%CI 1.10-1.35,P<0.001;图2),纳入研究的异质性程度较低(I²=0%)。通过剔除单项研究进行的敏感性分析显示结果一致。
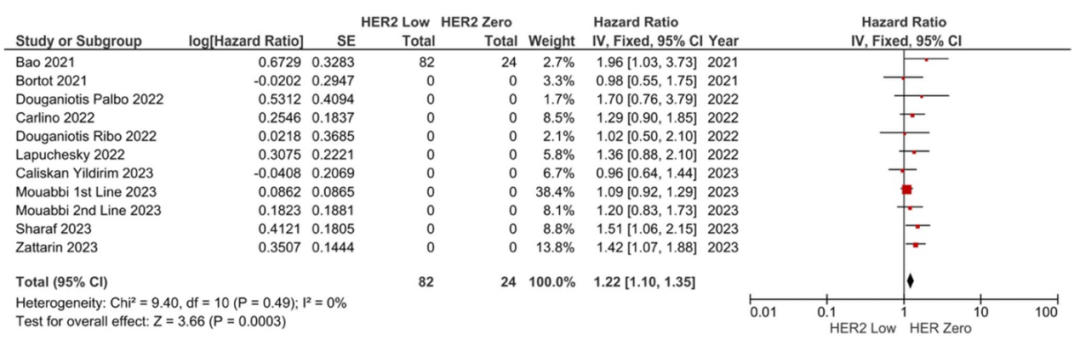
图2.PFS的Meta分析 菱形表示合并效应量1
亚组分析显示,一线(HR:1.18,95%CI 1.04-1.34,P=0.010)和二线(HR:1.20,95%CI 0.83-1.73,P=0.330)治疗的风险相似,亚组间差异无统计学意义(P=0.930)。需说明的是,其中四项研究未提供各治疗线独立数据,仅一项研究明确纳入二线治疗患者。
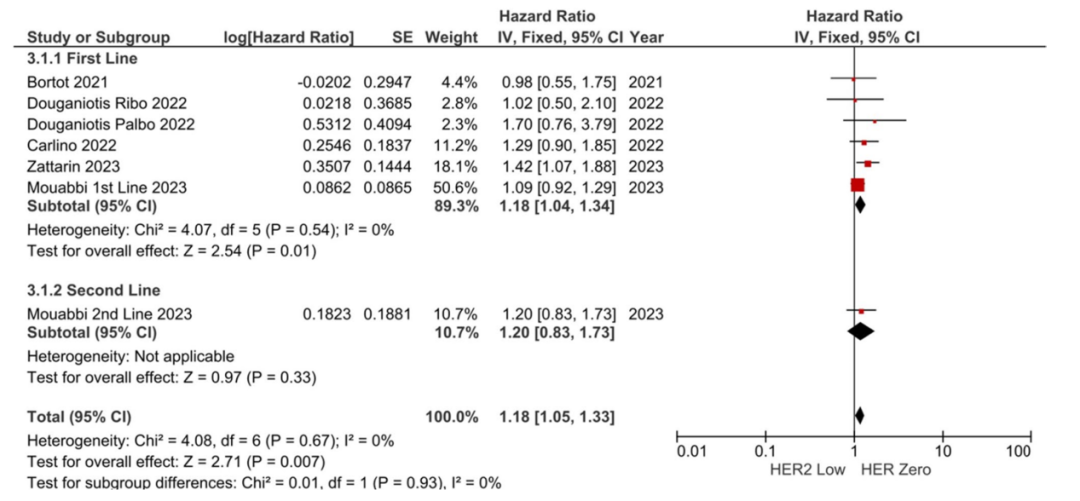
图3.按治疗线进行的PFS亚组分析1
(三)HER2低表达状态与OS/ORR的关联
共有5项和3项研究分别报告了OS和ORR。在5项研究的汇总分析中,HER2低表达组死亡风险高于HER2 0表达组(HR:1.22,95%CI 1.04-1.44,P=0.010;图4)。纳入研究异质性低(I²=0%),通过剔除单项研究进行的敏感性分析显示结果一致。
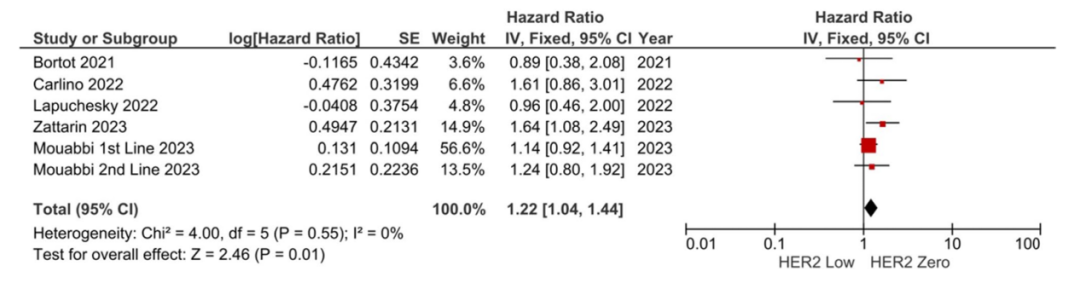
图4.OS的Meta分析 菱形表示合并效应量1
CDK4/6抑制剂治疗的总合并ORR为:HER2低表达组47.8%,HER2 0表达组58.3%。无论HER2低表达状态如何,ORR均无显著差异(HR:0.80,95%CI 0.44-1.44,p=0.460;图5)。ORR的Meta分析存在高度异质性(I²=50%)。
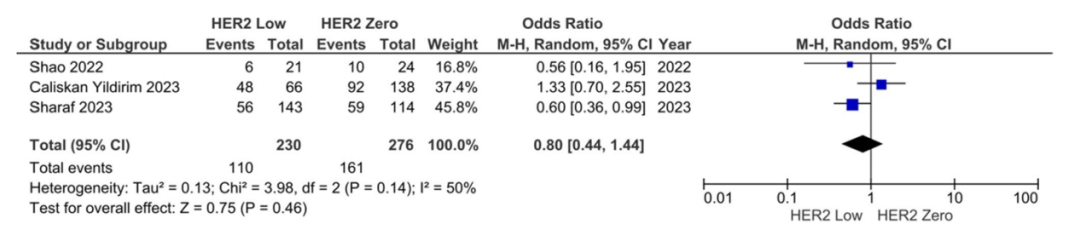
图5.ORR的Meta分析1
研究结论
现有证据表明,HER2低表达MBC患者接受CDK4/6抑制剂治疗时,疾病进展或死亡风险显著更高。尽管CDK4/6抑制剂联合内分泌治疗是独立于HER2低表达状态的标准治疗方案,但仍需进一步研究以改善HR+/HER2低表达MBC患者的治疗结局。
讨论与总结
本研究通过系统评价与Meta分析,明确了HER2低表达状态与接受CDK4/6抑制剂治疗的HR+转移性乳腺癌患者生存结局的关联。从生物学机制来看,HER2低表达肿瘤可能通过高表达ESR1、AKT等与CDK4/6抑制剂耐药相关的分子,影响治疗效果,且HER2低表达状态可能作为ErbB2通路激活的替代指标,为临床疗效预测提供参考。
但研究存在一定局限性,多数纳入研究为回顾性设计,样本量有限,研究队列在治疗线和内分泌治疗方案方面存在异质性,限制了开展具有充分统计效能的亚组分析。多数研究随访时间较短,可能影响总生存期结果的可靠性。此外,多数研究未对额外临床参数进行调整。最后,由于多数研究具有回顾性特征,无法确证HER2低表达状态对生存结局的影响具有因果关系,故研究者在报告中采用“关联性”而非“效应”表述。
综上,HER2低表达状态可作为接受CDK4/6抑制剂治疗的HR+转移性乳腺癌患者的不良预后标志物。未来需开展大样本、长期随访的前瞻性研究,明确HER2低表达的标准化定义及检测标准,进一步验证其预后价值,并探索新型联合治疗方案,以改善HR+/HER2低表达肿瘤患者的治疗结局。
参考文献:
1.Guven DC, Sahin TK. The association between HER2-low status and survival in patients with metastatic breast cancer treated with Cyclin-dependent kinases 4 and 6 inhibitors: a systematic review and meta-analysis. Breast Cancer Res Treat. 2024;204(3):443-452. doi:10.1007/s10549-023-07226-1IF: 3.0 Q2
审批编号:CN-178618
有效期至:2027/2/5
本文由阿斯利康提供,仅供医疗卫生专业人士参考,不可用于推广目的。
编辑:KIKI
审校:River
排版:Ben
执行:Ocean
本平台旨在为医疗卫生专业人士传递更多医学信息。本平台发布的内容,不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议。如该等信息被用于了解医学信息以外的目的,本平台不承担相关责任。本平台对发布的内容,并不代表同意其描述和观点。若涉及版权问题,烦请权利人与我们联系,我们将尽快处理。

