
两项突破性研究结果重磅发布!依洛尤单抗降脂获益人群拓宽,替尔泊肽心肾保护优势明确,引领心血管代谢精准防治新方向丨ACC.26 重磅
当地时间3月28日,第75届美国心脏病 学会科学年会(ACC.26)在美国新奥尔良重磅启幕。会议期间,27项最新突破性临床试验(LBCT)、19项特色临床研究(FCR)结果重磅发布,涵盖肺栓塞
学会科学年会(ACC.26)在美国新奥尔良重磅启幕。会议期间,27项最新突破性临床试验(LBCT)、19项特色临床研究(FCR)结果重磅发布,涵盖肺栓塞 、心血管代谢疾病、心肌梗死
、心血管代谢疾病、心肌梗死 、高血压
、高血压 、心力衰竭
、心力衰竭 、结构性心脏病等多个领域,为心血管疾病
、结构性心脏病等多个领域,为心血管疾病 防治带来里程碑式新证据。本文汇总了会议首日发布的两项心血管代谢领域药物相关的重磅研究结果,以飨读者。
防治带来里程碑式新证据。本文汇总了会议首日发布的两项心血管代谢领域药物相关的重磅研究结果,以飨读者。

✎VESALIUS-CV亚组研究证实,无显著动脉粥样硬化 的糖尿病患者,早期应用依洛尤单抗
的糖尿病患者,早期应用依洛尤单抗 可显著降低首发心血管事件及死亡风险。
可显著降低首发心血管事件及死亡风险。
来自美国哈佛医学院附属布莱根妇女医院的Nicholas Marston教授在LBCT-II专场公布了VESALIUS-CV试验二次分析的结果,证实在无显著动脉粥样硬化的糖尿病患者中,依洛尤单抗可显著降低首发主要不良心血管事件(MACE)风险。研究结果同步发表于JAMA杂志。
目前PCSK9抑制剂主要用于已有明确动脉粥样硬化患者的强化降脂治疗,而无明确动脉粥样硬化的糖尿病高危人群能否从中获益,尚不明确。本研究旨在探讨依洛尤单抗能否降低此类患者的首发MACE风险。
VESALIUS-CV试验为一项全球多中心、随机、双盲、安慰剂对照试验,共纳入33个国家774家中心的12257例无心肌梗死或卒中病史,低密度脂蛋白胆固醇(LDL-C)≥90 mg/dL,且合并已确诊动脉粥样硬化或糖尿病的患者。
本次亚组分析聚焦无已知显著动脉粥样硬化的糖尿病患者(如存在≥50%的动脉狭窄或冠状动脉钙化[CAC]评分≥100分)。在优化他汀±依折麦布 基础上,随机给予依洛尤单抗(140 mg,每2周皮下注射一次)或安慰剂进行治疗,中位随访4.8年。
基础上,随机给予依洛尤单抗(140 mg,每2周皮下注射一次)或安慰剂进行治疗,中位随访4.8年。
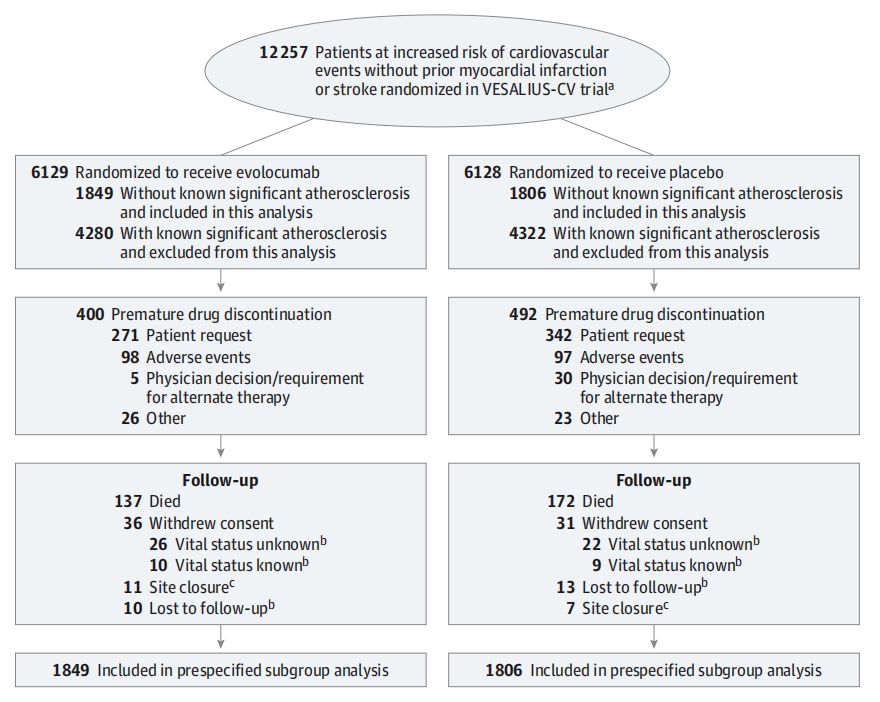
图1 研究设计
研究的主要终点为3P-MACE(包括冠心病 死亡、心肌梗死或缺血性卒中)和4P-MACE(包括3P-MACE和缺血驱动的动脉血运重建)发生率。次要终点包括全因死亡率等。
死亡、心肌梗死或缺血性卒中)和4P-MACE(包括3P-MACE和缺血驱动的动脉血运重建)发生率。次要终点包括全因死亡率等。
本队列共纳入3655例患者,中位年龄65岁,女性占57%。在治疗48周时,依洛尤单抗组的中位LDL-C为52 mg/dL,安慰剂组为111 mg/dL(P<0.001)。
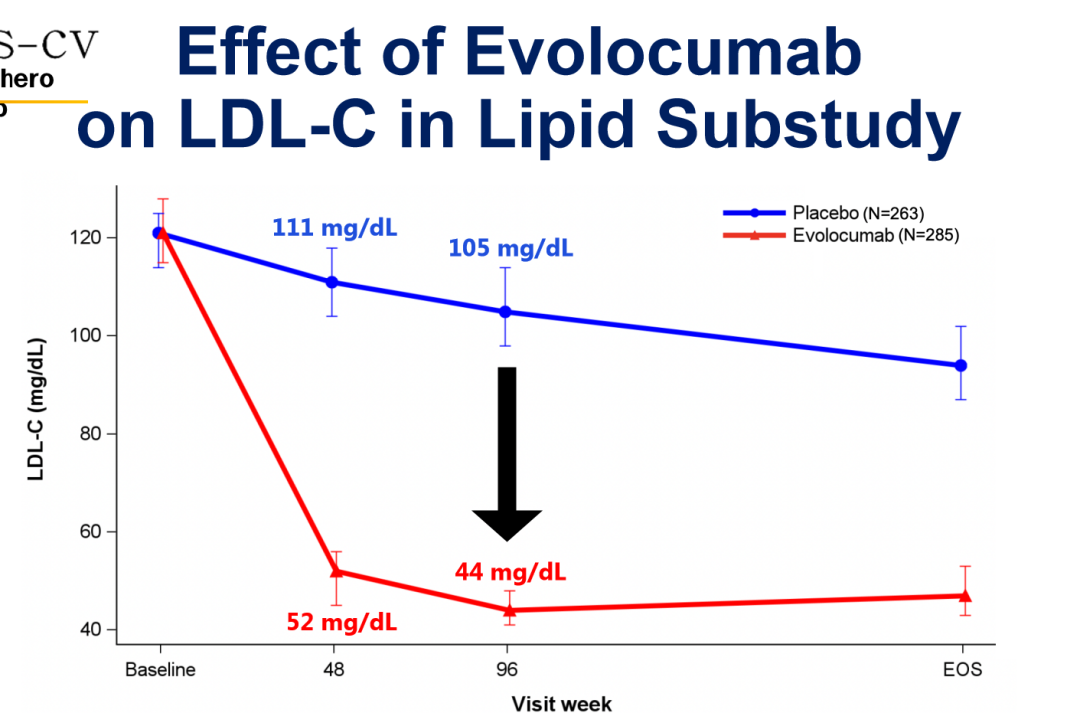
图2 LDL-C降低情况
与安慰剂组相比,依洛尤单抗可显著降低3-P MACE风险31%(5.0% vs. 7.1%;HR=0.69,95% CI:0.52~0.91,P=0.009);显著降低4-P MACE风险同样为31%(7.6% vs 10.5%;HR=0.69,95% CI:0.55~0.86,P=0.001)。获益在治疗1年后开始显现,之后3-P MACE风险降低41%,4-P MACE风险降低39%。
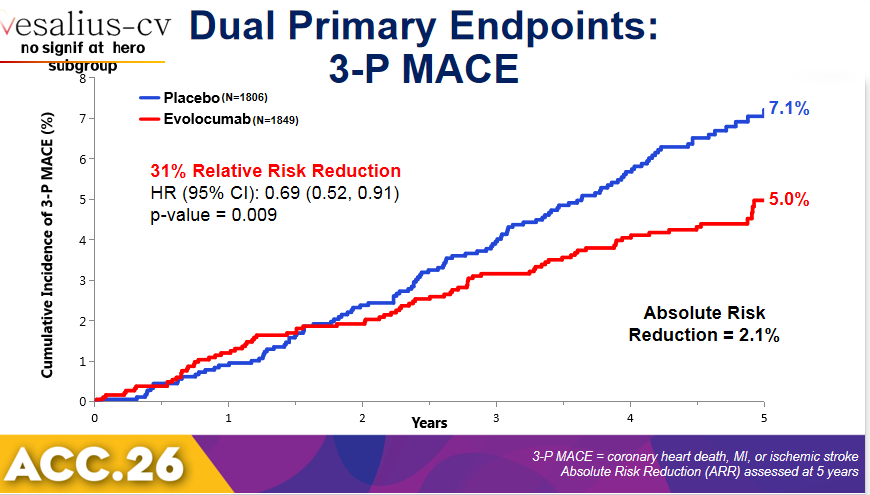
图3 3-P MACE风险
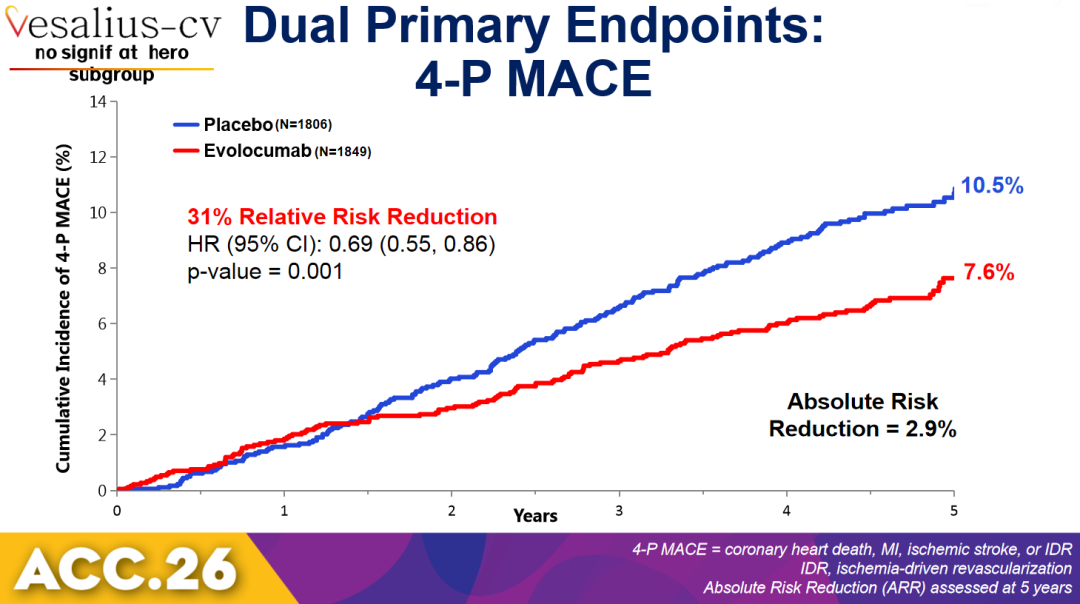
图4 4-P MACE风险
此外,研究的心血管死亡(HR=0.68;95%CI:0.46~0.99,P=0.046)和全因死亡风险(HR=0.76;95%CI:0.61~0.95,P=0.017)亦明显降低。
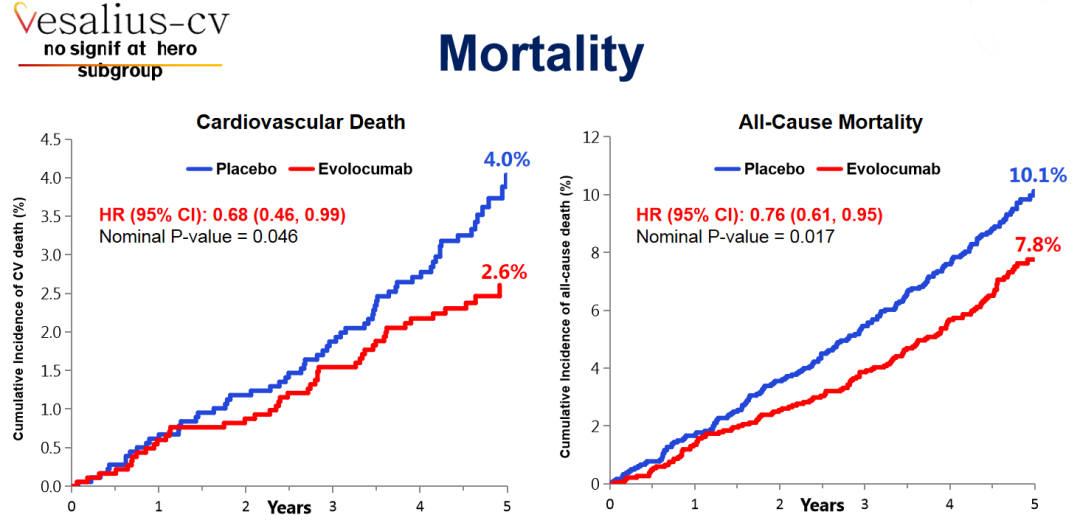
图5 血管死亡和全因死亡风险
在安全性方面,依洛尤单抗组与安慰剂组的严重不良事件(包括被认为与研究药物相关的事件,以及导致研究药物停药的事件)发生率相似。
表1 安全性结局
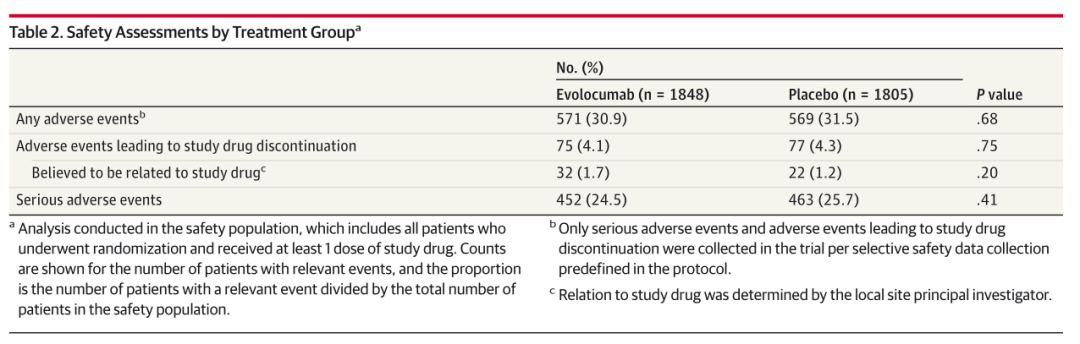
研究表明,在无显著动脉粥样硬化的糖尿病患者中,依洛尤单抗可显著降低首发MACE、心血管死亡及全因死亡风险。本亚组分析结果支持,在动脉粥样硬化性心血管疾病病程更早阶段,启动他汀以外的强化降脂治疗。
本研究的临床获益幅度与CTTC(胆固醇治疗试验协作组)试验的预期结果一致,凸显了将此类患者的LDL-C水平降至约40 mg/dL的价值。这些研究数据强烈支持,在此类风险相对较低的患者,可采用既往仅用于极高危二级预防人群的LDL-C目标值。
本研究未要求进行系统性影像学检查,部分患者或存在未被诊断的显著动脉粥样硬化,但该情况也符合指南推荐与临床实践现状。
此外,所有入组患者均为高危糖尿病患者,或无法延展至其他无已知动脉粥样硬化的高危人群。因此,在其他类型的无已知动脉粥样硬化高危人群中验证本结论具有重要意义。
SURPASS-CVOT试验事后分析:替尔泊肽可显著降低糖尿病合并心血管疾病患者的心肾不良事件风险
来自克利夫兰诊所的Steven E. Nissen教授在FCR II专场公布了SURPASS-CVOT试验事后分析的结果,证实替尔泊肽在心肾保护方面显著优于度拉糖肽,为2型糖尿病 合并心血管疾病患者的优选治疗提供了关键证据。研究结果已同步发表于JAMA杂志。
合并心血管疾病患者的优选治疗提供了关键证据。研究结果已同步发表于JAMA杂志。
GLP-1受体激动剂可降低ASCVD合并糖尿病、肥胖或慢性肾脏病 (CKD)患者的主要不良心血管与肾脏结局风险。替尔泊肽是GLP-1/GIP双受体激动剂,在体重、血糖控制及与不良心肾结局相关的生物标志物方面均可使患者获益。然而,尚无研究对比替尔泊肽和GLP-1受体激动剂度拉糖肽的主要心血管和肾脏不良事件结局。
(CKD)患者的主要不良心血管与肾脏结局风险。替尔泊肽是GLP-1/GIP双受体激动剂,在体重、血糖控制及与不良心肾结局相关的生物标志物方面均可使患者获益。然而,尚无研究对比替尔泊肽和GLP-1受体激动剂度拉糖肽的主要心血管和肾脏不良事件结局。
SURPASS-CVOT试验是首项头对头比较替尔泊肽和度拉糖肽心血管结局的研究,已发布的主要研究结果表明在2型糖尿病合并ASCVD患者中,替尔泊肽与度拉糖肽相比具有非劣效性。本事后分析旨在比较替尔泊肽与度拉糖肽对2型糖尿病合并心血管疾病患者多种不良心肾结局的影响。
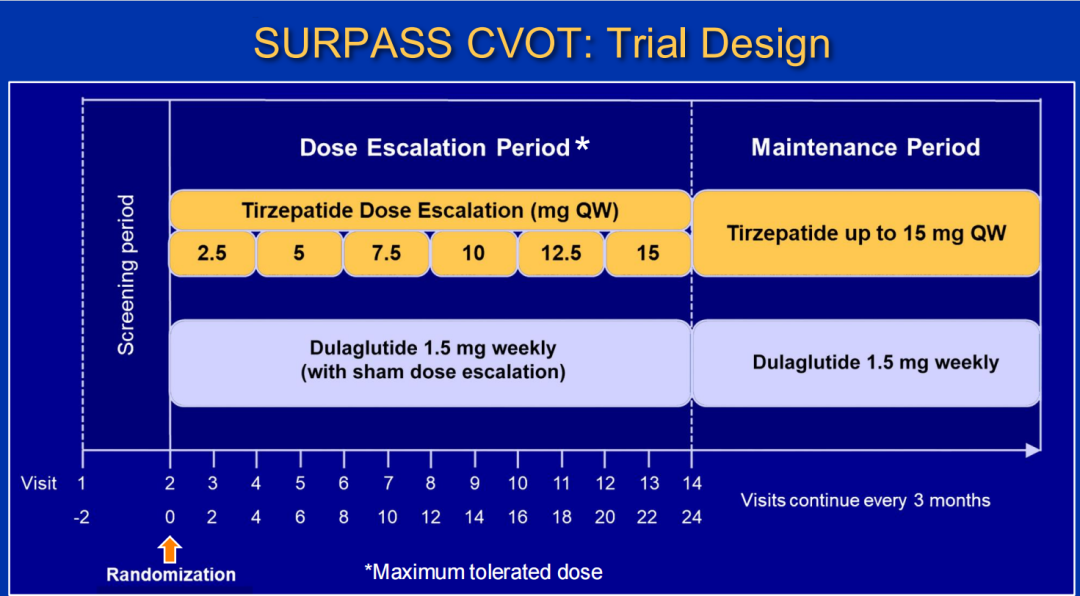
图6 研究设计
SURPASS-CVOT是一项全球多中心、随机、双盲、活性药物对照试验,共纳入北美、南美、欧洲、亚洲及大洋洲640家中心的13299例患者(其中134例因不符合入组标准而终止),并以1:1比例随机分为替尔泊肽组(6586例,最大剂量15 mg,每周1次)和度拉糖肽组(6579例,1.5 mg,每周1次)。
主要疗效终点为6组分不良心肾事件复合终点,包括全因死亡、心肌梗死、卒中、冠状动脉血运重建、心力衰竭住院及肾脏不良事件。敏感性分析终点为5组分终点(去掉不良肾脏结局)和4组分终点(去掉不良肾脏结局和心力衰竭终点)。关键次要终点包括MACE、肾脏不良事件及全因死亡风险等。
最终研究共纳入13165例患者,平均年龄64(8.8)岁,女性占29.0%,白人占 81.5%;47%既往心肌梗死史,19%既往卒中史,25%既往外周动脉疾病 史。
史。
基线时,平均LDL-C为81 mg/dL,平均糖化血红蛋白 (HbA1c)为8.4%。
(HbA1c)为8.4%。
中位随访46.9 个月显示,23.7%的替尔泊肽组患者和27.4%的度拉糖肽组患者达到了主要心肾终点(HR=0.84;95%CI:0.79-0.90;P<0.001),且所有单一组分终点(MACE,包括肾功能恶化、白蛋白尿 升高等关键事件的肾脏复合终点、全因死亡)均显示替尔泊肽组事件更少。
升高等关键事件的肾脏复合终点、全因死亡)均显示替尔泊肽组事件更少。
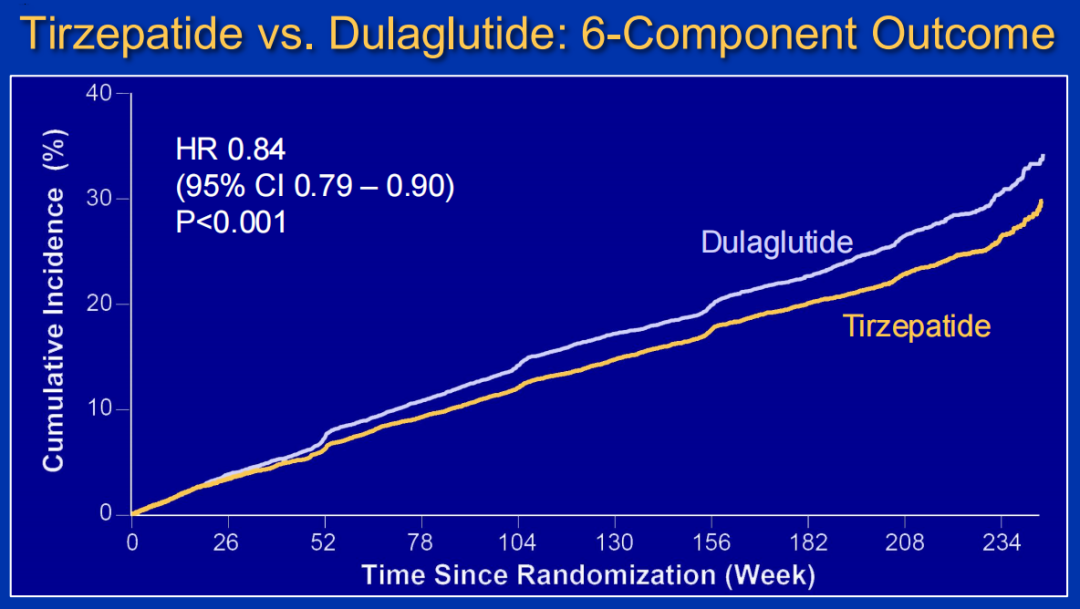
图7主要疗效终点(6组分不良心肾事件复合终点)
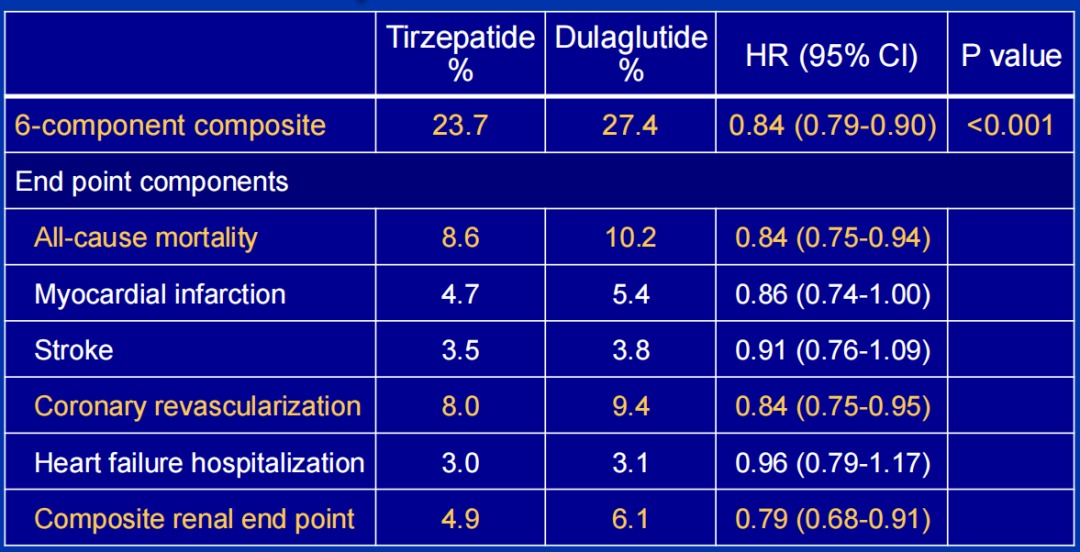 图8 主要疗效终点(6组分不良心肾事件复合终点及其各组成部分)
图8 主要疗效终点(6组分不良心肾事件复合终点及其各组成部分)
敏感性分析结果一致:5组分复合终点(HR=0.86;95% CI:0.80~0.93,P<0.001)和4组分复合终点(HR=0.86;95% CI:0.80~0.93,P<0.001)风险比相似。
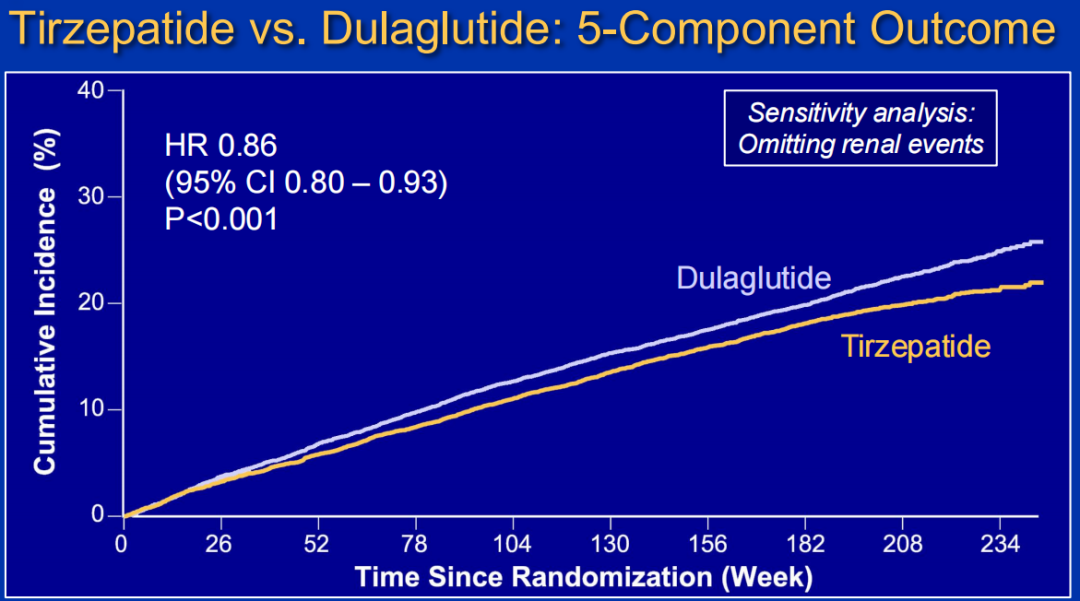
图9 5组分复合终点
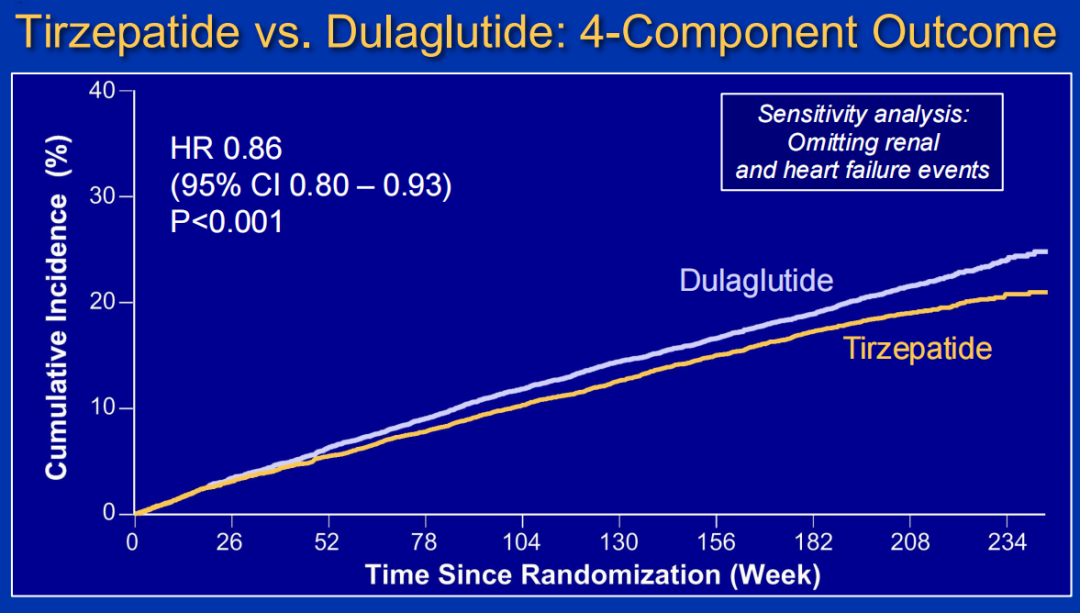
图10 4组分复合终点
在安全性方面,替尔泊肽组的胃肠道不良事件风险稍高(42.5% vs 35.9%),其他不良事件发生率两组相似,总体耐受性较好。
本次事后分析结果显示,在2型糖尿病合并心血管疾病患者中,GLP-1/GIP双受体激动剂替尔泊肽较度拉糖肽,可显著降低6组分复合心肾终点的发生风险。
信源:ACC 官网
编辑&排版:GXM
医脉通是专业的在线医生平台,“感知世界医学脉搏,助力中国临床决策”是平台的使命。医脉通旗下拥有「临床指南」「用药参考」「医学文献王」「医知源」「e研通」「e脉播」等系列产品,全面满足医学工作者临床决策、获取新知及提升科研效率等方面的需求。
本平台旨在为医疗卫生专业人士传递更多医学信息。本平台发布的内容,不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议。如该等信息被用于了解医学信息以外的目的,本平台不承担相关责任。本平台对发布的内容,并不代表同意其描述和观点。若涉及版权问题,烦请权利人与我们联系,我们将尽快处理。
