
卵巢癌患者的基因检测及遗传咨询
作者:曹波,黄奕等,湖北省肿瘤医院妇瘤科
国家癌症中心数据表明,2022年我国新发卵巢癌 约6.11万人,死亡3.26万人[1] 。由于缺乏有效筛查手段且早期无明显症状,卵巢癌初诊时多为晚期且疗效有限,成为妇科常见恶性肿瘤中死亡率最高的疾病。卵巢癌的病因、预防及控制策略一直是临床研究重点。20世纪70年代,研究发现癌症的发生与遗传因素相关。随后,卵巢癌等遗传性癌症综合征逐渐被识别[2] 。研究发现,母亲或姐妹罹患卵巢癌或乳腺癌
约6.11万人,死亡3.26万人[1] 。由于缺乏有效筛查手段且早期无明显症状,卵巢癌初诊时多为晚期且疗效有限,成为妇科常见恶性肿瘤中死亡率最高的疾病。卵巢癌的病因、预防及控制策略一直是临床研究重点。20世纪70年代,研究发现癌症的发生与遗传因素相关。随后,卵巢癌等遗传性癌症综合征逐渐被识别[2] 。研究发现,母亲或姐妹罹患卵巢癌或乳腺癌 的直系亲属是遗传性卵巢癌的高风险人群[3] 。在最常见的上皮性卵巢癌中,约24%与家族性或遗传性卵巢癌综合征(hereditaryovarian cancer syndromes,HOCS)相关,HOCS患者携带可遗传的肿瘤抑制基因突变[4] 。通过基因检测识别高风险个体和家庭,并提供遗传咨询和管理措施,可有效降低卵巢癌的发生率和死亡率。因此,卵巢癌患者的基因检测及遗传咨询具有重大意义。
的直系亲属是遗传性卵巢癌的高风险人群[3] 。在最常见的上皮性卵巢癌中,约24%与家族性或遗传性卵巢癌综合征(hereditaryovarian cancer syndromes,HOCS)相关,HOCS患者携带可遗传的肿瘤抑制基因突变[4] 。通过基因检测识别高风险个体和家庭,并提供遗传咨询和管理措施,可有效降低卵巢癌的发生率和死亡率。因此,卵巢癌患者的基因检测及遗传咨询具有重大意义。
1与HOCS相关的基因改变
目前,HOCS的主要类型包括遗传性乳腺癌/卵巢癌综合征(hereditary breast/ovarian cancer syndrome,HBOCS)及林奇综合征(Lynch syndrome,LS),相关研究多聚焦于这两者相关的基因改变。
1.1 Fanconi贫血 通路相关基因
通路相关基因
与遗传性卵巢癌风险相关的基因中,最常见的是Fanconi贫血通路中的乳腺癌易感基因BRCA1和BRCA2,呈常染色体 显性遗传,突变后可增加HBOCS、男性前列腺癌
显性遗传,突变后可增加HBOCS、男性前列腺癌 、胰腺癌
、胰腺癌 、黑色素瘤
、黑色素瘤 等患病风险。BRCA1和BRCA2基因突变携带者发生卵巢癌风险分别为40%和18%[5-6 ] ,卵巢癌中位发病年龄分别为54岁和59.5岁[7] 。其病理类型多为高级别浆液性腺癌。相比未突变患者,这类患者对铂类药物敏感性增加、更易从PARP抑制剂中获益[8] 。Fanconi贫血通路中其他基因的突变也增加了卵巢癌的风险,包括PALB2、ATM、RAD51C/D及BRIP1等。
等患病风险。BRCA1和BRCA2基因突变携带者发生卵巢癌风险分别为40%和18%[5-6 ] ,卵巢癌中位发病年龄分别为54岁和59.5岁[7] 。其病理类型多为高级别浆液性腺癌。相比未突变患者,这类患者对铂类药物敏感性增加、更易从PARP抑制剂中获益[8] 。Fanconi贫血通路中其他基因的突变也增加了卵巢癌的风险,包括PALB2、ATM、RAD51C/D及BRIP1等。
1.2错配DNA修复通路基因
林奇综合征是最常见的遗传性癌症综合征,患者携带错配修复基因突变,易罹患结肠癌 、子宫内膜癌
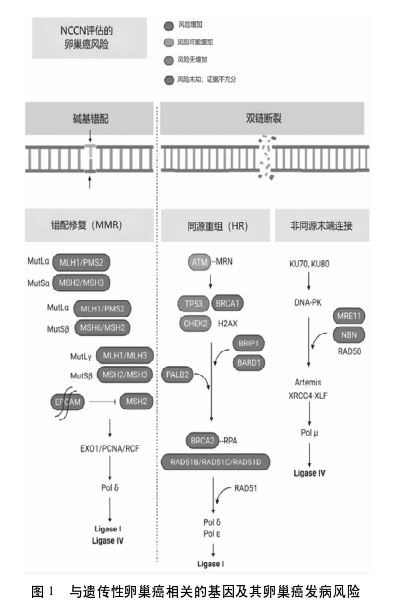
、子宫内膜癌 及其他癌症[9] 。除子宫内膜癌,林奇综合征患者卵巢癌发生概率也增加,75岁的发病风险分别为MLH1突变携带者的11%、MSH2突变携带者的17.4%、MSH6突变携带者的10.8%[10] 。林奇综合征相关卵巢癌平均发病年龄为45.3岁(19~82岁),常见突变为MSH2(47%)和MLH1(38%),常见的组织学类型为混合型(黏液性/子宫内膜样/透明细胞癌)。65%的患者就诊时为早期(FIGOⅠ/Ⅱ期)[1] 。与遗传性卵巢癌相关的基因及其卵巢癌发病风险见图1。
及其他癌症[9] 。除子宫内膜癌,林奇综合征患者卵巢癌发生概率也增加,75岁的发病风险分别为MLH1突变携带者的11%、MSH2突变携带者的17.4%、MSH6突变携带者的10.8%[10] 。林奇综合征相关卵巢癌平均发病年龄为45.3岁(19~82岁),常见突变为MSH2(47%)和MLH1(38%),常见的组织学类型为混合型(黏液性/子宫内膜样/透明细胞癌)。65%的患者就诊时为早期(FIGOⅠ/Ⅱ期)[1] 。与遗传性卵巢癌相关的基因及其卵巢癌发病风险见图1。
2 HOCS相关的基因检测
尽管上世纪90年代已明确BRCA基因的突变与HOCS密切相关,且后续研究也证实了其它相关基因突变,但肿瘤医生对基因检测的认识主要是在靶向或免疫治疗的开展后逐步提高的,例如PARP酶抑制剂用于BRCA突变携带者、免疫检查点抑制剂用于微卫星不稳定或错配修复缺陷的肿瘤等[12] ,均需行基因检测。目前,对于HOCS相关的基因检测,国内外的指南都有相应的推荐。
2.1基因检测的适用人群
遗传性卵巢癌的基因检测旨在寻找致病突变靶点及验证患者亲属的致病突变位点,由此评估患癌风险,明确筛查和预防措施[13] 。建议对上皮性卵巢癌患者、携带遗传性致病突变位点患者的家属进行相关基因的检测(年龄未满18岁者不推荐检测)。
2.2基因检测的内容、方式、样本与检测
2.2.1方法关键致病基因检测研究结果表明,某些基因的异常与家族性卵巢癌综合征明确相关。国内指南建议,应对11种与家族性卵巢癌综合征相关的基因进行检测,其中包括:Fanconi贫血通路相关的基因BRCA1/2、RAD51C、RAD51D、BRIP1、PALB2、ATM以及Lynch综合征相关基因(MLH1、MSH2、MSH6、PMS2、EPCAM)[15 ] 。
2.2.2单基因检测与多基因检测近年来,随着PARP酶抑制剂的推广应用,伴随诊断的BRCA基因突变检测也日益增多。因此,临床上BRCA的单基因检测使用最多。以BRCA为主的单基因检测,可协助临床评估患者预后、指导临床用药、明确HOCS家系,可以从检测结果、家族史中开展遗传咨询工作。
ASCO指南推荐,上皮性卵巢癌需开展包含多个基因的组合检测,其中包括BRCA1,BRCA2,BRIP1,EPCAM,MLH1,MSH2,MSH6,PALB2,PMS2,RAD51C, RAD51D基因。而包含多个基因的组合检测,有利于发现更多的HOCS、更好地筛选出靶向或免疫药物的获益人群。
单基因检测价格相对低廉,在临床上更容易开展与推广。多基因检测因其价格昂贵、检测项目不容易开展,在临床上推广相对困难。
2.2.3基因检测样本采集由于遗传性肿瘤携带者体内细胞均表现出相关基因异常,因此,与其它遗传性肿瘤一样,HOCS患者体内细胞均可作为检测样本。结合采样和检测的便利性,临床上多采用血液或唾液为检测样本。血液样本采用一次性EDTA抗凝管采集,2~5m L血液中提取的DNA可满足大多数检测需求;唾液样本中含口腔脱落细胞,一般2 m L唾液中的DNA可满足检测要求。某些特殊人群,如接受过输血 或骨髓移植,其血液或唾液中存在供体DNA污染,将影响检测结果。这类患者可采用带毛囊的头发作为样本,不易受供体干扰。这类人群最为准确的方法是提取患者的成纤维细胞行体外培养后提取DNA进行检测[16] ,但该方法要求较高,一般难以推广实施。
或骨髓移植,其血液或唾液中存在供体DNA污染,将影响检测结果。这类患者可采用带毛囊的头发作为样本,不易受供体干扰。这类人群最为准确的方法是提取患者的成纤维细胞行体外培养后提取DNA进行检测[16] ,但该方法要求较高,一般难以推广实施。
2.2.4基因检测方法目前,对于家族遗传性肿瘤的基因检测主要采用二代测序(next generationsequencing,NGS)的方法检测DNA碱基变异、小片段缺失或插入及甲基化,该方法具有速度快、成本低、灵敏度高的特点。当基因组出现基因组中较大区域的DNA序列的缺失或重复时,称为大片段重排(Large GenomicRearrangements,LGR),此类变异常常也导致基因功能的改变。采用NGS的检测方法难以发现大片段重排。多重链接依赖探针扩增技术(Multiplex Ligation-dependentProbeAmplification,MLPA)是最常用的检测LGR的方法,也是目前LGR检测的金标准。
当先证者(患者)检测发现基因异常的位点时,亲属家系验证可采取Sanger测序法进行定点验证。
2.3基因检测结果的解读
临床一般使用人类基因组变异协会(HumanGenome Variation Society,HGVS)命名法作为检出基因突变的命名原则,规范基因变异命名。按照ACMG解读规则/分子病理协会(AMP)序列变异解读标准和指南(2015版),遗传性肿瘤相关基因变异的致病性按照风险程度由高至低分为以下5类:致病性(pathogenic,5类)、可能/疑似致病性(likely pathogenic,4类)、意义未明(uncertain significance,3类)、可能良性(likely benign,2类)、良性(benign,1类),其致病可能性分别为>0.99、0.95~0.99、0.05~0.949、0.01~0.049、<0.01。
美国医学遗传学与基因组学学会(The AmericanCollege of Medical Genetics and Genomics,ACMG)强烈建议基因检测应在符合临床实验室改进修正案(CLIA)认证的实验室中进行,其检测结果应由通过职业认证的临床分子遗传学家或分子遗传病理学家或相同职能的专业人员解读。
3 HOCS相关的遗传咨询
遗传性肿瘤与肿瘤相关基因(如抑癌基因、DNA修复基因或癌基因等)的胚系突变有关,遵循孟德尔遗传规律[18] 。这种突变存在于所有体细胞及生殖细胞,并遗传给后代。因此,对HOCS家族成员开展遗传性肿瘤风险评估可有效识别肿瘤高危人群或家族。

随着NGS技术的不断进步以及靶向治疗伴随诊断的需求增长,接受基因检测的肿瘤患者显著增多。共识指出:当为肿瘤患者提供基因检测时,建议进行肿瘤风险评估,评估结果如提示遗传性肿瘤风险高,推荐进行遗传咨询[19] 。
一项研究回顾分析了35项研究的数据[20] ,结果表明:在卵巢癌患者中,不同种族的患者基因检测和遗传咨询的占比有差异,白人、黑人、亚裔患者的基因检测分别占40%、26%和14%,遗传咨询分别占43%、24%、23%。我国尚未见此类报道,以笔者临床经验认为,经济发达地区患者接受基因检测和遗传咨询的比例明显高于经济欠发达地区,这可能与检测的可及性、患者的经济条件、临床医生及患者、家属对于遗传性肿瘤的认知有关。
3.1 HOCS的遗传咨询对象
多项共识指出,具有下列1种或多种情形的妇女患有遗传性卵巢癌、输卵管癌或腹膜癌的可能性增加,应接受遗传咨询并进行基因检测:(1)卵巢上皮性癌、输卵管癌或腹膜癌。(2)年龄≤50岁,患有乳腺癌并有卵巢癌家族史;有卵巢上皮性癌、输卵管癌或腹膜癌家族史。(3)患有胰腺癌并有超过2个近亲患有乳腺癌、卵巢癌、输卵管癌或腹膜癌、胰腺癌或浸润性前列腺癌(Gleason评分≥7)。(4)需要不影响生理需求和保留生育功能的所有年轻恶性肿瘤患者。未患癌症的妇女具有下列1种或多种情形时,遗传性乳腺癌、卵巢癌、输卵管癌或腹膜癌的患病可能性增加,应接受遗传咨询并进行基因检测:(1)符合上述[34-35] 1个或多个标准的一级或多级近亲[36-37] 属。(2)1名近亲携带已知突变的BRCA1或BRCA2。(3)1名近亲患有男性乳腺癌。(4)已知遗传性肿瘤相关基因致病性/可能致病性(pathogenic/likelypathogenic,P/LP)状态的携带者。
3.2 HOCS遗传咨询的提供者
共识认为,遗传咨询师、医学遗传学家、肿瘤内科医师、外科医师、肿瘤科护士或其他在肿瘤遗传学方面具有相关知识和经验的专业人员都应尽早参与到遗传咨询工作中[19] 。然而,我国肿瘤遗传咨询工作起步较晚,肿瘤相关遗传咨询师欠缺,尤其是获得国家认证的肿瘤遗传咨询师。因此,大部分的肿瘤风险评估和遗传咨询工作目前由临床肿瘤医生承担。
3.3 HOCS的遗传咨询模式
目前,在熟悉患者的病史、家族史的前提下,多数医生采用面对面的遗传咨询方式。随着遗传咨询需求的增加,有限的人力资源难以对高危个体提供面对面遗传咨询[38-39] 。人们一直在探索更为便捷的方式开展遗传咨询。一项随机对照研究表明,针对HBOC的遗传咨询中,接受电话咨询的效果并不亚于面对面咨询[22] 。另外,也可采用视频遗传咨询及多学科会诊模式。
3.4 HOCS的遗传咨询流程
中国抗癌协会发布的妇科肿瘤 遗传咨询专家共识中,明确了开展HOCS的遗传咨询流程。
遗传咨询专家共识中,明确了开展HOCS的遗传咨询流程。
3.4.1检测前咨询在检测前遗传咨询时,首先,需评估咨询者的需求、了解咨询的目的,其次,需要评估咨询者个人和家族病史。包括:(1)采集全面的临床信息。(2)准确、详尽地收集家族史,应收集至少三代血亲家族史。(3)咨询者及其家庭成员之前基因检测结果的文件、详细的个人史。(4)体格检查。(5)绘制家系图谱。
3.4.2基因检测在进行风险评估后,咨询师应告知咨询者检测项目,制订最优的基因检测方案,并告知可能的检测结果,包括阳性(致病性、可能致病性)、阴性、意义未明或嵌合型变异结果和意外发现等,并签署知情同意书。
3.4.3检测后咨询若发现致病性及可能致病性变异,咨询师应与咨询者讨论可能的管理方案,包括如何加强监测、降低风险药物治疗和手术等。由于卵巢癌缺乏有效的筛查手段及降低风险的药物,目前关于HOCS的管理建议,主要是降低风险的双附件切除手术(risk-reducing bilateral salpingooophorectomy,RRBSO)。依据不同基因突变携带者发生卵巢癌的高发年龄,来推荐接受降风险手术的年龄。若家族成员发病年龄提前,则接受RRBSO的年龄应相应提前,具体推荐参见下页表1[4-13] 。对于生育年龄患者,应提供产前诊断和辅助生殖的选择,包括胚胎植入前的遗传学检测(preimplantation genetic testing,PGT)等,通过辅助生殖等干预措施,阻断突变遗传。
综上所述,约24%的上皮性卵巢癌与HOCS相关,其本质是此类患者携带可遗传的基因突变。当前,我国不同地区基因检测以及遗传咨询的普及率差异较大,受限于检测的可及性、患者经济条件及医患认知水平,通过遗传咨询降低高危人群卵巢癌发病率依然面临挑战。因此,亟需在临床工作中普及遗传性肿瘤的相关知识,妇科肿瘤医务工作者应掌握相关理论知识,识别HOCS患者群体,并积极开展遗传咨询,推荐相关的基因检测、针对检测报告做出合理的解读并为患者提供合理规范的管理方案,推荐适时的降风险的手术治疗。通过大力开展遗传咨询工作,使肿瘤遗传咨询工作规范化、普及化,以此有效降低卵巢癌的发生风险。
利益冲突作者均声明无利益冲突。
参考文献略。
来源:曹波,黄奕.卵巢癌患者的基因检测及遗传咨询[J].中国计划生育和妇产科,2026,18(01):25-28.
