
杨永峰/李莎莎:抗核抗体阳性提示高炎症负荷表型:原发性胆汁性胆管炎患者的多中心回顾性分析
来源:中华肝脏病杂志
引 用 本 文
李莎 莎, 李睿佳,张宇
莎, 李睿佳,张宇 , 姬文京, 包一珺,刘红
, 姬文京, 包一珺,刘红 丽, 龚宇翔,王怡
丽, 龚宇翔,王怡 婷, 陶宇林, 吴志贤,张瑜
婷, 陶宇林, 吴志贤,张瑜 , 张文华,李雯
, 张文华,李雯 ,叶峰
,叶峰 , 闫雪华, 毛天皓, 刘星,张凯
, 闫雪华, 毛天皓, 刘星,张凯 ,杨永峰
,杨永峰 . 抗核抗体阳性提示高炎症负荷表型:原发性胆汁性胆管炎
. 抗核抗体阳性提示高炎症负荷表型:原发性胆汁性胆管炎 患者的多中心回顾性分析[J]. 中华肝脏病杂志, 2026, 34(2):161-169. DOI: 10.3760/cma.j.cn501113-20251017-00440.
患者的多中心回顾性分析[J]. 中华肝脏病杂志, 2026, 34(2):161-169. DOI: 10.3760/cma.j.cn501113-20251017-00440.
通信作者:杨永峰,南京大学医学院教学医院南京市第二医院肝病科
专 家 简 介
杨永峰 教授
南京市第二医院院长,肝病学科带头人
医学博士,二级主任医师,教授,博士生导师
中华医学会肝病学分会委员、感染病学分会委员
江苏省感染病质量控制中心主任
江苏省中西医结合学会肝病分会主任委员
江苏省医学会
 肝病学分会副主任委员
肝病学分会副主任委员《新发传染病电子杂志》副主编,《中华肝脏病杂志》、《中华传染病杂志》、《中华临床感染病杂志》等杂志编委
江苏省有突出贡献中青年专家,第10届中国医师奖获得者
江苏省医学重点人才,江苏省卫生拔尖人才
发表第一或通信作者论文100余篇,其中SCI 50余篇,中华期刊论文30余篇,主持国家自然科学基金1项,江苏省自然科学基金、江苏省科技厅临床医学专项等课题9项,获江苏省科技进步一等奖等奖项10余项
精通肝脏疾病的临床、病理和影像诊断,擅长疑难重症肝病诊治
专 家 简 介
李莎莎 博士
南京大学医学院在读博士,师从杨永峰教授。研究方向为原发性胆汁性胆管炎中重度界面炎的临床和基础研究,以第一或共一作者发表SCI 4篇。相关研究摘要多次被亚太肝脏研究协会年会接收为口头报告及壁报交流
正文
原发性胆汁性胆管炎(primary biliary cholangitis,PBC)是一种由免疫介导的、以进行性破坏小叶间胆管为特征的非化脓性慢性胆汁淤积 性疾病,可进展至肝硬化甚至肝衰竭
性疾病,可进展至肝硬化甚至肝衰竭 [1-2]。其确切发病机制尚未完全阐明,遗传易感性、环境因素、免疫失调及感染因素均被认为参与其中。鉴于遗传背景与致病机制存在交叉重叠,PBC 常合并多种肝外自身免疫性疾病[3],尤以风湿免疫性疾病为著[4]。抗核抗体(antinuclear antibodies,ANAs)是一组针对细胞核内及胞质成分的自身抗体总称,研究结果显示其有助于临床医生识别自身免疫性肝病[5]。然而,在 PBC 患者群体中,尽管 ANAs 检出率较高[6-7],其与患者临床表现、疾病进展、特征性肝脏组织病理学表现如胆管损伤程度、界面性肝炎、纤维化分期等及预后之间的确切关联性,尚缺乏在充分控制潜在混杂因素研究中的明确阐释。因此,本研究拟采用倾向性评分匹配方法,通过严格匹配关键基线协变量,构建基线特征可比的患者队列,旨在系统探究ANAs对PBC患者临床表现、实验室指标、肝脏组织病理学特征及治疗反应的影响。
[1-2]。其确切发病机制尚未完全阐明,遗传易感性、环境因素、免疫失调及感染因素均被认为参与其中。鉴于遗传背景与致病机制存在交叉重叠,PBC 常合并多种肝外自身免疫性疾病[3],尤以风湿免疫性疾病为著[4]。抗核抗体(antinuclear antibodies,ANAs)是一组针对细胞核内及胞质成分的自身抗体总称,研究结果显示其有助于临床医生识别自身免疫性肝病[5]。然而,在 PBC 患者群体中,尽管 ANAs 检出率较高[6-7],其与患者临床表现、疾病进展、特征性肝脏组织病理学表现如胆管损伤程度、界面性肝炎、纤维化分期等及预后之间的确切关联性,尚缺乏在充分控制潜在混杂因素研究中的明确阐释。因此,本研究拟采用倾向性评分匹配方法,通过严格匹配关键基线协变量,构建基线特征可比的患者队列,旨在系统探究ANAs对PBC患者临床表现、实验室指标、肝脏组织病理学特征及治疗反应的影响。
资料与方法
1. 研究对象:本研究为多中心回顾性病例对照研究,纳入了 2017 年 1 月至 2023 年 10 月在 8 家医疗中心(南京市第二医院 、联勤保障部队第九〇〇医院、昆明医科大学第二附属医院、青海省第四人民医院、兰州市第二人民医院、甘肃武威肿瘤医院、威海市立医院、西安交通大学第一附属医院)就诊的 690 例 PBC 患者。纳入标准:(1)符合中华医学会肝病学分会制定的《原发性胆汁性胆管炎的诊断和治疗指南(2021)》中 PBC 诊断标准[8];(2)接受肝脏穿刺活组织检查(简称活检)。排除标准:(1)合并其他肝脏疾病如病毒性肝炎 、代谢相关性脂肪肝
、代谢相关性脂肪肝 病、酒精性肝病等;(2)合并影响肝功能的结缔组织病如系统性红斑狼疮;(3)肝组织样本量不足;(4)缺乏必需临床数据;(5)合并艾滋病
病、酒精性肝病等;(2)合并影响肝功能的结缔组织病如系统性红斑狼疮;(3)肝组织样本量不足;(4)缺乏必需临床数据;(5)合并艾滋病 ;(6)年龄<18 岁。本研究为回顾性研究,豁免知情同意,并获得南京市第二医院伦理委员会通过[批文号(2024-LS-ky-607)]。
;(6)年龄<18 岁。本研究为回顾性研究,豁免知情同意,并获得南京市第二医院伦理委员会通过[批文号(2024-LS-ky-607)]。
2. 研究指标及定义:患者数据采集自电子健康记录系统,包括人口学与临床基线资料 、血液学指标、肝脏生物化学指标、自身抗体谱及免疫球蛋白水平。为确保数据准确性与一致性,基线数据仅分析肝活检前 14 d 内的实验室结果。所有连续变量在分析前均进行标准化处理。所有患者均行超声引导下肝活检,组织长度≥1 cm 且包含≥6 个汇管区判断为样本量充足。病理评估由南京市第二医院 2 名资深病理医师采用双盲法完成。界面性肝炎依据淋巴浆细胞 浸润范围分为:无、轻度(<1/3 汇管区周长)、中度(1/3~1/2 汇管区周长)及重度(>1/2 汇管区周长)。
浸润范围分为:无、轻度(<1/3 汇管区周长)、中度(1/3~1/2 汇管区周长)及重度(>1/2 汇管区周长)。
Ludwig 分期系统采用 1978 年 Ludwig 提出的PBC分期系统[8],Ⅰ期组织学改变为汇管区炎症;Ⅱ期组织学改变为汇管区周围炎,即界面炎;Ⅲ期出现桥接坏死、纤维化;Ⅳ期为肝硬化。Nakanuma 评分[9]根据纤维化、胆管缺失和坏死性炎症活动的严重程度进行分期和分级。(1)纤维化评分:0 分为几乎没有纤维化或纤维化局限于汇管区;1 分为纤维化范围超出汇管区,偶有不完全纤维间隔;2 分为桥接纤维化伴小叶紊乱;3 分为肝硬化(广泛纤维化和再生结节);(2)胆管缺失评分,0 分为标本中的所有汇管区均可见小叶间胆管;1 分和 2 分分别为<1/3 和 1/3~2/3 的汇管区有胆管缺失;3分为 >2/3 的汇管区有胆管缺失;(3)在对每一项进行评分后,获得总分,根据总分进行分期。因无常规进行地衣红染色,则纤维化和胆管缺失评分的总和也适用[10]。 Ⅰ 期( 无进展 ):总分为 0 分 ;Ⅱ 期( 轻度进展):总分为 1~2 分;Ⅲ期(中度进展):总分为 3~4 分;Ⅳ期(重度进展):总分为 5~6 分;(4)坏死性炎症活动分级,分为胆管炎活动(cholangitis activity,CA)和肝炎活动(hepatitis activity,HA)。CA 分级为 4 个等级:CA0(无活动):无胆管炎,但可能存在轻度胆管上皮细胞损伤;CA1(轻度活动):可见1个受损的胆管完全被轻度-中度的淋巴-浆细胞包围;CA(2 中度活动):超过 2 个胆管伴有明显的慢性胆管炎;CA(3 重度活动):至少有 1 个受损的胆管表现为慢性非化脓性胆管炎,慢性非化脓性胆管炎表现为胆管上皮细胞受损,胆管完全被大量的淋巴-浆细胞浸润,受损的胆管部分或全部被上皮样肉芽肿包围。HA 分为 4 个等级:HA0(无活动):无界面肝炎,且无或最轻微的小叶性肝炎;HA1(轻度活动):指界面肝炎累及一个汇管区或纤维间隔周围连续 10 个肝细胞,且有轻度 - 中度小叶性肝炎;HA2(中度活动):界面肝炎累及 2 个以上汇管区或纤维间隔周围连续 10 个肝细胞,且有轻度-中度小叶性肝炎;HA3(重度活动):界面肝炎累及超过一半数量的汇管区周围连续 20 个肝细胞,且有中度小叶性肝炎或桥接或带状坏死。炎症分级(grading,G)和纤维化分期(staging,S)采用 Scheuer 评分系统[11]。
3. 治疗方案、生物化学应答标准及主要终点事件:熊去氧胆酸 (ursodeoxycholic acid,UDCA)起始剂量为 13~15 mg·kg−1·d−1,部分患者病理表现为中至重度界面性肝炎者酌情加用激素治疗,胆管缺失者酌情加用贝特类药物治疗。生物化学应答标准具体参照参考文献[12-13],即治疗 1 年时碱性磷酸酶水平低于正常范围上限的 1.67 倍,从基线至少降低 15%,且总胆红素水平正常。本研究的主要复合终点为包括随访期间新出现的肝硬化失代偿事件(显性腹水
(ursodeoxycholic acid,UDCA)起始剂量为 13~15 mg·kg−1·d−1,部分患者病理表现为中至重度界面性肝炎者酌情加用激素治疗,胆管缺失者酌情加用贝特类药物治疗。生物化学应答标准具体参照参考文献[12-13],即治疗 1 年时碱性磷酸酶水平低于正常范围上限的 1.67 倍,从基线至少降低 15%,且总胆红素水平正常。本研究的主要复合终点为包括随访期间新出现的肝硬化失代偿事件(显性腹水 ,食管-胃底静脉曲张
,食管-胃底静脉曲张 破裂出血、显性肝性脑病),肝衰竭,肝移植
破裂出血、显性肝性脑病),肝衰竭,肝移植 ,肝脏相关恶性肿瘤以及全因死亡,并采用首次事件分析法进行分析。随访截至2025 年 10 月 12 日。
,肝脏相关恶性肿瘤以及全因死亡,并采用首次事件分析法进行分析。随访截至2025 年 10 月 12 日。
4. 统计学方法:采用 SPSS 26.0 软件进行统计分析。符合正态分布的连续变量以均值±标准差(xˉ±s)表示,组间比较采用独立样本 t检验;非正态分布的连续变量以中位数(四分位数间距)[M(Q1,Q3)]表示,组间比较采用 Mann-Whitney U检验;分类变量以例数(百分比)[例(%)]表示,两组间比较采用χ2检验或 Fisher 精确检验,等级资料采用 Mann-Whitney U检验。在 Kaplan-Meier 生存分析中,通过 log-rank 检验比较组间差异。用 Cox 比例风险模型分析影响预后的风险因素。利用受试者操作特征曲线确定数值变量截断值。P<0.05 为差异有统计学意义。
结 果
1. 倾向性匹配结果:本研究共纳入 690 例确诊 PBC 患者,其中 ANAs 阴性组 96 例,阳性组 594 例,阳性率为 86.1%。为控制基线混杂,采用倾向性评分匹 配 法 :以性 别 及 年 龄 分 层(21~40 岁/41~60 岁/61~76 岁 )为协变量,按 1∶1 比例、卡钳值 0.2 的最近邻法进行匹配。匹配后标准化均数差均<0.1,提示组间基线特征达均衡,最终 192 例样本(96 对)进入后续分析。 匹配队列中位年龄为 52 岁,女性为主,共 146 例(76%)。匹配后两组患者性别、年龄差异均无统计学意义(表 1)。
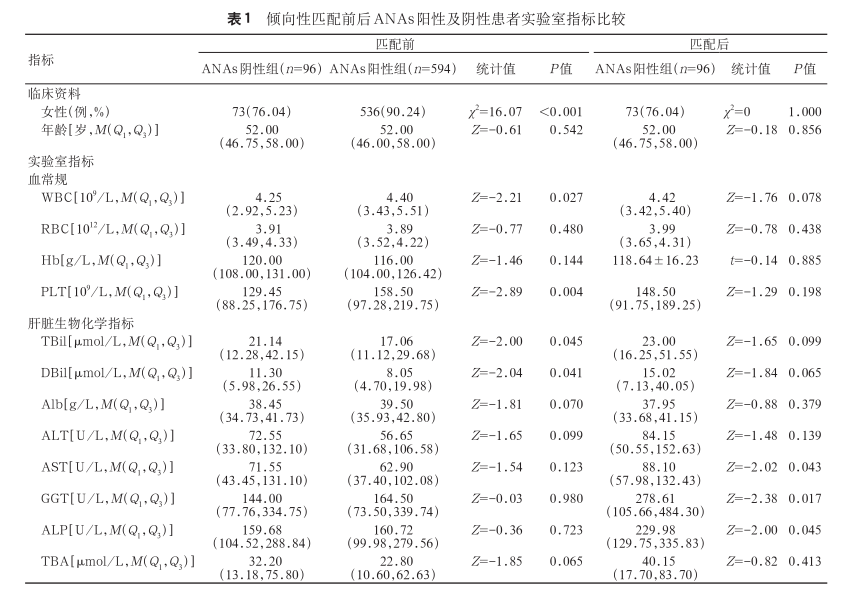
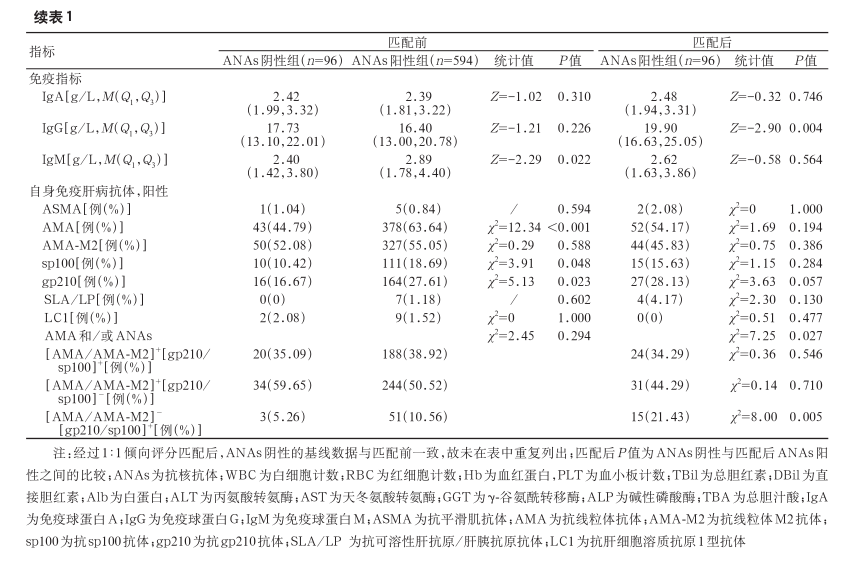
2. 两组患者实验室指标比较:通过对各组患者血常规 、肝功能、免疫球蛋白、自身免疫肝病抗体进行比较分析结果显示,ANAs 阳性组的患者 γ-谷氨酰转移酶、天冬氨酸转氨酶和碱性磷酸酶水平显著高于 ANAs 阴性组,两组比较,差异均有统计学意义(P值均<0.05)。与 ANAs 阴性组相比,ANAs 阳性组的直接胆红素(15.0/μmol/L比 11.3/μmol/L, P=0.065) 和总胆红素(23.0/μmol/L 比 21.1/μmol/L,P=0.099)水平均呈现较高的趋势,但差异无统计学意义。在免疫指标方面,ANAs 阳性组免疫球蛋白 G 水平显著高于 ANAs 阴性组。抗 gp210 抗体阳性率在 ANAs 阳性组较高(28.1% 比 16.7%,P=0.057),(AMA/AMA-M2)-(抗 gp210 抗体/抗 sp100 抗体)+的抗体模式在 ANAs 阳性患者中的发生率更高(21.43% 比5.26%,P=0.005)(表 1)。
、肝功能、免疫球蛋白、自身免疫肝病抗体进行比较分析结果显示,ANAs 阳性组的患者 γ-谷氨酰转移酶、天冬氨酸转氨酶和碱性磷酸酶水平显著高于 ANAs 阴性组,两组比较,差异均有统计学意义(P值均<0.05)。与 ANAs 阴性组相比,ANAs 阳性组的直接胆红素(15.0/μmol/L比 11.3/μmol/L, P=0.065) 和总胆红素(23.0/μmol/L 比 21.1/μmol/L,P=0.099)水平均呈现较高的趋势,但差异无统计学意义。在免疫指标方面,ANAs 阳性组免疫球蛋白 G 水平显著高于 ANAs 阴性组。抗 gp210 抗体阳性率在 ANAs 阳性组较高(28.1% 比 16.7%,P=0.057),(AMA/AMA-M2)-(抗 gp210 抗体/抗 sp100 抗体)+的抗体模式在 ANAs 阳性患者中的发生率更高(21.43% 比5.26%,P=0.005)(表 1)。
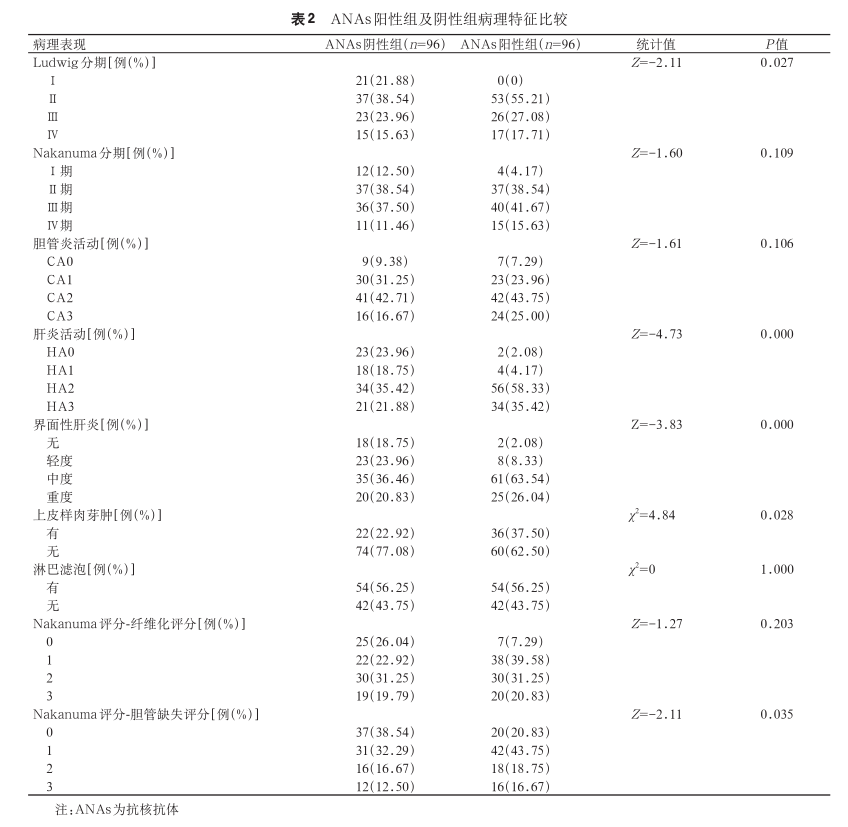
3.ANAs 阳性及阴性 PBC 患者病理特点:ANAs阳性组与阴性组比较显示,Ludwig 分期分布差异显著(P=0.027),ANAs 阳性组分期重于阴性组 。ANAs 阳性组和阴性 Nakanuma 分期总体差异无统计学意义。ANAs 阳性组的炎症活动程度、界面炎程度均显著重于阴性组(P<0.001)。ANAs 阳性组上皮样肉芽肿检出率更高(37.5% 比 22.9%,P=0.028)。其余病理表现如 CA、淋巴滤泡检出率及纤维化评分差异均无统计学意义(P值均>0.05)(表 2)。
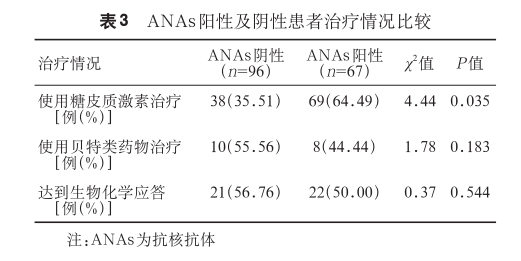
4.ANAs 阳性及阴性 PBC 患者治疗后的生物化学应答情况比较:倾向性匹配的 192 例病例中 162 例来自南京市第二医院,107 例(55.7%)因病情需要接受了糖皮质激素治疗,两组激素治疗情况差异有统计学意义(P=0.035)。18 例(9.4%)在病程中曾使用贝特类药物。在可获得 12 个月随访数据的 81 例患者中,ANAs 阴性组 56.7%(21/37)的患者达到生物化学应答,而 ANAs 阳性组中生物化学应答者为 50.0%(22/44)。两组间生物化学应答率的差异无统计学意义(P=0.544)(表 3)。
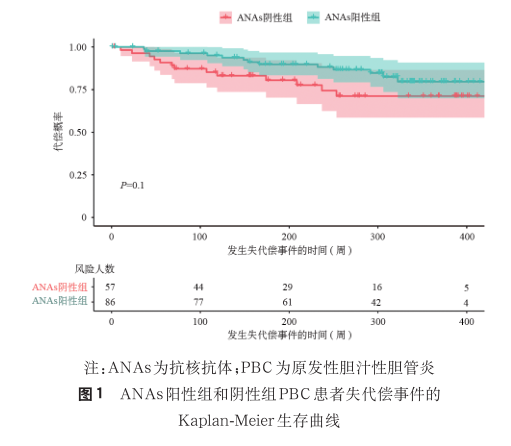
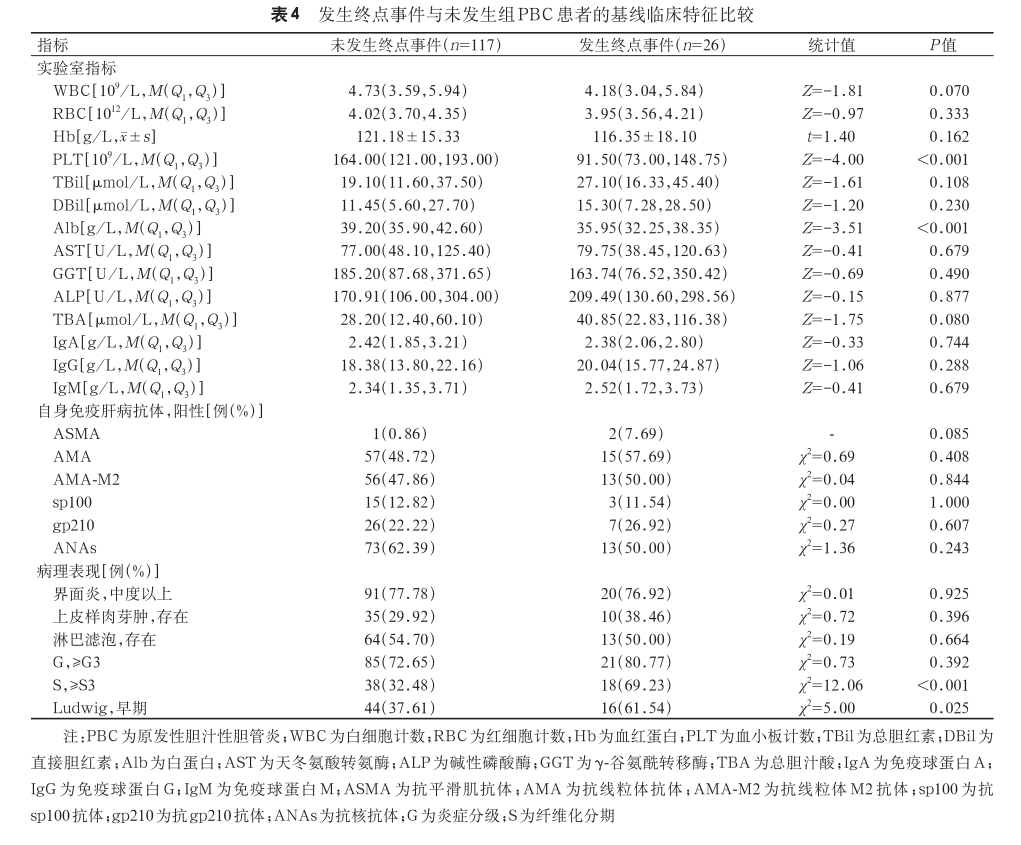
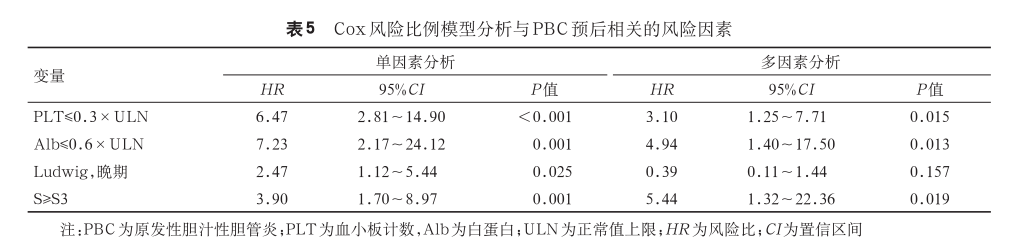
5. 与 PBC 患者预后相关的风险因素:162 例患者中 16 例就诊时已经发生肝硬化失代偿事件,3 例患者失访,失访率 2%。截至随访结束,主要复合终点的累积发生率为 18.2%(26/143),其构成为肝硬化失代偿事件 22 例(15.4%)、全因死亡 3 例(2.1%)及肝脏相关恶性肿瘤 1 例(0.7%)。所有死亡均发生于首次失代偿事件之后,死因均源于肝脏疾病(消化道出血后失血性休克 2 例,肝衰竭后继发感染1例)。采用 Kaplan-Meier 生存曲线比较 ANAs 阳性与 ANAs 阴性 PBC 患者的失代偿发生率的差异(图 1),结果显示 ANAs 阳性患者的失代偿事件发生较早,但两组间差异无统计学意义(log-rank 检验,P=0.103)。对发生终点事件与未发生终点事件患者的基线临床特征进行比较( 表 4),选取 P<0.05 的变量,并借助受试者操作特征曲线以确定数值变量截断值,将其代入 Cox 回归分析。单因素分析显示,血小板计数、白蛋白 、S 分期、Ludwig 分期与失代偿事件显著相关(P<0.05)。经多因素 Cox回归校正各指标间相互影响后,血小板计数≤0.3×正常值上限 、白蛋白≤0.6×正常值上限及 S≥S3 是PBC 患者发生终点事件的独立危险因素(表 5)。
、S 分期、Ludwig 分期与失代偿事件显著相关(P<0.05)。经多因素 Cox回归校正各指标间相互影响后,血小板计数≤0.3×正常值上限 、白蛋白≤0.6×正常值上限及 S≥S3 是PBC 患者发生终点事件的独立危险因素(表 5)。
讨 论
本研究检测到 PBC 患者中 ANAs 阳性率为86.1%,处于国内文献报道的 75.9%~96.2% 区间范围内[7,14]。另有研究结果显示,在 PBC 的早期阶段,当抗线粒体抗体和抗线粒体 M2 抗体均阴性时,ANAs 阳性的检出率高达 92.3%[15]。ANAs 阳性的PBC 患者入院时表现出更高的天冬氨酸转氨酶、碱性磷酸酶、γ-谷氨酰转移酶及免疫球蛋白 G 水平,提示该部分患者存在更严重的肝细胞、胆管损伤及体液免疫活化[16]。本研究观察到 ANAs 阳性患者伴有更高水平的免疫球蛋白 G,这与既往研究结果一致。Li 等[17]的一项大型回顾性分析表明,在非肝硬化PBC 患者中,基线免疫球蛋白 G 升高与 PBC 特异性自身抗体(包括 ANAs、抗 sp100 抗体和抗 gp210 抗体)的阳性率显著相关。免疫球蛋白 G 升高是疾病进展为肝硬化(风险比=9.507)和肝相关死亡(风险比=27.140)的独立高风险因素,而治疗后的免疫球蛋白 G 复常则预示着良好的预后。该研究提示对于ANAs 阳性且免疫球蛋白 G 升高的 PBC 患者,应视为高危人群并进行更密切的监测与管理。研究显示抗线粒体抗体及 PBC 特异性 ANAs 包括抗gp210 和抗 sp100 均阳性对不典型 PBC 的诊断具有极高的价值[18-19],在本研究中我们发现,在抗线粒体抗体及抗线粒体 M2 抗体均为阴性的患者亚组中,ANAs 阳性与抗 gp210 和/或抗 sp100 抗体的检出率显著升高密切相关。对于此类“抗线粒体抗体阴性 PBC”的诊断,国际指南强烈依赖对 ANAs 谱中高度特异性抗体的检测,其中最具代表性的就是抗gp210 和抗 sp100 抗体。我们的数据验证了这一临床实践[20-21]。尽管 ANAs 阳性患者表现出更重的生物化学指标,但在联合使用糖皮质激素的比例显著较高的情况下,其生物化学应答与长期结局与阴性组无显著差异。这一发现提示,部分 ANAs 阳性且具有“高炎症负荷”表型的 PBC 患者,或许能从免疫抑制治疗中获益。本队列中大部分患者肝组织学表现为中至重度界面性肝炎,虽未完全满足巴黎标准而诊断为 PBC-自身免疫性肝炎重叠综合征,但仍接受了糖皮质激素治疗。这一临床决策与近年研究证据相呼应[22]。Wang 等[23]研究表明,对于伴有中重度界面性肝炎的 PBC 患者,UDCA 联合免疫抑制治疗在促进纤维化逆转方面显著优于 UDCA 单药 。对于具有自身免疫特征但不符合典型重叠综合征诊断标准的 PBC 患者,Li 等[24]发现加用免疫抑制剂可改善生物化学应答、无移植生存率并降低失代偿风险。然而,这应严格限于经慎重评估的特定表型患者,并非所有 PBC 患者的常规治疗选择。本研究结果为此类精准治疗策略提供了进一步的临床观察依据。多因素 Cox 回归模型显示,血小板减少、低白蛋白及肝纤维化进展仍是驱动失代偿的关键指标。这与既往研究结果一致[25],提示临床评估 PBC 患者预后时,应重点关注肝储备功能及组织学进展而非单一免疫学表型。
本研究的重要发现为肝组织学分析揭示了ANAs 阳性与阴性 PBC 患者之间存在显著的病理学差异。本研究结果显示 ANAs 阳性 PBC 患者的上皮样肉芽肿检出率显著更高,提示其可能存在更为活跃的 T 细胞介导免疫反应。既往研究曾提出,PBC 肝脏肉芽肿的形成可能与不成熟树突状细胞和免疫球蛋白 M 的相互作用有关。而本研究从血清学角度揭示了 ANAs 状态与肉芽肿形成的潜在关联。该研究结果表明,ANAs 阳性可能反映了特定的免疫激活模式,从而提示 PBC 患者可能存在不同的免疫学亚型,这为深入理解 PBC 的免疫病理提供了新的视角。PBC 的病理损伤模式为胆汁淤积,炎症主要集中在汇管区,小叶炎相对较轻。本研究结果显示 ANAs 阳性患者界面炎严重程度高于 ANAs 阴性患者,提示 ANAs 阳性的患者可能具有自身免疫性肝炎特征。ANAs 阳性组就诊时至少已达到LudwigⅡ期,汇管区炎症已突破界板。以上病理表现均提示 ANAs 阳性的患者炎症活动明显,可建议患者进一步行肝穿刺活检明确是否为 PBC-自身免疫性肝炎重叠综合征,从而及时启动 UDCA 联合免疫抑制剂,改善患者预后。Nakanuma 分期系统根据纤维化、胆管缺失、地衣红阳性颗粒沉积和坏死性炎症活动的严重程度进行分期和分级,可以更为客观地反映疾病的进程。坏死性炎症活动分级,分为 CA 和 HA,这两种病变可导致肝细胞损伤和纤维化逐渐加重,最终形成胆汁性肝硬化和肝功能衰竭。本研究仅发现 ANAs 阳性患者 HA 较重,CA 在两组间无显著差异,考虑可能样本量较小,未得到两者一致变化。而在胆管缺失程度上,ANAs 阳性组患者发生率更高,提示 ANAs 阳性组患者可能预后较差,及时加用贝特类药物的获益情况仍需要开展进一步大规模研究。为评估 PBC-自身免疫性肝炎重叠综合征对本研究结论的可能影响,我们依据巴黎标准进行了敏感性分析。在排除符合该标准的患者后,ANAs 阳性组仍表现出显著更高的基线天冬氨酸转氨酶水平与中重度界面性肝炎比例(数据未展示)。这表明,ANAs 阳性所关联的“高炎症负荷”表型并不仅限于满足现行重叠综合征诊断标准的患者,可能代表了一个更广泛的、具有活跃界面性肝炎的 PBC 疾病谱。
综上所述,本研究在多中心回顾性队列中证实,ANAs 阳性 PBC 患者呈现出“高炎症负荷”表型,表现为更严重的界面炎、肉芽肿形成及胆管缺失。临床仍应加强对 ANAs 阳性患者的随访,必要时行肝活检排查重叠综合征,并考虑早期联合治疗。本研究为回顾性设计,存在一定选择偏倚,且部分患者随访不全。长期结局分析仅基于单中心数据,结论外推需谨慎。未来需开展前瞻性、多中心研究,结合多组学数据进一步阐明其机制,以指导精准干预。
本平台旨在为医疗卫生专业人士传递更多医学信息。本平台发布的内容,不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议。如该等信息被用于了解医学信息以外的目的,本平台不承担相关责任。本平台对发布的内容,并不代表同意其描述和观点。若涉及版权问题,烦请权利人与我们联系,我们将尽快处理。



