
五味子活性成分登上《Nature》子刊|精准燃烧白色脂肪,一夜减重26.8%+胰岛素敏感性飙升,奥利司他黯然失色!
全球肥胖流行已达到触目惊心的程度,超过25亿成年人处于超重状态,其中近9亿人达到肥胖标准,这一数字仍在持续攀升。肥胖不仅是体型问题,更是2型糖尿病 、心血管疾病
、心血管疾病 、非酒精性脂肪性肝病
、非酒精性脂肪性肝病 以及多种恶性肿瘤的独立危险因素,给全球医疗体系带来沉重负担。尽管当前治疗手段包括生活方式干预、药物治疗和减重手术,但均存在明显局限:单纯节食与运动的一年复重率高达50%至三分之二,GLP-1受体激动剂虽风靡全球却伴随胰腺炎
以及多种恶性肿瘤的独立危险因素,给全球医疗体系带来沉重负担。尽管当前治疗手段包括生活方式干预、药物治疗和减重手术,但均存在明显局限:单纯节食与运动的一年复重率高达50%至三分之二,GLP-1受体激动剂虽风靡全球却伴随胰腺炎 、肠梗阻
、肠梗阻 、甲状腺癌
、甲状腺癌 等严重不良反应,减重手术虽效果显著却创伤大、费用高、并发症风险不容忽视。因此,寻找安全、有效、可长期口服的天然减肥药物成为医学界迫切需求。
等严重不良反应,减重手术虽效果显著却创伤大、费用高、并发症风险不容忽视。因此,寻找安全、有效、可长期口服的天然减肥药物成为医学界迫切需求。
传统中药五味子作为收涩固精、益气生津的经典药材,其木脂素成分Schisantherin A(Sin A)在保肝护肾、改善神经退行性疾病方面已有研究基础,但其在能量代谢调控中的作用长期未被揭示。
上海中医药大学丁丽丽教授、杨莉 教授联合美国希望之城国家医学中心黄文东教授团队,近期在《Nature Communications》发表的重磅研究,首次系统阐明了Sin A通过重塑肠道菌群结构、升高结合型胆汁酸水平、激活脂肪组织TGR5-p-CREB-STAT6信号轴、驱动M2型巨噬细胞极化并偶联交感神经促进产热的完整分子机制,为肥胖治疗提供了源自天然产物、靶点清晰、安全窗口优异的全新策略,也为中医药"健脾化湿、疏肝理气"理论在现代代谢疾病中的应用提供了坚实的科学注脚。
教授联合美国希望之城国家医学中心黄文东教授团队,近期在《Nature Communications》发表的重磅研究,首次系统阐明了Sin A通过重塑肠道菌群结构、升高结合型胆汁酸水平、激活脂肪组织TGR5-p-CREB-STAT6信号轴、驱动M2型巨噬细胞极化并偶联交感神经促进产热的完整分子机制,为肥胖治疗提供了源自天然产物、靶点清晰、安全窗口优异的全新策略,也为中医药"健脾化湿、疏肝理气"理论在现代代谢疾病中的应用提供了坚实的科学注脚。
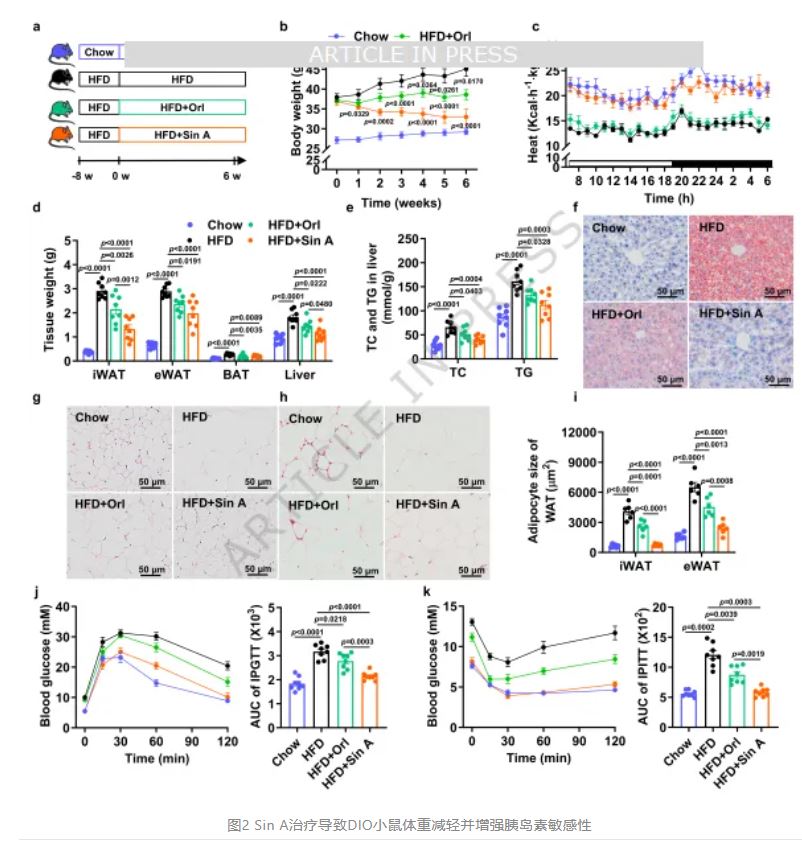
Sin A治疗导致DIO小鼠体重减轻并增强胰岛素 敏感性
敏感性
研究团队首先采用60%高脂饲料喂养8周建立饮食诱导肥胖(DIO)小鼠模型,以美国FDA批准的减肥药物奥利司他 作为阳性对照,系统评估Sin A的减肥效果。经过6周灌胃给药,Sin A 80 mg/kg剂量组小鼠体重较模型组下降26.8%,显著优于奥利司他组的14.3%减重幅度,且各组小鼠摄食量无显著差异,提示减重效应独立于热量摄入限制。代谢笼监测显示,Sin A治疗3周后小鼠24小时能量支出显著增加,体重匹配实验进一步证实这一增耗效应并非继发于体重下降,而是药物直接作用结果。组织解剖分析表明,Sin A显著降低腹股沟白色脂肪组织(iWAT)、附睾白色脂肪组织(eWAT)、棕色脂肪组织(BAT)及肝脏重量,肝脏甘油
作为阳性对照,系统评估Sin A的减肥效果。经过6周灌胃给药,Sin A 80 mg/kg剂量组小鼠体重较模型组下降26.8%,显著优于奥利司他组的14.3%减重幅度,且各组小鼠摄食量无显著差异,提示减重效应独立于热量摄入限制。代谢笼监测显示,Sin A治疗3周后小鼠24小时能量支出显著增加,体重匹配实验进一步证实这一增耗效应并非继发于体重下降,而是药物直接作用结果。组织解剖分析表明,Sin A显著降低腹股沟白色脂肪组织(iWAT)、附睾白色脂肪组织(eWAT)、棕色脂肪组织(BAT)及肝脏重量,肝脏甘油 三酯和总胆固醇水平下降约30%,血清总胆固醇、甘油三酯和低密度脂蛋白胆固醇降低而高密度脂蛋白胆固醇升高。
三酯和总胆固醇水平下降约30%,血清总胆固醇、甘油三酯和低密度脂蛋白胆固醇降低而高密度脂蛋白胆固醇升高。
形态学观察显示,Sin A明显减少肝脏和脂肪组织的脂质沉积,缩小脂肪细胞体积。糖代谢评估中,Sin A显著改善DIO小鼠的葡萄糖 耐量和胰岛素敏感性,糖耐量试验曲线下面积缩小32%,胰岛素耐量试验指数提高42%。值得注意的是,Sin A对正常饲料喂养小鼠的体重、代谢指标、肝肾功能标志物及主要脏器组织学均无不良影响,显示其优异的治疗窗和安全性特征。雌性DIO小鼠3周干预实验重现了上述代谢获益,证实效应无性别差异。剂量效应研究表明,即使20 mg/kg的较低剂量也能显著改善代谢参数,包括降低体重、增强糖耐量、减少肝脂和提高能量支出,且不影响食物摄入。这些结果共同确立Sin A为有效且安全的口服抗肥胖候选分子,其减重幅度和代谢综合改善效果超越现有临床药物。
耐量和胰岛素敏感性,糖耐量试验曲线下面积缩小32%,胰岛素耐量试验指数提高42%。值得注意的是,Sin A对正常饲料喂养小鼠的体重、代谢指标、肝肾功能标志物及主要脏器组织学均无不良影响,显示其优异的治疗窗和安全性特征。雌性DIO小鼠3周干预实验重现了上述代谢获益,证实效应无性别差异。剂量效应研究表明,即使20 mg/kg的较低剂量也能显著改善代谢参数,包括降低体重、增强糖耐量、减少肝脂和提高能量支出,且不影响食物摄入。这些结果共同确立Sin A为有效且安全的口服抗肥胖候选分子,其减重幅度和代谢综合改善效果超越现有临床药物。
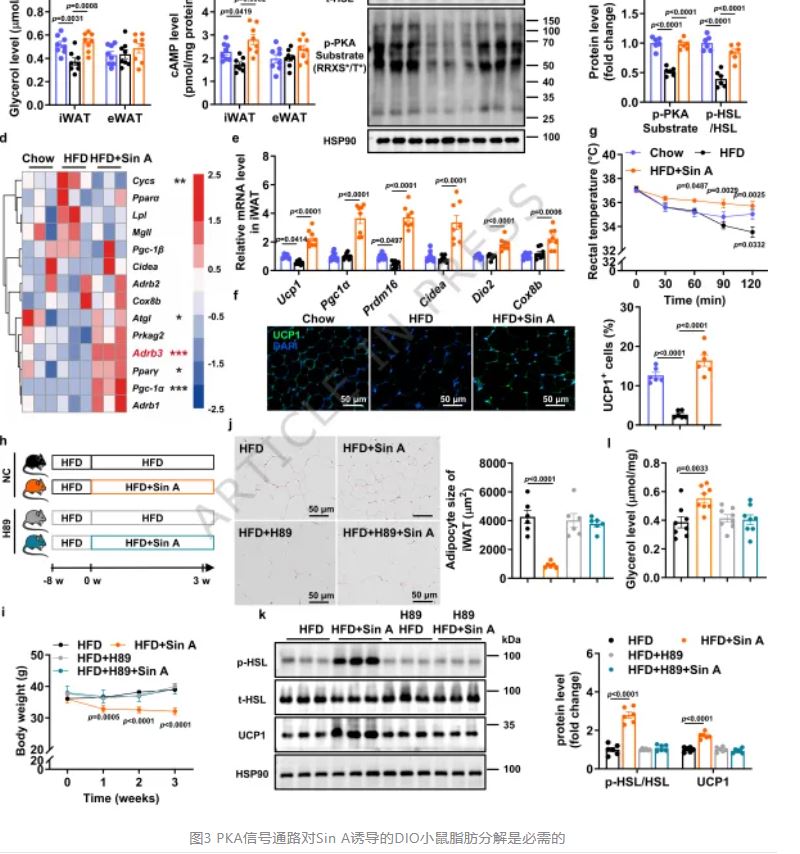
PKA信号通路对Sin A诱导的DIO小鼠脂肪分解是必需的
脂肪组织减少必然涉及脂解过程增强。研究团队检测发现,Sin A特异性升高iWAT中甘油释放水平和环磷酸腺苷 (cAMP)浓度,而对eWAT无显著影响,提示脂解作用具有组织选择性。Western blot分析显示,Sin A显著上调iWAT中磷酸化PKA底物和磷酸化激素敏感脂酶(p-HSL)表达,表明PKA信号通路被激活。为验证PKA在Sin A效应中的必要性,研究者联合使用PKA特异性抑制剂H89进行干预。结果显示,H89完全阻断Sin A诱导的体重下降、能量支出增加、肝脏和脂肪组织脂质减少,并抑制iWAT中UCP1、p-HSL及磷酸化PKA底物的上调,同时取消甘油释放增加效应。转录组测序进一步揭示,Sin A显著上调iWAT中β3-肾上腺素受体(Adrb3)及经典产热基因包括解偶联蛋白1(Ucp1)、过氧化物酶体增殖物激活受体γ辅激活因子1α(Pgc1α)、细胞色素c氧化酶亚基8B(Cox8b)和2型碘
(cAMP)浓度,而对eWAT无显著影响,提示脂解作用具有组织选择性。Western blot分析显示,Sin A显著上调iWAT中磷酸化PKA底物和磷酸化激素敏感脂酶(p-HSL)表达,表明PKA信号通路被激活。为验证PKA在Sin A效应中的必要性,研究者联合使用PKA特异性抑制剂H89进行干预。结果显示,H89完全阻断Sin A诱导的体重下降、能量支出增加、肝脏和脂肪组织脂质减少,并抑制iWAT中UCP1、p-HSL及磷酸化PKA底物的上调,同时取消甘油释放增加效应。转录组测序进一步揭示,Sin A显著上调iWAT中β3-肾上腺素受体(Adrb3)及经典产热基因包括解偶联蛋白1(Ucp1)、过氧化物酶体增殖物激活受体γ辅激活因子1α(Pgc1α)、细胞色素c氧化酶亚基8B(Cox8b)和2型碘 甲状腺原氨酸脱碘酶(Dio2)的表达,而H89处理可逆转这一转录特征。冷暴露实验显示,Sin A治疗小鼠在4℃环境中直肠温度下降更缓慢,产热能力显著增强,与UCP1介导的非颤抖产热增加一致。这些发现共同证明,PKA信号通路是Sin A启动脂肪分解、促进白色脂肪棕色化和增强适应性产热的关键分子开关,位于药物作用机制的核心环节。
甲状腺原氨酸脱碘酶(Dio2)的表达,而H89处理可逆转这一转录特征。冷暴露实验显示,Sin A治疗小鼠在4℃环境中直肠温度下降更缓慢,产热能力显著增强,与UCP1介导的非颤抖产热增加一致。这些发现共同证明,PKA信号通路是Sin A启动脂肪分解、促进白色脂肪棕色化和增强适应性产热的关键分子开关,位于药物作用机制的核心环节。
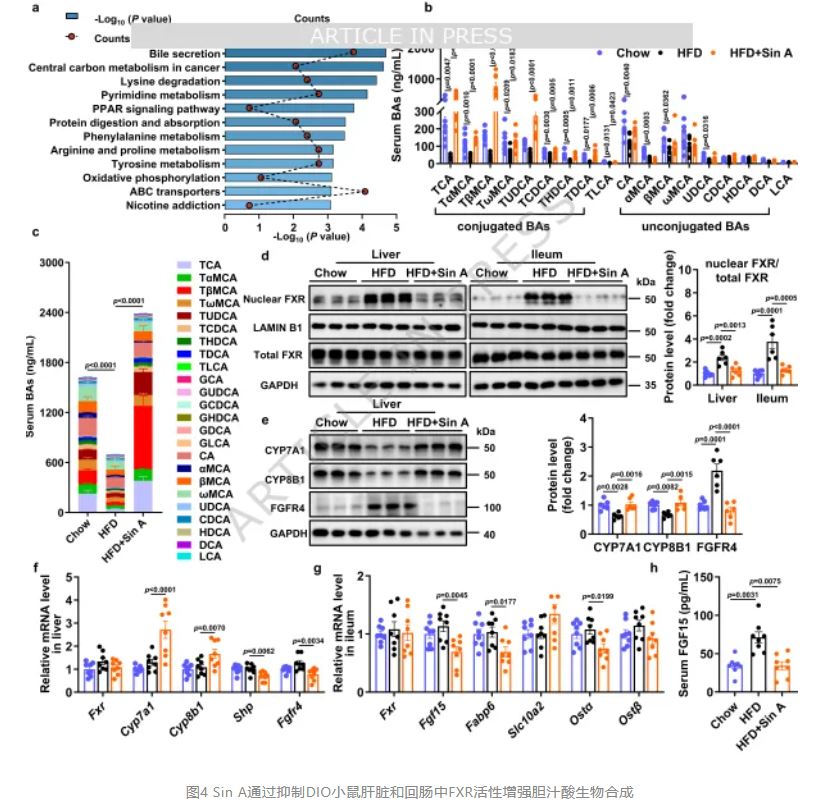
Sin A通过抑制DIO小鼠肝脏和回肠中FXR活性增强胆汁酸生物合成
胆汁酸传统上被视为脂质消化吸收的乳化剂,近年研究揭示其作为内分泌信号分子调控全身代谢的新功能。研究团队采用非靶向血清代谢组学分析发现,Sin A处理后胆汁酸分泌通路富集度最高;靶向定量代谢组学进一步鉴定出特异性升高的结合型胆汁酸(CBA)组分,包括牛磺-β-鼠胆酸 (TβMCA)、牛磺胆酸(TCA)和牛磺熊脱氧胆酸(TUDCA),血清浓度升高2至4倍,而粪便总胆汁酸水平下降,提示肠肝循环重分布。机制探索中,Western blot显示Sin A显著降低肝脏和回肠核内法尼醇X受体(FXR)蛋白水平,解除其对胆汁酸合成限速酶胆固醇7α-羟化酶(CYP7A1)和甾醇12α-羟化酶(CYP8B1)的转录抑制,两种酶mRNA和蛋白表达均显著上调。同时,FXR下游靶基因小异二聚体伴侣(Shp)转录下调,进一步证实FXR活性受抑。在回肠,FXR抑制伴随胆汁酸转运基因有机溶质转运体α(Osta)和肠胆汁酸结合蛋白(I-babp)表达降低,血清和回肠成纤维细胞生长因子15(FGF15)水平下降,肝脏FGF15受体FGFR4表达减少,从而解除对CYP7A1的负反馈抑制,形成胆汁酸合成增加的放大环路。这些结果共同阐明Sin A通过肝-肠双重抑制FXR转录活性,解除其对胆汁酸合成的刹车作用,导致具有代谢活性的CBA池扩增,为后续脂肪组织效应提供分子基础。
(TβMCA)、牛磺胆酸(TCA)和牛磺熊脱氧胆酸(TUDCA),血清浓度升高2至4倍,而粪便总胆汁酸水平下降,提示肠肝循环重分布。机制探索中,Western blot显示Sin A显著降低肝脏和回肠核内法尼醇X受体(FXR)蛋白水平,解除其对胆汁酸合成限速酶胆固醇7α-羟化酶(CYP7A1)和甾醇12α-羟化酶(CYP8B1)的转录抑制,两种酶mRNA和蛋白表达均显著上调。同时,FXR下游靶基因小异二聚体伴侣(Shp)转录下调,进一步证实FXR活性受抑。在回肠,FXR抑制伴随胆汁酸转运基因有机溶质转运体α(Osta)和肠胆汁酸结合蛋白(I-babp)表达降低,血清和回肠成纤维细胞生长因子15(FGF15)水平下降,肝脏FGF15受体FGFR4表达减少,从而解除对CYP7A1的负反馈抑制,形成胆汁酸合成增加的放大环路。这些结果共同阐明Sin A通过肝-肠双重抑制FXR转录活性,解除其对胆汁酸合成的刹车作用,导致具有代谢活性的CBA池扩增,为后续脂肪组织效应提供分子基础。
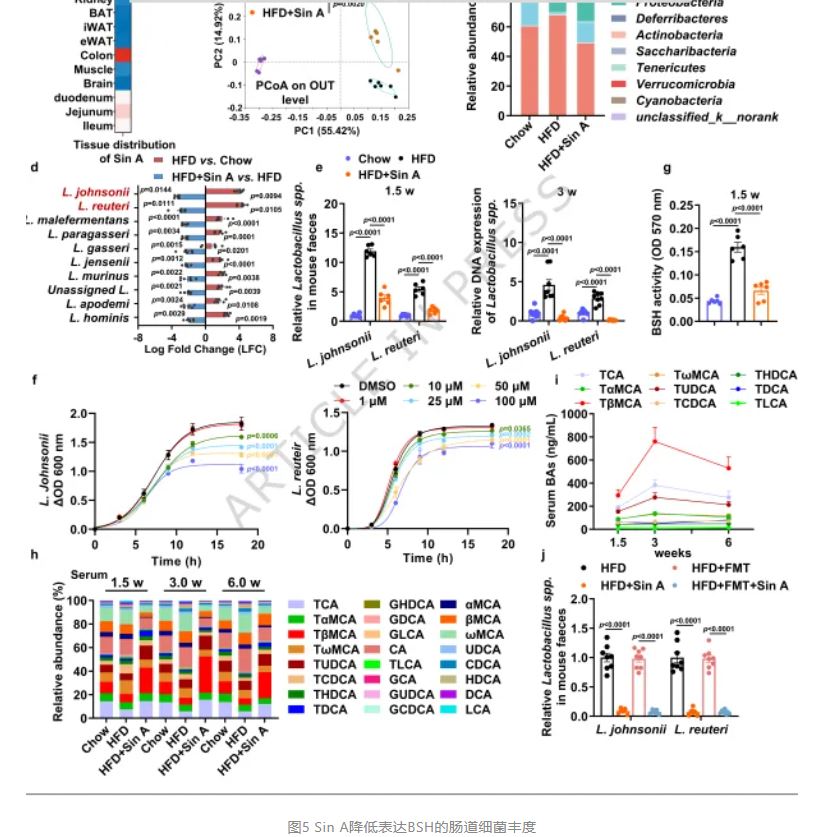
Sin A降低表达BSH的肠道细菌丰度
结合型胆汁酸的解离由肠道菌群编码的胆汁盐水解酶(BSH)催化,是决定CBA生物利用度的关键步骤。16S rRNA测序显示,Sin A不改变肠道菌群整体α多样性指数,但主坐标分析(PCoA)揭示处理组与对照组微生物群落结构显著分离。ANCOM-BC2差异丰度分析锁定厚壁菌门中乳杆菌属 (Lactobacillus)为显著降低的核心类群;宏基因组测序进一步在种水平鉴定出5种被Sin A选择性抑制的BSH高产菌:约氏乳杆菌(L. johnsonii)、罗伊氏乳杆菌(L. reuteri)、鼠乳杆菌(L. murinus)、詹氏乳杆菌(L. jensenii)和格氏乳杆菌(L. gasseri),其中前两种的log倍数变化最大。
(Lactobacillus)为显著降低的核心类群;宏基因组测序进一步在种水平鉴定出5种被Sin A选择性抑制的BSH高产菌:约氏乳杆菌(L. johnsonii)、罗伊氏乳杆菌(L. reuteri)、鼠乳杆菌(L. murinus)、詹氏乳杆菌(L. jensenii)和格氏乳杆菌(L. gasseri),其中前两种的log倍数变化最大。
体外培养实验证实,Sin A在1至100 μM范围内剂量依赖性抑制L. johnsonii和L. reuteri生长,而对代谢有益的非BSH菌嗜黏蛋白阿克曼菌(Akkermansia muciniphila)无显著影响。粪悬液共培养实验和BSH酶活性测定显示,Sin A处理1.5周和3周后粪便BSH活性显著下降60%,与血清TβMCA水平升高呈负相关,且CBA升高早在1.5周即出现并持续至6周干预结束。为严格验证肠道菌群的必要性,研究者采用抗生素清除联合粪菌移植 (FMT)策略:广谱抗生素(氨苄西林
(FMT)策略:广谱抗生素(氨苄西林 、甲硝唑
、甲硝唑 、新霉素
、新霉素 、万古霉素
、万古霉素 )预处理完全消除Sin A的减重、改善糖代谢、增加能量支出和诱导UCP1等所有效应;将Sin A处理小鼠的粪菌移植给抗生素清除后的受体小鼠,3周内即可"复制"出供体的减重、降脂、提高能量支出和改善胰岛素敏感性等全部表型,且伴随L. johnsonii和L. reuteri丰度降低及BSH活性下降。这些结果共同证明,Sin A通过选择性抑制BSH高产肠道细菌、保护CBA不被解离而发挥代谢益处,肠道菌群是药物作用的必需环节和关键靶点。
)预处理完全消除Sin A的减重、改善糖代谢、增加能量支出和诱导UCP1等所有效应;将Sin A处理小鼠的粪菌移植给抗生素清除后的受体小鼠,3周内即可"复制"出供体的减重、降脂、提高能量支出和改善胰岛素敏感性等全部表型,且伴随L. johnsonii和L. reuteri丰度降低及BSH活性下降。这些结果共同证明,Sin A通过选择性抑制BSH高产肠道细菌、保护CBA不被解离而发挥代谢益处,肠道菌群是药物作用的必需环节和关键靶点。
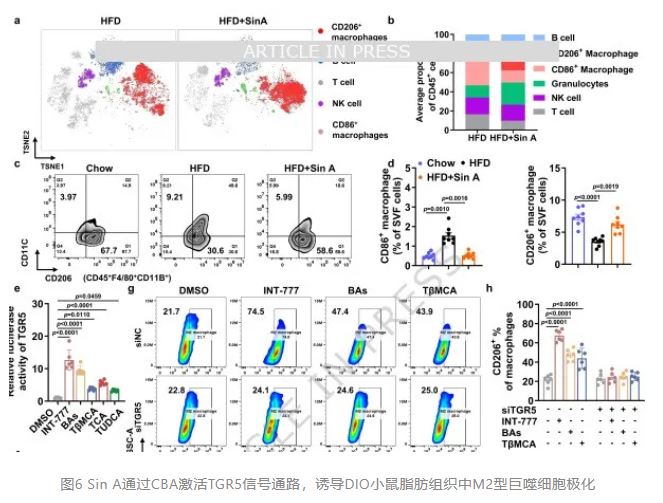
Sin A通过CBA激活TGR5信号通路,诱导DIO小鼠脂肪组织中M2型巨噬细胞极化
CBA如何远程 调控脂肪组织代谢?研究团队聚焦已知胆汁酸受体Takeda G蛋白偶联受体5(TGR5)。质谱流式细胞术(CyTOF)和常规流式细胞术一致显示,Sin A显著增加iWAT基质血管组分(SVF)中M2样巨噬细胞(CD45+F4/80+CD11b+CD206+)比例,而M1样巨噬细胞、B细胞、T细胞相应减少,NK细胞和粒细胞无显著变化。定量PCR验证M2标志基因甘露糖受体C型1(Mrc1)、C型凝集素结构域家族10成员A(Clec10a)、精氨酸酶1(Arg1)和信号转导及转录激活因子6(Stat6)同步上调。
调控脂肪组织代谢?研究团队聚焦已知胆汁酸受体Takeda G蛋白偶联受体5(TGR5)。质谱流式细胞术(CyTOF)和常规流式细胞术一致显示,Sin A显著增加iWAT基质血管组分(SVF)中M2样巨噬细胞(CD45+F4/80+CD11b+CD206+)比例,而M1样巨噬细胞、B细胞、T细胞相应减少,NK细胞和粒细胞无显著变化。定量PCR验证M2标志基因甘露糖受体C型1(Mrc1)、C型凝集素结构域家族10成员A(Clec10a)、精氨酸酶1(Arg1)和信号转导及转录激活因子6(Stat6)同步上调。
体外功能实验中,TβMCA、CBA混合物或TGR5特异性激动剂INT-777均可直接提高THP-1巨噬细胞CD206阳性率和M2标志基因表达,而TGR5敲低(TGR5-KD)THP-1细胞或Tgr5-/-小鼠原代SVF细胞完全丧失该反应,证实CBA-TGR5偶联是M2极化的直接驱动机制。Seahorse细胞能量代谢分析显示,TβMCA处理使M2巨噬细胞基础氧耗率和储备呼吸能力提高40%,脂肪酸氧化(FAO)增强;同时CD36、肉碱棕榈酰转移酶1b(Cpt1b)、过氧化物酶体增殖物激活受体γ辅激活因子1α(Pgcla)等脂代谢基因上调,提示M2细胞脂肪酸摄取和氧化能力增强,为后续产热提供能量底物。这些发现共同揭示Sin A通过菌群依赖的CBA升高,激活脂肪组织TGR5信号,驱动巨噬细胞向M2表型极化,建立免疫-代谢偶联的新范式。
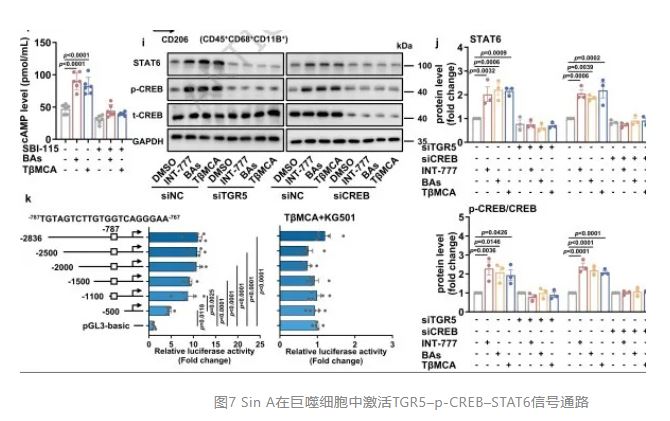
Sin A在巨噬细胞中激活TGR5–p-CREB–STAT6信号通路
TGR5作为Gs蛋白偶联受体,激活腺苷酸环化酶-cAMP-蛋白激酶A(PKA)级联,促使cAMP反应元件结合蛋白(CREB)磷酸化。Western blot显示,Sin A处理小鼠iWAT-SVF中磷酸化PKA底物、磷酸化CREB(p-CREB)和STAT6蛋白显著上调。在THP-1细胞中,INT-777、TβMCA或CBA混合物均可提高p-CREB和STAT6水平,而TGR5-KD完全阻断这一效应;CREB敲低(CREB-KD)同样抑制STAT6蛋白诱导,提示"TGR5→CREB→STAT6"级联通路。启动子区分析构建一系列STAT6启动子缺失突变体(-3000至+100 bp),荧光素酶报告基因实验显示TβMCA或CREB激动剂Forskolin可激活全长启动子,而-1100至-500 bp片段缺失使激活效应降低50%,CREB抑制剂KG-501完全取消TβMCA依赖性激活。生物信息学预测结合电泳迁移率变动分析(EMSA)证实,-780至-761 bp处存在典型cAMP反应元件(CRE),序列为GTAGTCTTGTGGTCAGGGAA,重组人CREB蛋白可直接结合该位点,突变探针或竞争性冷探针可抑制结合,抗CREB抗体产生超迁移条带。这些结果共同阐明CBA通过TGR5-cAMP-PKA使CREB磷酸化,磷酸化CREB直接结合STAT6启动子CRE位点,完成从代谢信号到免疫转录的分子嫁接,是Sin A诱导M2极化的核心转录机制。
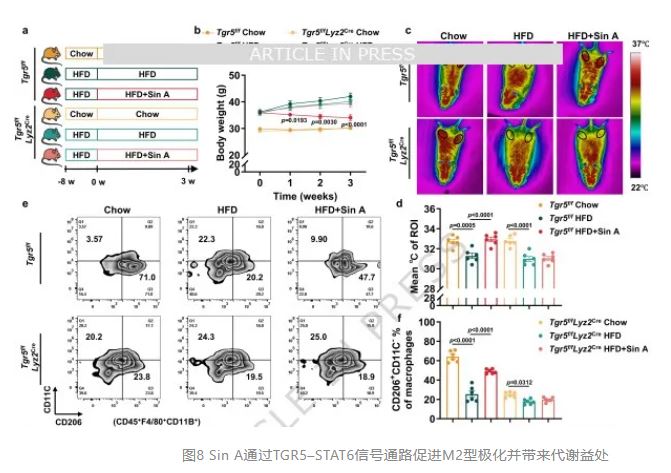
Sin A通过TGR5–STAT6信号通路促进M2型极化并带来代谢益处
为验证TGR5-STAT6轴心在整体代谢中的必要性,研究者采用骨髓细胞特异性Tgr5敲除(Tgr5fl/flLyz2Cre)DIO小鼠模型。Sin A在Tgr5fl/fl对照小鼠中显著降低体重、血清甘油三酯和总胆固醇、减少肝脏和脂肪组织脂质沉积、提高能量支出和iWAT局部温度,并增加M2巨噬细胞比例;而在Tgr5fl/flLyz2Cre小鼠中,上述所有代谢获益完全消失,UCP1表达、脂解指标和产热能力均无改善。流式细胞术证实Sin A无法增加骨髓TGR5缺失小鼠脂肪组织中的M2巨噬细胞。同理,STAT6整体敲除(Stat6-/-)DIO小鼠也完全抵抗Sin A的减重、改善血脂、增强能量代谢和提高胰岛素敏感性等效应,M2极化和产热表型同样缺失。这些遗传学证据共同证明,Sin A依赖骨髓细胞固有的TGR5-STAT6信号通路完成M2巨噬细胞极化,并由此介导全身的代谢改善,确立该轴心为天然产物干预肥胖的"非冗余"分子靶点,无法被其他代偿机制所替代。
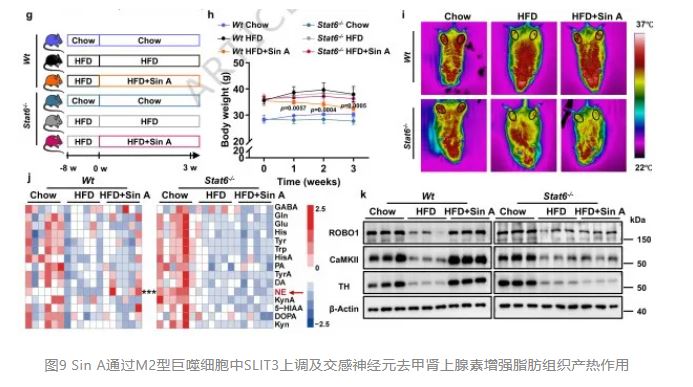
Sin A通过M2型巨噬细胞中SLIT3上调及交感神经元去甲肾上腺素 增强脂肪组织产热作用
增强脂肪组织产热作用
M2巨噬细胞如何与脂肪细胞对话以执行产热指令?研究团队聚焦SLIT3-ROBO1轴这一新近发现的神经-免疫通讯通路。既往报道脂肪驻留M2细胞分泌SLIT3蛋白,通过结合交感神经元表面 roundabout guidance receptor 1(ROBO1)受体,激活钙/钙调蛋白依赖性蛋白激酶II(CaMKII)信号,促进酪氨酸羟化酶(TH)表达和去甲肾上腺素(NE)合成释放,NE进而激动脂肪细胞β3-肾上腺素受体(ADRB3),启动cAMP-PKA-UCP1产热级联。实验显示,Sin A显著升高iWAT中SLIT3蛋白水平和NE含量,同步增加TH、ROBO1和CaMKII表达;Stat6敲除完全阻断这一系列变化,iWAT局部温度不再升高。为严格验证SLIT3和ROBO1的因果作用,研究者利用重组腺相关病毒血清型2/8(rAAV2/8)介导的shRNA,分别在iWAT局部敲低Slit3或Robo1基因。结果显示,两种敲低均完全废除Sin A的减重、降脂、提高能量支出、升高局部温度及诱导UCP1和磷酸化HSL的能力,而 scramble 对照病毒组效应完好;同时,TH和CaMKII的诱导也被阻断。这些结果共同证明,SLIT3-ROBO1是Sin A效应的下游必需效应器,位于TGR5-STAT6-M2轴与交感神经-脂肪产热偶联的关键节点。
结语
研究完整绘制了Sin A的作用机制图谱:口服后选择性抑制肠道BSH菌→保护CBA不被解离→CBA吸收入血激活脂肪组织TGR5→cAMP-PKA-CREB磷酸化→CREB结合并激活STAT6转录→STAT6驱动M2巨噬细胞极化→M2细胞分泌SLIT3→SLIT3激活ROBO1-CaMKII-TH→交感神经释放NE→NE激动ADRB3-cAMP-PKA-UCP1→白色脂肪棕色化和产热。中医“脾主运化、肝主疏泄”理论在现代语境下可解读为“肝-肠-菌-免疫-神经”多脏器协同,Sin A正扮演“疏肝理脾、调菌助运”的现代分子使者。这一"菌群-CBA-免疫-神经-脂肪"的多脏器、多细胞类型协同网络,为理解中药多靶点、整体调节特点提供了现代分子诠释,也为开发新一代减肥药物提供了可验证、可干预的精准靶点群。
参考文献:
Wang X, Wang X, Yu S, Huang L, Xue Q, Yang X, Wang Z, Lin W, Jiang Y, Xu Y, Liao Q, Jin L, Wang Z, Tao F, Yang L, Huang W, Ding L. Schisantherin A interacts with gut bacteria to stimulate adipose tissue thermogenesis in obese mice via a TGR5‒p-CREB‒STAT6 signaling pathway. Nat Commun. 2025 Dec 11. doi: 10.1038/s41467-025-67172-y. Epub ahead of print. PMID: 41381461.
来源|梅斯循证中医药
