
双重作用,应对极高骨折风险:从 Wnt 通路到靶向硬骨抑素的治疗新策略
问题一:在骨代谢调控中,Wnt 信号通路被认为是一条重要通路。能否请您从机制角度,介绍一下 Wnt 通路对骨的调节作用?
娄楠 教授:
Wnt 信号通路是调控骨代谢的重要通路。一方面,Wnt 蛋白的激活可以启动下游成骨相关基因的转录,从而促进骨形成;另一方面,Wnt 通路的激活还可上调骨保护素(OPG)的表达。OPG 通过与 RANKL 竞争性结合,阻断其与 RANK 的相互作用,进而抑制破骨细胞的分化与成熟,发挥抑制骨吸收的作用。因此,Wnt 通路在生理状态下同时参与「促成骨、抑吸收」的双重调控作用。在这一调控体系中,硬骨抑素是 Wnt 信号通路中关键的内源性抑制因子之一 [2]。
问题二:相较于传统骨质疏松治疗药物多以单一方向进行干预,靶向硬骨抑素的治疗在机制上呈现出同时促进骨形成并抑制骨吸收的特点。您能否从机制角度,解读这一「双重作用」是如何实现的?
娄楠 教授:
硬骨抑素主要由骨细胞分泌,是 Wnt 信号通路中关键的内源性抑制因子之一。当靶向硬骨抑素进行干预后,这种抑制作用被解除,Wnt 信号通路得以重新激活。一方面,成骨细胞功能增强,骨形成水平明显提升;另一方面,随着 OPG 表达上调,RANKL 介导的破骨细胞活性受到抑制,从而实现对骨吸收的同步抑制。这也从机制层面解释了,靶向硬骨抑素治疗为何能够在同一信号通路框架下,同时作用于成骨和破骨两个方向 [4-5]。
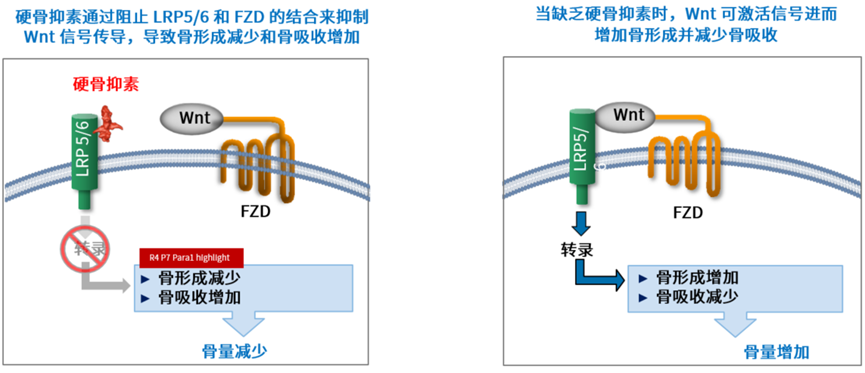
注:FZD = 卷曲蛋白受体;LRP = 低密度脂蛋白受体相关蛋白
图 1 硬骨抑素通过 Wnt 信号通路影响骨形成和骨吸收 [6-10]
进一步来看,靶向硬骨抑素治疗通过激活 Wnt 信号通路,能够在松质骨表面及皮质骨内层上启动基于骨塑建的骨形成过程。而传统抗骨质疏松药物主要作用于骨重建过程,即骨吸收陷窝内由破骨细胞-成骨细胞偶联完成的骨转换 [11,12]。
问题三:目前,在「港澳药械通」政策背景下,靶向硬骨抑素治疗已在大湾区率先应用于临床。基于您的临床实践,您如何评价该「双重作用」在极高骨折风险(VHFR)骨质疏松患者治疗中的临床价值?
娄楠 教授:
在大湾区「港澳药械通」政策支持下,有机会在真实世界中较早接触并应用具有「双重作用」的硬骨抑素单克隆抗体 —— 罗莫索珠单抗。从临床实践来看,这一治疗策略在极高骨折风险骨质疏松患者中逐渐体现出其独特的临床价值。接下来,娄教授结合了两例临床中较为典型的病例与大家分享。
第一个病例是一名 78 岁的绝经后女性患者,因肱骨近端的骨折接受了手术治疗。通过手术治疗的过程中以及术前检查,我们发现这是一个重度骨松患者,且从未接受过系统的抗骨质疏松药物治疗。对患者进行了一个风险模型(FRAX)的建立以及详细的评估。骨密度方面,DXA 检测显示:腰椎 T 值为 −3.6,全髋 T 值为 −2.7,股骨颈 T 值为 −3.2;骨转换标志物方面,检测显示 P1NP 为 124.6,β-CTX 为 431.9,提示骨转换整体处于较为活跃状态,且骨吸收明显增强。
在制订治疗方案时,娄教授重点考虑到该患者属于初治且极高骨折风险人群,已经出现了不止一次的骨折。国内外指南均指出,对于此类绝经后女性患者,具有促骨形成作用的药物可作为初始治疗选择 [1,13,14]。进一步分析发现,该患者虽然存在一定程度的成骨升高,但不足以抵消显著增强的骨吸收,整体骨量仍呈持续丢失状态。在这种背景下,如果仅单向促进成骨、而不能同步抑制骨吸收,整体骨量的改善可能仍然受限。
因此,在补充钙剂和维生素 D 的基础上,为患者选择了罗莫索珠单抗治疗。治疗过程中患者整体耐受性良好,未观察到不良反应。随访显示,治疗 6 个月后,腰椎骨密度 T 值由 −3.6 提升至 −2.7,髋部骨密度 T 值由 −2.7 提升至 −2.6,分别改善约 25% 和 3%。这里可以看到患者腰椎骨密度改善最为明显。
第二个病例是一名 84 岁的绝经后女性患者。既往曾接受阿仑膦酸钠治疗约 1 年,整体依从性尚可,但随访过程中发现骨密度改善有限。DXA 检测显示:腰椎 T 值 −3.3,全髋 T 值 −2.4,股骨颈 T 值 −3.3,仍处于极高骨折风险状态,提示骨吸收仍占主导,骨重建平衡尚未恢复。
娄教授指出,在这种情况下,需要更为快速、强效的干预策略,仅依赖单一抗骨吸收治疗往往难以取得理想的治疗效果。因此,将治疗方案由单纯抗骨吸收调整为罗莫索珠单抗治疗。治疗期间患者耐受性良好,随访过程中未观察到不良反应。
随访显示,治疗 6 个月后,患者腰椎骨密度 T 值由 −3.3 提升至 −2.6,改善约 21%;同时,还观察到患者的骨痛症状及乏力情况逐步缓解,整体生活质量得到明显改善。
综合这两例病例娄教授总结到,对于极高骨折风险骨质疏松重度患者而言,尽早实施快速而强效的干预至关重要。以罗莫索珠单抗为代表的、具有「双重作用」的治疗策略,凭借其在同一机制框架下同步促进骨形成并抑制骨吸收的特点,为这类极高骨折风险的绝经后妇女的早期强化干预提供了新的临床选择。
专家简介
娄楠 教授
香港大学深圳医院 骨科医学中心
副顾问医生,主任医师,硕士研究生导师
香港大学李嘉诚医学院荣誉助理教授
CAOS-AAHKS Oversea 访问学者
特种外科医院 HSS-China 临床访问学者
新加坡中央医院 SGH 临床访问学者
广东省医学会关节外科学分会青年委员会委员
广东省医师协会关节外科医师分会委员
深圳市医师协会骨科分会第三界理事
深圳市医学会关节外科专业委员会委员
深圳市医学会关节外科专业委员会青年委员会副主任委员
深圳市健康管理协会骨质疏松和骨矿盐疾病专业委员会副主任委员
主持和参与国家自然科学基金、广东省医学科学研究基金、深圳市科技重大专项、深圳科创委重点研究项目、面上项目、深医专项 SMART 等各级科研基金多项,发表 SCI 论文 20 余篇
参考文献
审批编号:SC-CHN-AMG785-00126
有效期至:2028-03-25 材料过期,视同作废
仅供医疗卫生专业人士查看,且不作为临床指导
病例内容来自专家个人临床经验,仅代表专家个人观点
本材料由安进制作


