
双剑合璧,SHR-A2009联合阿美替尼释放强效协同潜力 | 2026 ELCC
前言
2026年欧洲肺癌大会(ELCC 2026)于3月25日至28日在丹麦哥本哈根顺利召开,汇聚全球肺癌领域顶尖学者,共话临床研究新进展、共探治疗新方向。本次大会中,广东省人民医院吴一龙 教授公布了新型HER3靶向抗体偶联药物(ADC)SHR-A2009联合阿美替尼
教授公布了新型HER3靶向抗体偶联药物(ADC)SHR-A2009联合阿美替尼 ,在一线和二线及以上治疗EGFR突变非小细胞肺癌
,在一线和二线及以上治疗EGFR突变非小细胞肺癌 (NSCLC)中的安全性与初步疗效数据,为后续关键研究奠定了重要基础。
(NSCLC)中的安全性与初步疗效数据,为后续关键研究奠定了重要基础。

研究背景
SHR-A2009为新型HER3靶向ADC,由抗HER3 IgG1单克隆抗体、可切割肽连接子及DNA拓扑异构酶I抑制剂偶联而成。其I期临床研究显示,SHR-A2009在经治EGFR突变NSCLC中已展现出初步抗肿瘤活性与可控的安全性。本研究为一项多部分Ib/II期临床试验,旨在探索SHR-A2009联合方案在EGFR突变NSCLC中的治疗价值,现报告其联合第三代EGFR-TKI阿美替尼用于二线及以上(PA1)与一线(PA2)治疗的Ib期研究结果。
研究方法
SHR-A2009(每3周1次,静脉输注)与阿美替尼(每日1次,口服)以3周为 1个治疗周期给药。PA1队列中,患者在剂量递减队列中持续接受SHR-A2009(9、8或6 mg/kg)联合阿美替尼(110或55 mg)治疗。PA2队列中,患者按1:1比例随机分配至两组,一组接受SHR-A2009 6 mg/kg联合阿美替尼110 mg持续治疗(R1组),另一组接受该联合方案治疗4~8个周期后,序贯阿美替尼单药治疗(R2组)。本研究主要目的为评估该联合方案的耐受性与安全性,并确定II期推荐剂量(RP2D)。
1个治疗周期给药。PA1队列中,患者在剂量递减队列中持续接受SHR-A2009(9、8或6 mg/kg)联合阿美替尼(110或55 mg)治疗。PA2队列中,患者按1:1比例随机分配至两组,一组接受SHR-A2009 6 mg/kg联合阿美替尼110 mg持续治疗(R1组),另一组接受该联合方案治疗4~8个周期后,序贯阿美替尼单药治疗(R2组)。本研究主要目的为评估该联合方案的耐受性与安全性,并确定II期推荐剂量(RP2D)。
研究结果
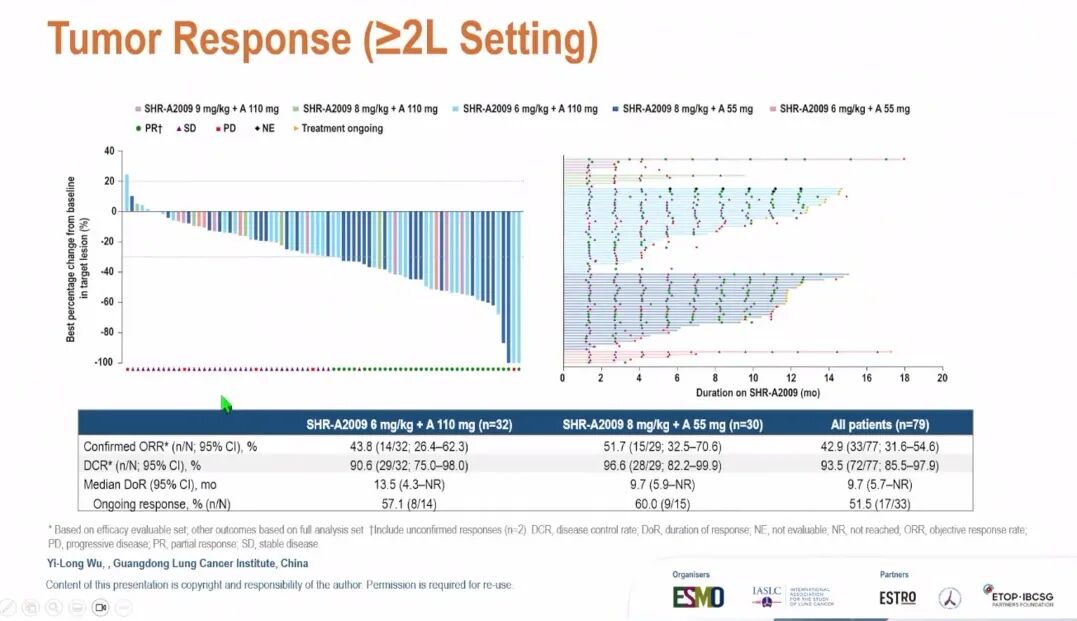
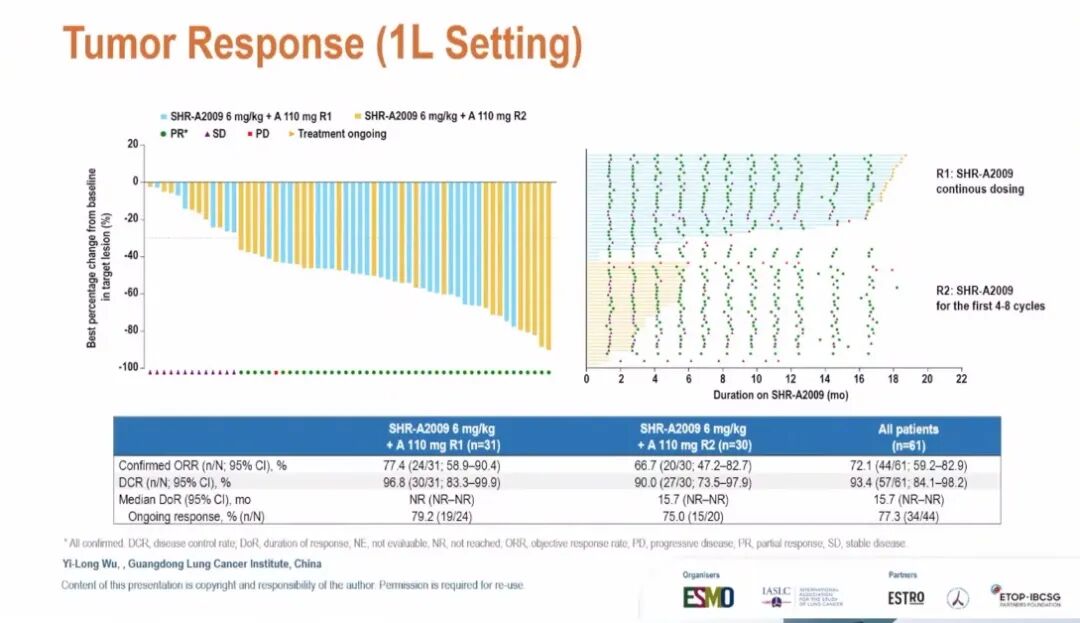
PA1队列共纳入79例患者,其中东部肿瘤协作组(ECOG)体能状态评分为1分者占97.5%,IV期患者占97.5%,接受二线及以上既往治疗者占53.2%,既往经第三代EGFR-TKI治疗者占83.5%,接受过化疗者占48.1%。PA2队列共61例患者接受R1/R2方案治疗,ECOG 1分者占96.7%,IV期患者占98.4%,EGFR 19号外显子缺失占59.0%,L858R突变占41.0%。
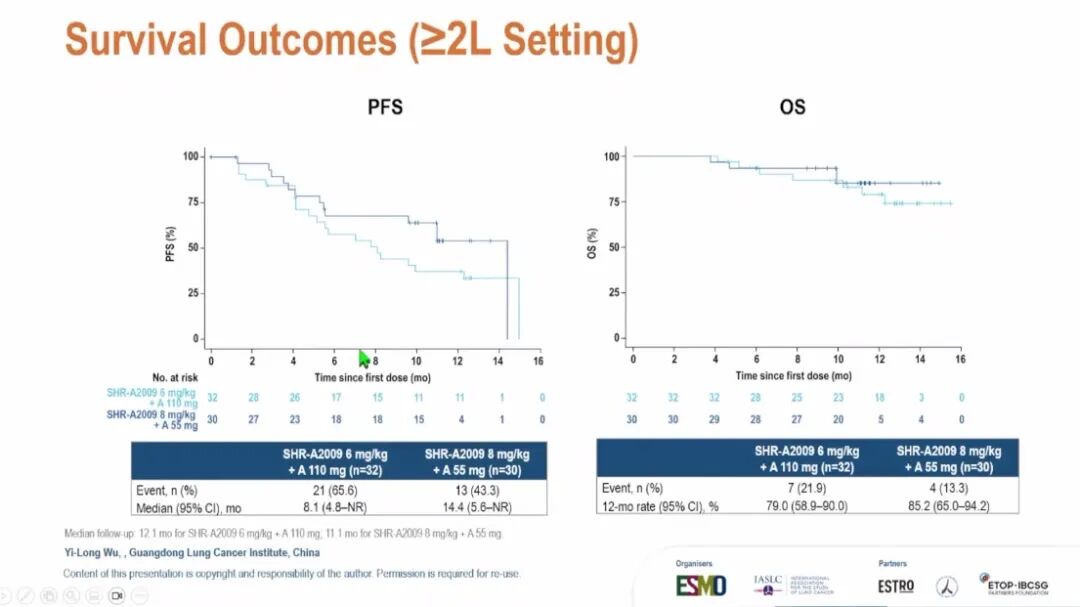
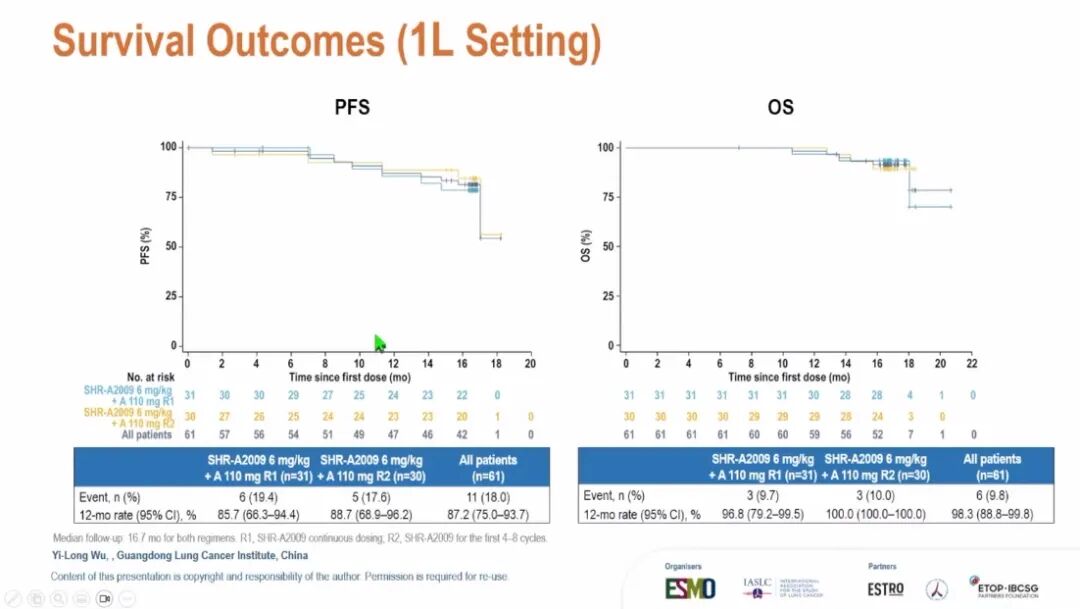
截至数据截止日期(2025年11月20日),PA1队列中位随访11.3个月,PA2队列中位随访16.7个月。安全性方面,PA1与PA2队列≥3级治疗相关不良事件(TRAE)发生率分别为59.5%、31.3%。因TRAE停用SHR-A2009的比例分别为7.6%、13.1%,停用阿美替尼的比例分别为7.6%、4.9%。PA1队列间质性肺病 (ILD)发生率为7.6%(≥3级占3.8%),PA2队列为4.9%(≥3级占1.6%)。PA2队列发生1例治疗相关死亡(原因未明确)。PA1与PA2队列疗效数据详见下图。
(ILD)发生率为7.6%(≥3级占3.8%),PA2队列为4.9%(≥3级占1.6%)。PA2队列发生1例治疗相关死亡(原因未明确)。PA1与PA2队列疗效数据详见下图。
研究结论
SHR-A2009联合阿美替尼方案在一线和二线及以上EGFR突变NSCLC治疗中,均展现出可控的安全性与优异的抗肿瘤活性。SHR-A2009 6 mg/kg联合阿美替尼110 mg持续给药方案已确定作为一线关键研究的评估剂量,后线治疗剂量仍在进一步探索中。目前一项III期临床试验(NCT07183189)正在开展,旨在比较该联合方案与阿美替尼单药一线治疗EGFR突变NSCLC的疗效差异。
参考文献:
[1] Yilong Wu, et al. SHR-A2009, a HER3-targeted ADC, plus aumolertinib (A) as 1L or >2L treatment for EGFR-mutated (EGFRm) NSCLC: A phase lb/ll study. 2026 ELCC Abstract 10MO.
撰写:Kenken
审核:Faline
排版:Kenken
执行:Ocean
 ,助力中国临床决策”是平台的使命。医脉通旗下拥有「临床指南」「用药参考」「医学文献王」「医知源」「e研通」「e脉播」等系列产品,全面满足医学工作者临床决策、获取新知及提升科研效率等方面的需求。
,助力中国临床决策”是平台的使命。医脉通旗下拥有「临床指南」「用药参考」「医学文献王」「医知源」「e研通」「e脉播」等系列产品,全面满足医学工作者临床决策、获取新知及提升科研效率等方面的需求。