
临床研究 | 韩英/罗洁:抗 gp210 抗体与 ACA 双阳性对原发性胆汁性胆管炎患者临床预后的影响:风险分析及应答标准的建立
来源:中华肝脏病杂志
引 用 本 文
罗洁, 丁大伟,郭冠亚 , 苏树豪, 杨彩云, 贾桂, 孙瑞青, 邓娟, 郑林华, 罗贯虹, 尹芳, 刘雁声,崔丽
, 苏树豪, 杨彩云, 贾桂, 孙瑞青, 邓娟, 郑林华, 罗贯虹, 尹芳, 刘雁声,崔丽 娜, 郭长存,周新民
娜, 郭长存,周新民 , 尚玉龙,韩英
, 尚玉龙,韩英 . 抗 gp210 抗体与 ACA 双阳性对原发性胆汁性胆管炎
. 抗 gp210 抗体与 ACA 双阳性对原发性胆汁性胆管炎 患者临床预后的影响:风险分析及应答标准的建立[J]. 中华肝脏病杂志, 2026, 34(3):224-231.DOI:10.3760/cma.j.cn501113-20250616-00242.
患者临床预后的影响:风险分析及应答标准的建立[J]. 中华肝脏病杂志, 2026, 34(3):224-231.DOI:10.3760/cma.j.cn501113-20250616-00242.
通信作者:韩英,空军军医大学第一附属医院消化内科
专 家 简 介
韩 英 教授
空军军医大学西京医院(空军军医大学第一附属医院)消化内科主任医师、教授、博导
军队专业技术少将
长江学者特聘教授 享受国务院特帖
军队科技创新领军人才
中华医学会内科学分会第十四届主任委员
中华医学会肝病学分会副主任委员
中华肝脏病学分会自免肝学组组长
获省部级科技成果奖一等奖三项
获吴杨
 奖、吴阶平医药创新奖
奖、吴阶平医药创新奖承担国家自然科学基金-国际合作项目、十三五重点研发计划、重大新药创制专项等多项重大科研课题。在STTT、Hepatology、CGH 、AJG等肝病和免疫性疾病权威杂志发表SCI论著90余篇
正文
原发性胆汁性胆管炎(primary biliary cholangitis,PBC)是一种以肝内小胆管进行性破坏为特征的慢性胆汁淤积 性疾病,好发于中老年女性,可进展至肝硬化 、肝衰竭
性疾病,好发于中老年女性,可进展至肝硬化 、肝衰竭 甚至死亡。熊去氧胆酸(ursodeoxycholic acid,UDCA)是目前唯一的一线治疗药物,但约 30%~40% 的 PBC 患者对 UDCA应答不佳[1-4]。抗糖蛋白 210(anti-glycoprotein 210,抗-gp210)抗体是 PBC 的特异性抗核抗体,不仅可以作为诊断性抗体[5-6],还与 PBC 患者的疾病严重程度及其预后相关,是 PBC 患者出现死亡和肝移植的独立预测因素[7-11]。近年来也有研究探讨了抗着丝粒抗体(anti-centromere antibody,ACA)与 PBC 患者预后的关系,发现 ACA 阳性的 PBC 患者出现门静脉高压
甚至死亡。熊去氧胆酸(ursodeoxycholic acid,UDCA)是目前唯一的一线治疗药物,但约 30%~40% 的 PBC 患者对 UDCA应答不佳[1-4]。抗糖蛋白 210(anti-glycoprotein 210,抗-gp210)抗体是 PBC 的特异性抗核抗体,不仅可以作为诊断性抗体[5-6],还与 PBC 患者的疾病严重程度及其预后相关,是 PBC 患者出现死亡和肝移植的独立预测因素[7-11]。近年来也有研究探讨了抗着丝粒抗体(anti-centromere antibody,ACA)与 PBC 患者预后的关系,发现 ACA 阳性的 PBC 患者出现门静脉高压 的风险较高[12]。并且有报道,抗gp210 抗体联合 ACA 阳性的 PBC 患者预后较差,是 PBC 患者出现肝移植或死亡的独立预后标志物,可以用于优化 GLOBE 评分对患者进行风险分层[13]。本文旨在通过大样本回顾性队列研究,分析抗 gp210 抗体 和 ACA 双阳性 PBC 患者的预后情况,探索适合双阳性患者的生物化学应答标准,为 PBC 患者的风险分层和治疗策略提供新依据。
的风险较高[12]。并且有报道,抗gp210 抗体联合 ACA 阳性的 PBC 患者预后较差,是 PBC 患者出现肝移植或死亡的独立预后标志物,可以用于优化 GLOBE 评分对患者进行风险分层[13]。本文旨在通过大样本回顾性队列研究,分析抗 gp210 抗体 和 ACA 双阳性 PBC 患者的预后情况,探索适合双阳性患者的生物化学应答标准,为 PBC 患者的风险分层和治疗策略提供新依据。
资料与方法
1. 研究对象:本研究为回顾性队列研究,选择2006 年 6 月至 2025 年 3 月就诊于空军军医大学第一附属医院消化内科并确诊为 PBC 的患者作为研究对象 。 符合以下三条中的两条即可确诊 PBC[14]:(1)存在胆汁淤积的生物化学证据,主要是碱性磷酸酶(alkaline phosphatase,ALP)和 γ-谷氨酰转移酶(γ-glutamyl transpeptidase,GGT)升高;(2)抗线粒体抗体及其 M2 亚型阳性,或其他 PBC 特异性自身抗体(抗 gp210 抗体、抗 sp100 抗体)阳性;(3)组织学上有非化脓性破坏性胆管炎和小胆管破坏的证据。纳入标准:(1)根据指南[14]确诊为 PBC 的患者;(2)进行了自身抗体检测的患者。排除标准:(1)合并有其他肝脏疾病,比如自身免疫性肝炎 、乙型病毒性肝炎、丙型病毒性肝炎
、乙型病毒性肝炎、丙型病毒性肝炎 、酒精性肝损害以及药物性肝损害;(2)基线时出现失代偿事件,比如腹水、静脉曲张出血、肝移植或死亡;(3)无随访记录。
、酒精性肝损害以及药物性肝损害;(2)基线时出现失代偿事件,比如腹水、静脉曲张出血、肝移植或死亡;(3)无随访记录。
2. 随访及临床终点指标:以 PBC 患者首次确诊时间为基线,患者确诊后即开始 UDCA 治疗,并维持剂量为 13~15 mg/kg。随访终点以及不良事件定义为:出现肝硬化相关并发症,包括腹水、肝性脑病、静脉曲张出血、肝癌、肝移植以及死亡;腹水的诊断参考《肝硬化腹水 诊疗指南(2023 年版)》[15],肝性脑病的诊断依据《肝硬化肝性脑病诊疗指南(2024 年版)》[16],肝癌的诊断标准符合《原发性肝癌
诊疗指南(2023 年版)》[15],肝性脑病的诊断依据《肝硬化肝性脑病诊疗指南(2024 年版)》[16],肝癌的诊断标准符合《原发性肝癌 诊疗指南(2024 年版》[17]。随访过程中未出现终点事件的患者在末次随访时删失处理。
诊疗指南(2024 年版》[17]。随访过程中未出现终点事件的患者在末次随访时删失处理。
3. 观察指标:收集基线的临床资料,包括人口学资料:性别及年龄;实验室检查指标:血小板计数(platelet count,PLT)、白蛋白(albumin,Alb)、ALP、GGT、总胆红素(total bilirubin,TBil)、丙氨酸 转氨酶(alanine transaminase,ALT)、天冬氨酸转氨酶(aspartate transaminase,AST)、免疫球蛋白 M(immunoglobulin M,IgM)、抗 gp210 抗体和ACA,抗 gp210 抗体和 ACA 采用免疫印迹法进行检测;以及组织学分期和腹部超声资料,根据Ludwig 分期[18],按照基线时患者的组织学分期资料,将病理Ⅰ+Ⅱ期定义为早期,病理Ⅲ+Ⅳ期定义为晚期。巴黎Ⅰ标准[19]( Paris Ⅰ)、巴黎Ⅱ标准[20](Paris Ⅱ)和鹿特丹标准[21]( Rotterdam)用以评估PBC 患者 UDCA 治疗 1 年后的生物化学应答情况;GLOBE 评分系统[22]用于评估 PBC 患者病情的严重程度,在 UDCA 治疗 1 年后 GLOBE 评分≤0.3 分的患者预后较好。定义新生物化学应答标准:UDCA治疗 1 年后,Alb≥1×正常参考值下限(lower limit of normal,LLN)且 PLT≥1×LLN。
转氨酶(alanine transaminase,ALT)、天冬氨酸转氨酶(aspartate transaminase,AST)、免疫球蛋白 M(immunoglobulin M,IgM)、抗 gp210 抗体和ACA,抗 gp210 抗体和 ACA 采用免疫印迹法进行检测;以及组织学分期和腹部超声资料,根据Ludwig 分期[18],按照基线时患者的组织学分期资料,将病理Ⅰ+Ⅱ期定义为早期,病理Ⅲ+Ⅳ期定义为晚期。巴黎Ⅰ标准[19]( Paris Ⅰ)、巴黎Ⅱ标准[20](Paris Ⅱ)和鹿特丹标准[21]( Rotterdam)用以评估PBC 患者 UDCA 治疗 1 年后的生物化学应答情况;GLOBE 评分系统[22]用于评估 PBC 患者病情的严重程度,在 UDCA 治疗 1 年后 GLOBE 评分≤0.3 分的患者预后较好。定义新生物化学应答标准:UDCA治疗 1 年后,Alb≥1×正常参考值下限(lower limit of normal,LLN)且 PLT≥1×LLN。
4. 统计学方法:采用 SPSS 26.0 软件对数据进行统计学分析,符合正态分布的计量资料以均数±标准差(xˉ±s)表示,组间比较采用独立样本 t检验;非正态分布的计量资料以中位数及四分位数[M(Q1,Q3)]表示,组间比较采用 Mann-Whitney U秩和检验。计数资料以频数和百分比表示,组间比较采用χ2 检验或 Fisher 确切概率法检验,不同生物化学标准的应答者/非应答者终点事件发生率比较采取χ2检验。以出现相关终点事件(肝硬化相关并发症、肝移植或死亡)为结局,采用 Kaplan-Meier 法绘制生存曲线,组间差异比较采用 Log-Rank 检验,计算风险比(hazard ratio,HR)及 95% 置信 区 间(confidence interval,CI),以 P<0.05 为差异有统计学意义。通过受试者操作特征(receiver opera-ting characteristic curve,ROC)曲线下面积(area under the curve,AUC)、灵敏度、特异度分析不同生物化学应答标准和评分系统的预测效能;为进一步验证新生物化学应答标准 ROC 曲线的稳定性,采用 Bootstrap 自助法重复抽样 1 000 次,计算抗 gp210 抗体和 ACA 双阳性早期 PBC 患者中新生物化学应答标准 AUC 的 95%CI,评估模型预测效能的可靠性。
结 果
1. 各组患者临床特征:本研究从 1 997 例 PBC患者中,按筛选流程 ,共纳 入 1 286 例 PBC 患者( 图 1)。 将 1 286 例患者按照抗 gp210 抗体和 ACA 的状态分为 4 组 :Anti-gp210-ACA-组、Anti-gp210+ACA-组、ACA+Anti-gp210- 组以及Anti-gp210+ACA+组,患者临床特征见表 1。4 组患者女性占比分别为 84.07%(459/546)、81.57%(301/369)、96.27%(258/268)和 94.17%(97/103);PLT 中位数分别为 1.42×LLN、1.41×LLN、1.17×LLN 和 1.02×LLN;各组出现静脉曲张出血的患者比例为 4.95%(27/546)、7.05%(26/369)、11.19%(30/268)和 18.45%(19/103);出现终点事件的患者比例为 19.05%(104/546)、26.56%(98/369)、28.73%(77/268)和 46.60%(48/103)。相较于其他 3 组,Anti-gp210+ACA+组早期患者出现终点事件的发生率较高(46.05%,35/76),差异有统计学意义(P<0.001),而晚期患者出现终点事件的发生率差异无统计学意义。生存分析显示,相较于其他 3 组,Anti-gp210+ACA+组无不良事件生存期显著缩短,差异有统计学意义(P<0.05),见图 2。
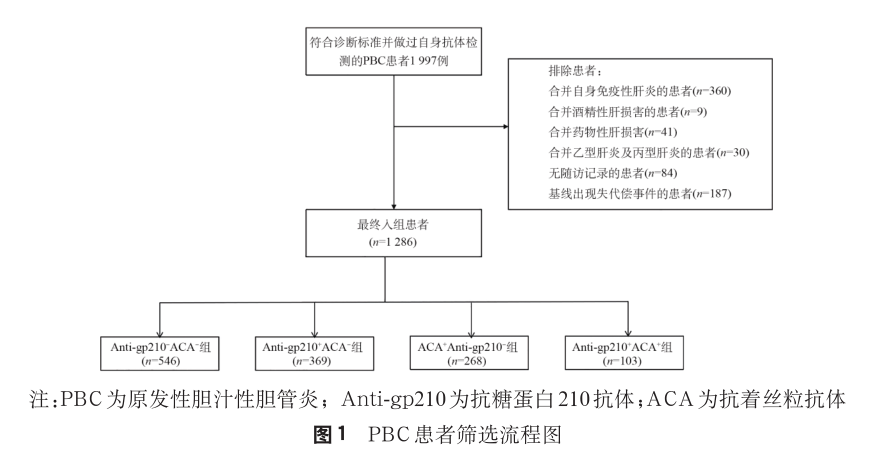
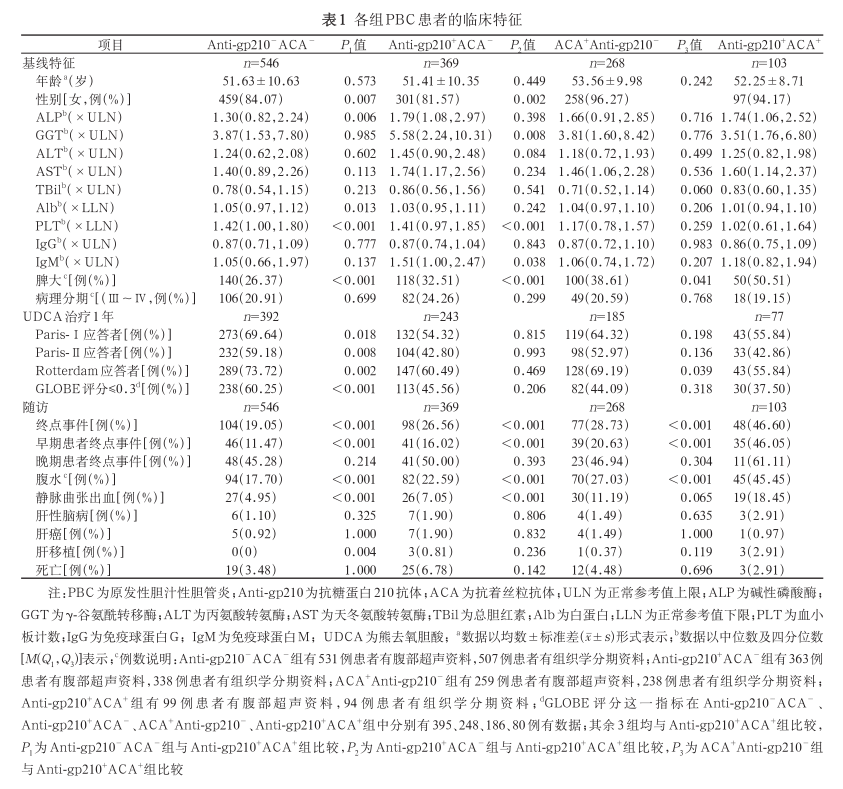
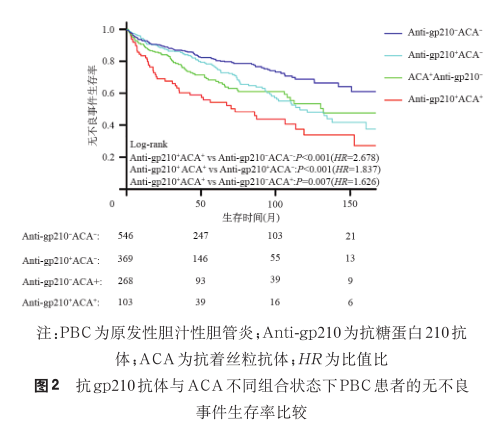
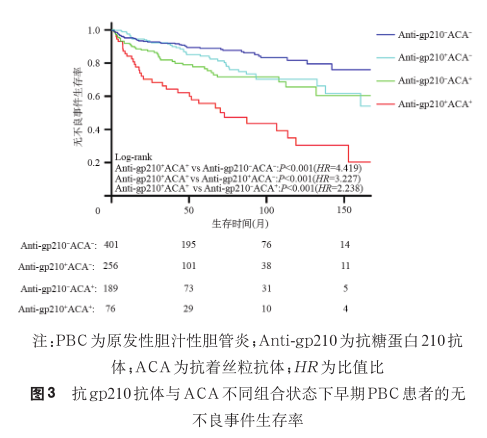
2. 早期 PBC 患者中各组的临床特征:按照抗gp210 抗体和 ACA 的状态将早期 PBC 患者分为4 组 :Anti-gp210-ACA-组、Anti-gp210+ACA-组、ACA+Anti-gp210-组以及 Anti-gp210+ACA+组,临床特征见表 2。 4组患者女性占比分别为 84.29%(338/401)、82.42%(211/256)、96.30%(182/189)和 94.74%(72/76);Alb 中位数为 1.07×LLN、1.05×LLN、1.05×LLN 和 1.02×LLN;PLT 中位数为 1.51×LLN、1.55×LLN、1.22×LLN 和 1.01×LLN。与其他 3 组相比,Anti-gp210+ACA+组 Alb 和PLT 水平更低,差异有统计学意义(P<0.05)。4 组患者出现静脉曲张出血的比例为 2.00%(8/401)、4.30%(11/256)、8.99%(17/189)和 23.68%(18/76);出现终点事件的患者比例为 11.47%(46/401)、16.02%(41/256)、20.63%(39/189)和 46.05%(35/76)。UDCA 治疗 1 年后,4 组患者 Paris-Ⅰ标准的应答率为 74.83%、60.77%、69.47% 和 55.17%;Paris-Ⅱ标准的应答率为 64.83%、48.07%、60.31% 和 44.83%。相较于 Anti-gp210-ACA- 组,Anti-gp210+ACA+ 组Paris-Ⅰ标准、Paris-Ⅱ标准和 Rotterdam 标准的生物化学应答率较低,GLOBE 评分≤0.3 分的患者比例更低,差异有统计学意义(P值均<0.05);而相较于其他 2 组,Anti-gp210+ACA+组的部分生物化学应答率差异无统计学意义。生存分析显示,相较于其他 3 组,Anti-gp210+ACA+组无不良事件生存率较低,差异有统计学意义(P<0.05),见图 3。
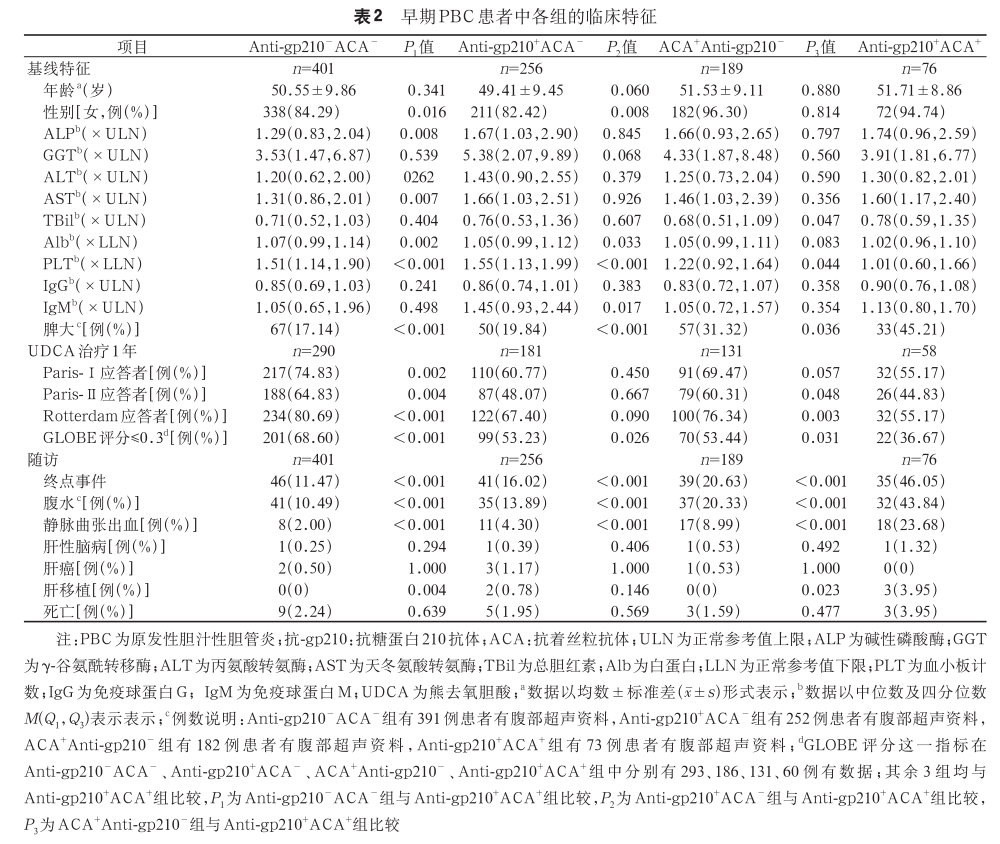
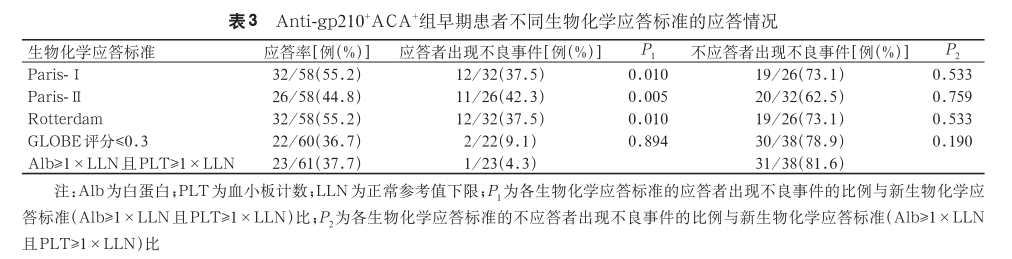
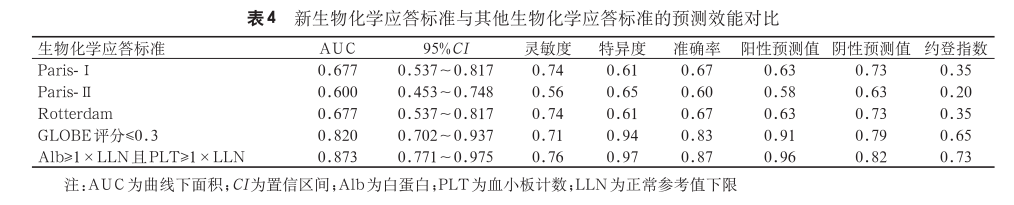
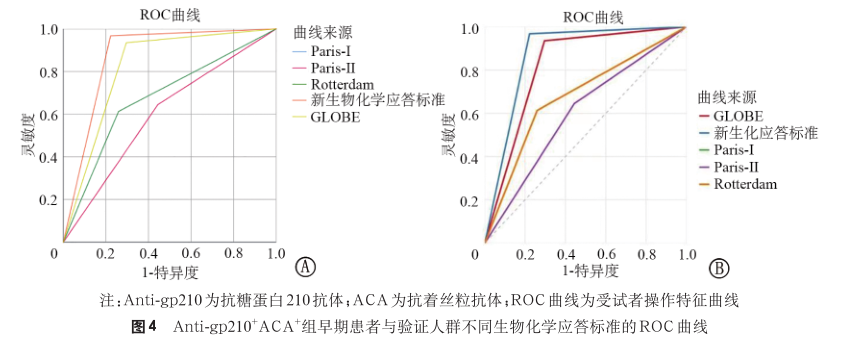
3. Anti-gp210+ACA+组早期患者的生物化学应答情况:新生物化学应答标准定义为,UDCA 治疗 1 年后,Alb≥1×LLN 且 PLT≥1×LLN。 各生物化学应答标准的应答情况见表 3。Paris-Ⅰ标准 、Paris-Ⅱ标准、Rotterdam 标准以及新生物化学应答标准的应答率为 55.2%、44.8%、55.2% 和 37.7%;应答者出现不良事件的比例为 37.5%、42.3%、37.5%和 4.3%;不应答者出现不良事件的比例为 73.1%、62.5%、73.1% 和 81.6%。新生物化学应答标准与其他生物化学应答标准相比,应答者出现不良事件的比例显著降低,差异有统计学意义(P<0.05),而不应答者出现不良事件比例差异无统计学意义。GLOBE 评分系统≤0.3 分的患者出现不良事件的比例为 9.1%,与新生物化学应答标准的差异无统计学意义。 ROC 曲线 显 示( 图 4A),Paris- Ⅰ 标准 、Paris-Ⅱ标准、Rotterdam 标准、GLOBE 评分以及新生物化学应答标准的 AUC 分别为 0.677、0.600、0.677、0.820 和 0.873;约登指数分别为 0.35、0.20、0.35、0.65 和 0.73,见表 4。用 Bootstrap 方法对早期双阳性患者的新生物化学应答标准进行 ROC 曲线稳定性的验证,Bootstrap 验证显示新生物化学应答标准 的 AUC 为 0.873, 95%CI 为 0.769~0.942(图 4B)。
讨 论
PBC 是一种以进行性胆管破坏为特征的慢性肝病,约 30%~40% 患者对一线药物 UDCA 应答不佳,预后不良风险显著升高[14,23-25]。抗 gp210 抗体是 PBC 的特异性抗核抗体,其阳性率在不同洲的人群中略有差异,在西方国家人群中抗 gp210 抗体阳性率约为16.7%[7],而东方亚洲国家人群抗 gp210 抗体阳性率较高,为 26.1%~48.2%[8,26-27],本中心抗 gp210 抗体阳性率为 36.7%。而 ACA 的阳性率变化较大,本中心 ACA 阳性率为 28.8%,高于之前的一项研究24.9%[28];抗 gp210 抗体和 ACA 与 PBC 患者的预后相关;抗 gp210 抗体阳性的 PBC 患者预后较差,病程常表现为肝衰竭型进展,而 ACA 阳性的 PBC 患者常表现为门静脉高压型进展[29-32]。
本研究根据抗 gp210 抗体和 ACA 的状态,将总人群分为 4 组,发现抗 gp210 抗体阳性且 ACA 阳性的 PBC 患者预后较差,这与之前的研究结论一致,该研究发现抗 gp210 抗体阳性且 ACA 阳性是 PBC 患者出现肝移植或死亡的独立预后标志物,可进一步优化 GLOBE 评分[13]。但抗 gp210 抗体和 ACA 双阳性患者预后差的原因尚不明确,之前的研究并未探索现有的生物化学应答标准是否适用于双阳性的患者。
本研究揭示了抗 gp210 抗体和 ACA 双阳性对 PBC 患者的预后与病理分期相关,仅早期患者出现终点事件的风险显著增加。而组织学分期晚期的患者的终点事件发生率在各组间差异无统计学意义。抗 gp210 抗体靶向核孔复合体蛋白 gp210,有研究结果显示,抗 gp210 抗体加剧胆管上皮细胞凋亡及胆管损伤,且抗 gp210 抗体阳性患者存在更严重的胆管破坏和纤维化进程[30,33],而 ACA 会促进 PBC 患者的门静脉高压进展,可能与 ACA 阳性患者的胆管反应、胆管损伤或胆管缺失严重相关[34-35],从而导致早期双阳性患者预后较差。而晚期患者可能因为进入终末期,并发症较多,抗体状态对预后的影响被终末期病理进程掩盖,并且 UDCA 对晚期患者疗效有限,因此晚期双阳性患者的终点事件发生率与其他组差异无统计学意义,提示双阳性患者需要积极监测病情发展情况并尽早干预。
本研究结果显示,抗 gp210 抗体和 ACA 双阳性的早期患者 Alb 和 PLT 水平显著低于其他患者,提示这类患者在早期肝脏合成功能就受到影响,门静脉高压风险较高。现有生物化学应答标准主要包含了胆汁淤积相关指标,而不包含门静脉高压相关指标如 PLT,用现有的生物化学应答标准去评估早期双阳性患者 UDCA 治疗 1 年后的生物化学应答情况,发现目前的生物化学应答标准可能低估了双阳性患者的实际风险,应答者出现终点事件的比例仍较高。因此,我们提出一个新的生物化学应答标准,即将 Alb、PLT 均正常定义为生物化学应答。新的生物化学应答标准能有效区分出应答者和不应答者,应答者出现终点事件的比例显著降低,预测效能优于现有的生物化学应答标准。而 GLOBE 评分也能以 0.3 分为阈值,较好地预测早期双阳性患者出现终点事件的风险。这可能是因为现有的生物化学应答标准均不含有 PLT 这一指标 ,而早期双阳性患者Alb、PLT 值显著降低,GLOBE 评分系统和新生物化学应答标准均含有 Alb、PLT 这两个指标,因此预测效能较好。而相比 GLOBE 评分,我们提出的新生物化学应答标准更简易,更便于临床医生使用。
本研究也存在一定的局限性,单中心回顾性研究可能导致选择偏移,纳入的患者群体主要反映中国西北地区人群特征,并且作为三甲医院可能富集病情更复杂,进展更快的患者,可能导致双阳性组终点事件率偏高,但本研究的大样本量和对患者的长期随访能在一定程度上弥补这一缺陷。其次,本研究没有设计验证队列,未来还需要前瞻性的多中心大队列来进一步验证本研究提出的生物化学应答标准的预测效能和临床应用价值。
总之,本研究通过大样本回顾性队列,揭示了抗 gp210 抗体和 ACA 双阳性对早期 PBC 患者预后的突出影响,并基于 UDCA 治疗 1 年后的 Alb 和 PLT 水平提出了针对该人群的生物化学应答标准,为高危 PBC 患者的早期干预提供了重要依据。
本平台旨在为医疗卫生专业人士传递更多医学信息。本平台发布的内容,不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议。如该等信息被用于了解医学信息以外的目的,本平台不承担相关责任。本平台对发布的内容,并不代表同意其描述和观点。若涉及版权问题,烦请权利人与我们联系,我们将尽快处理。


