
话题|时空解码,多维融合:毛晓韵教授解读2025乳腺癌研究关键突破(基础篇)
“基于循证,立足临床;聚焦争议,表达观点”——欢迎来到医脉通特别栏目《话题》

前言
2025年圣安东尼奥乳腺癌 研讨会(SABCS)的年度回顾环节中,来自匹兹堡大学医学中心希尔曼癌症中心(UPMC Hillman Cancer Center)的 Adrian V. Lee 博士于12月12日发表了题为《2025 Year in Review–Basic Science》的专题报告,不仅系统梳理了乳腺癌基础研究领域过去一年的突破性进展,更重点聚焦于人工智能驱动的计算生物学、单细胞与空间测序技术,以及循环肿瘤DNA(ctDNA)、循环肿瘤细胞(CTC)分析等液体活检手段的融合应用展开系统分析。这些技术正在以前所未有的分子分辨率,从时空维度重塑临床医生对乳腺癌的解析能力,为理解乳腺癌病因、耐药机制及最终改善患者预后带来深远影响。
研讨会(SABCS)的年度回顾环节中,来自匹兹堡大学医学中心希尔曼癌症中心(UPMC Hillman Cancer Center)的 Adrian V. Lee 博士于12月12日发表了题为《2025 Year in Review–Basic Science》的专题报告,不仅系统梳理了乳腺癌基础研究领域过去一年的突破性进展,更重点聚焦于人工智能驱动的计算生物学、单细胞与空间测序技术,以及循环肿瘤DNA(ctDNA)、循环肿瘤细胞(CTC)分析等液体活检手段的融合应用展开系统分析。这些技术正在以前所未有的分子分辨率,从时空维度重塑临床医生对乳腺癌的解析能力,为理解乳腺癌病因、耐药机制及最终改善患者预后带来深远影响。
生殖系与体细胞基因组学
一篇2025年1月发表于《Cell》的研究[1]介绍了PCSK9(Proprotein Convertase Subtilisin/Kexin Type 9)胚系突变,野生型PCSK9蛋白在人体中与肝脏表面LRP1(Low-Density Lipoprotein Receptor-Related Protein 1)结合介导LRP1溶酶体降解,从而减少细胞表面LRP1数量,最终影响脂质代谢、细胞信号传导及疾病进程。研究显示,一旦PCSK9出现rs562556(V474I,474位缬氨酸变为异亮氨酸)胚系变异,它就不再与肝细胞中LRP1受体结合,只与肿瘤细胞表面的LRP1受体结合,进一步解除LRP1对XAF1、USP18等促转移基因的抑制,最终导致肿瘤细胞的肺转移起始能力与转移灶增殖能力增强。小鼠基因敲入模型进一步验证了该变异的促转移效应,抗PCSK9抗体治疗或宿主PCSK9敲除可显著抑制转移定植,PCSK9这一功能获得性单核苷酸变异在白人女性中的携带率约为70%。瑞典早期乳腺癌大队列数据显示该变异纯合子患者的15年远处转移复发风险高达22%,而非纯合子患者仅为2%,风险差异达10倍。世界人群分布图谱也显示V474I变异在欧洲、北美及部分亚洲人群中广泛存在,该研究为携带V474I变异肿瘤人群降低其复发转移风险提供了极具潜力的新方向。
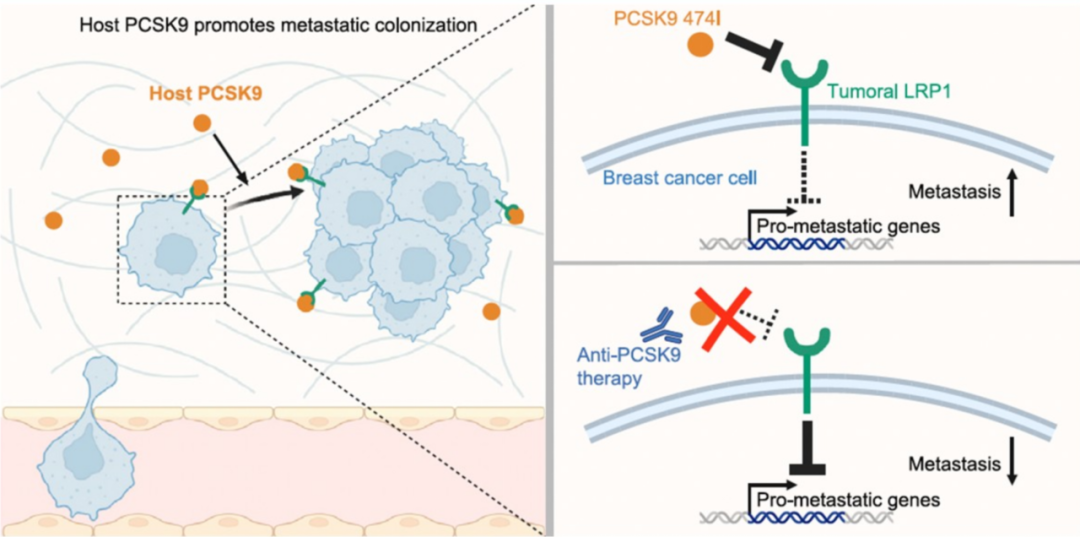
图1 PCSK9 靶向 LRP1 解除对促进转移基因表达抑制作用的机制图[1]
另一篇来自斯坦福大学研究团队发表于《Nature》的重磅研究[2]则发现,复杂基因组重排是驱动ER+和HER2+乳腺癌发生的关键因素之一。Christina Curtis团队将1828例乳腺肿瘤样本(导管原位癌、浸润性癌原发灶、转移性乳腺癌灶)基因组和转录组数据整合聚类(Integrative Cluster),结合近20年的随访数据开发了ENiClust(Ensemble Integrative Clustering)亚型系统,将乳腺癌分为三种主要基因组原型:TNBC、ER+/HER2−(典型风险和高风险)以及HER2+型。其中三阴性乳腺癌(TNBC)表现为全基因组不稳定性、同源重组缺陷和APOBEC编辑单核苷酸变异;典型风险ER+/HER2−表现为基因组相对稳定,以二倍体、低突变负荷为特征;高风险ER+/HER2−亚型以复杂局部扩增和ecDNA驱动为核心;HER2+型乳腺癌则伴随ER激活R-loop形成和APOBEC3B编辑,这些复杂的基因组重排模式在免疫逃逸和肿瘤免疫共同进化中发挥着关键作用,最终导致复发转移风险升高。上述基因组原型在肿瘤发生早期就已确立并塑造肿瘤微环境,并在转移性疾病中仍得以保留。不过这些复杂的结构性改变虽然促进了复制压力和免疫逃逸,并在肿瘤演变过程中持续存在,但也同时揭示了其潜在的脆弱性。研究最后强调不同乳腺癌亚型存在差异化潜在治疗靶点,如PARP抑制剂对HRD样肿瘤具有治疗敏感性,而针对复制压力途径的新药物则对局部扩增的ER+高风险肿瘤提供了潜在治疗策略。
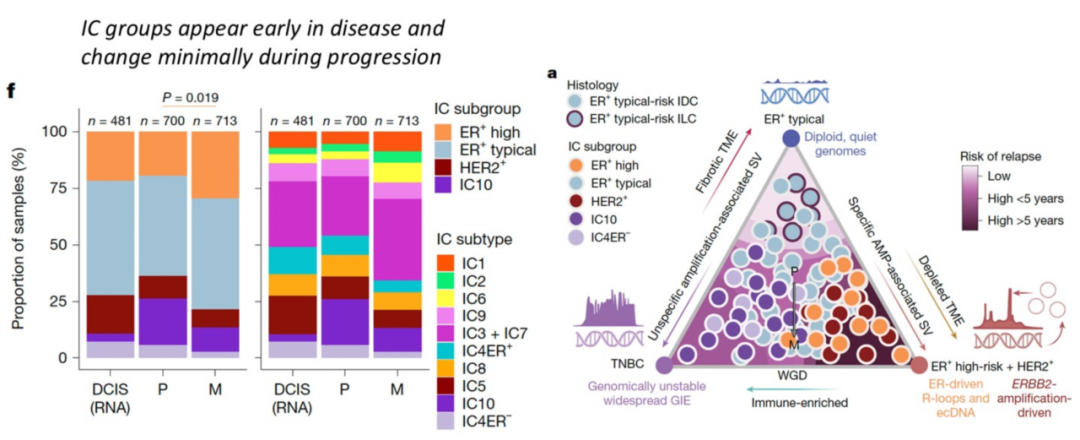
图2 IC亚群在不同进展阶段、祖先和组织学的分布[2]
单细胞和空间组学
肿瘤祖先克隆由于其基因组变化小,表型上更接近于正常上皮细胞,但这些祖细胞存在的比例极低(甚至可能在进化过程中消失),因此一直难以被捕获和研究。与此同时,在乳腺癌发生发展过程中,基因型改变(如DNA拷贝数的变异CNAs)如何影响表型(如基因的表达变化)从而推动乳腺癌进程,也是一个尚未解决的核心问题。根据经典的基因剂量模型,DNA拷贝数变化通常会引发同一染色体 区域基因表达水平的相应改变,但因缺乏单细胞层面基因型与表型的对应关系,这种改变始终难以精准量化。制约上述两个核心科学问题的最大瓶颈,在于缺乏高通量、高分辨率的单细胞基因型-表型共测序技术。一篇由MD安德森癌症中心的Nicholas Navin团队发表于《Cell》上的“Coalescing single-cell genomes and transcriptomes to decode breast cancer progression”研究[3]首次报道了高通量、高基因组分辨率的单细胞基因组(DNA)与转录组(RNA)共测序方法:wellDR-seq(well-based single-cell DNA and RNA sequencing),这种新技术可以在一个纳升反应小孔里面同时完成对DNA和RNA分子的标记和扩增,同时对数千个单细胞的基因组和转录组进行分析。研究者进一步对12例激素受体阳性乳腺癌研究发现,其祖先克隆RNA都具有最高的LumHR(Luminal Hormone-Responsive)上皮细胞特征计分,推测ER+的乳腺癌起源于正常乳腺的LumHR上皮细胞。
区域基因表达水平的相应改变,但因缺乏单细胞层面基因型与表型的对应关系,这种改变始终难以精准量化。制约上述两个核心科学问题的最大瓶颈,在于缺乏高通量、高分辨率的单细胞基因型-表型共测序技术。一篇由MD安德森癌症中心的Nicholas Navin团队发表于《Cell》上的“Coalescing single-cell genomes and transcriptomes to decode breast cancer progression”研究[3]首次报道了高通量、高基因组分辨率的单细胞基因组(DNA)与转录组(RNA)共测序方法:wellDR-seq(well-based single-cell DNA and RNA sequencing),这种新技术可以在一个纳升反应小孔里面同时完成对DNA和RNA分子的标记和扩增,同时对数千个单细胞的基因组和转录组进行分析。研究者进一步对12例激素受体阳性乳腺癌研究发现,其祖先克隆RNA都具有最高的LumHR(Luminal Hormone-Responsive)上皮细胞特征计分,推测ER+的乳腺癌起源于正常乳腺的LumHR上皮细胞。
该研究还首次在单细胞层面系统性地量化了基因拷贝数变异对基因表达的影响。通过对多个ER+乳腺癌样本的分析,有56%的CNAs片段与平均基因表达量呈正相关,随着拷贝数增加基因表达水平呈近线性增长。在单基因表达水平上,研究进一步将所有基因分为剂量敏感型(RNA表达量和功能与DNA拷贝数明显相关)和剂量不敏感型(RNA表达量和功能不受DNA拷贝数变化影响),PGR、AURKA和RB1为剂量敏感性,PIK3CA、BRCA1和TP53为剂量不敏感型,这些数据表明,CNAs虽然对基因表达有直接影响,但并非是所有基因表达差异的唯一决定因素。通过wellDR-seq的双模态数据,该研究揭示了基因组变异对转录组的复杂影响,为理解肿瘤的表型多样性提供了重要依据。
另一篇发表于《Cancer Cell》的文章[4]则对TNBC细胞表型和肿瘤空间结构特征进行了分层研究,既往多项研究聚焦TNBC的单细胞测序展开分析,但这项研究转换思路,用成像质谱流式技术(IMC)对215例TNBC患者的肿瘤样本进行单细胞分辨率的空间表型分析,结合肿瘤细胞表型和免疫细胞的空间分布和其快速复发临床预后,提出11种主导性肿瘤细胞表型,并整合肿瘤细胞的角蛋白表达谱(CK7 vs.CK5)和CD8+T细胞的空间分布模式将TNBC分为五个预后亚型:BL(Basoluminal,CK5+/CK7+为主)、B(Basal,CK5+为主)、L(Luminal,CK7+为主)和N型(Not basal/Not luminal,CK5-/CK7-为主)、INF型(炎症型),结合其不同的预后简化为高(BL)、中(B/L/N)、低(INF)风险组。联合多个队列分析发现,INF组对新辅助治疗有最佳的响应,而BL高风险组肿瘤具有干细胞样特征,在机制上可能通过巨噬细胞浸润、缺少与肿瘤互作的CD8+T细胞以及免疫抑制检查点上调等介导免疫逃逸,具有重要临床指导价值。
以上两项研究均聚焦原发性乳腺癌,然而在临床中,新辅助治疗后残留病灶所蕴含的信息往往也极具关注价值。一项来自于《Cell Reports Medicine》的研究[5],不仅覆盖了多种分子分型乳腺癌,还整合了大量多组学数据,为乳腺癌精准诊疗提供了新方向。单细胞空间转录组结合全基因组测序技术是一种保留组织原位结构的单细胞基因表达分析技术。传统单细胞转录组测序会把组织里的细胞打散,分离后再检测基因表达,无法知道细胞在组织里的真实位置和“邻居”是谁;而CosMx SMI技术可以直接对切片后的肿瘤组织进行检测,既能精准定位每个细胞在组织中的位置,又能分析单个细胞里上千个基因的表达情况。
由Ji-Yeon Kim领头的韩国研究团队借助单细胞空间转录组与全基因组测序技术,针对新辅助化疗后残留肿瘤负荷较高的乳腺癌患者开展研究,破解了这类患者预后差异显著的关键机制,单细胞空间转录组关注肿瘤微环境里的“细胞互动实况”,基因组测序则更重视肿瘤自身的“基因先天缺陷”,两者结合就能完整解析肿瘤的复杂特征。研究发现,不同乳腺癌亚型的预后受截然不同的基因组特征与肿瘤微环境调控——TNBC的预后好坏由免疫细胞互作主导,CXCL9阳性巨噬细胞与CD8+T细胞的协同作用则能改善预后,而缺氧信号驱动的SPP1阳性巨噬细胞与癌细胞的相互作用则会导致预后不良;非TNBC的预后则与基底样癌细胞占比、其与免疫细胞的空间距离,以及肿瘤自身的基因组异常密切相关,如HR+亚型的同源重组缺陷、HER2+亚型的染色体外ERBB2 DNA结构变异,都会加剧预后不良风险,该研究不仅为高残留肿瘤负荷乳腺癌患者的精准预后分层提供了可靠标志物,更为后续开发亚型特异性的靶向治疗方案奠定了重要基础。
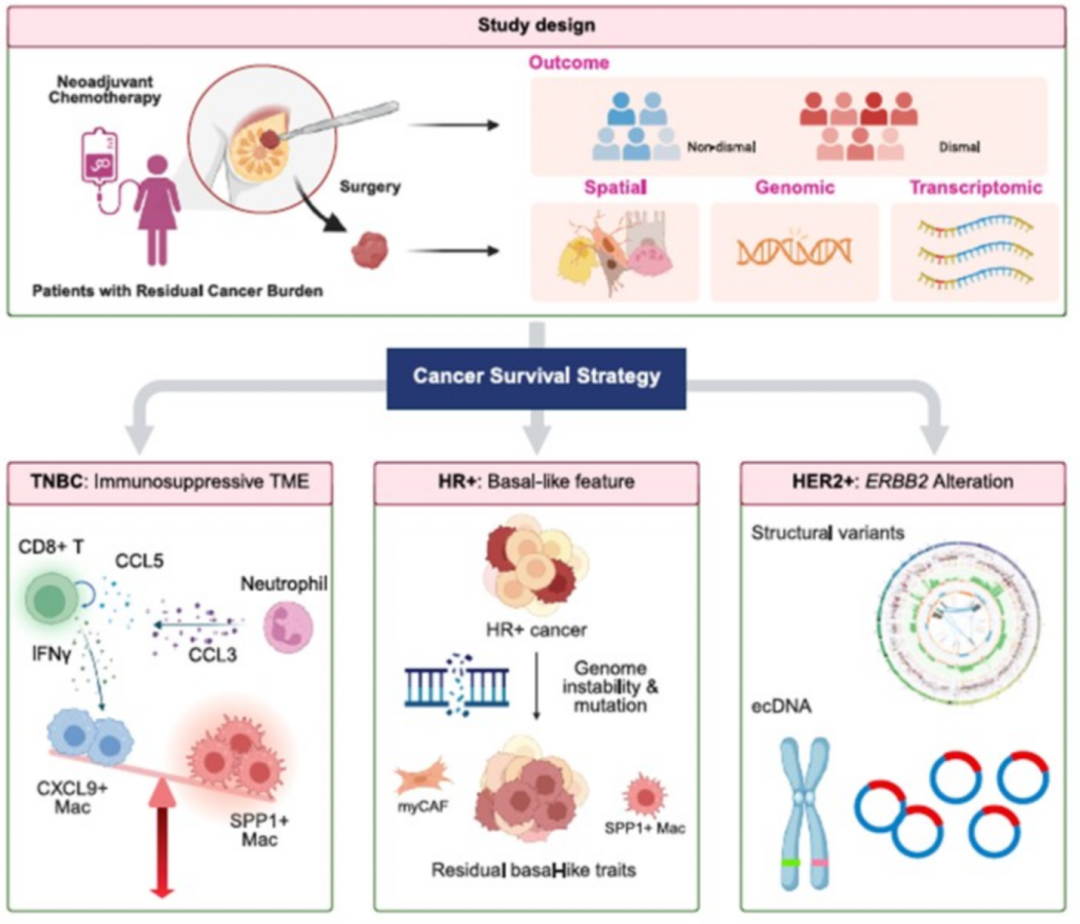
图3 新辅助化疗后残留乳腺癌的空间和基因组特征分析[5]
液体活检 (ctDNA)
该领域研究难度颇高,药物处理后耐药性等复杂因素的介入则进一步加剧了研究挑战难度,也正因如此,液体活检和ctDNA技术才会快速发展起来。一项由Nancy U Lin开展的抗HER2靶向治疗前后的液体活检研究[6],将肿瘤组织全外显子测序(WES)与治疗前ctDNA动态监测结合起来,对111例患者的73份肿瘤活检样本和120份ctDNA样本进行了系统性分析。这种整合策略不仅覆盖了更大规模的患者队列,寻找治疗耐药后被激活的信号通路,发现已知耐药驱动基因(如Ras、p53、PIK3CA、ERBB2)的变异,从而验证了PI3K-AKT通路激活、HER2基因扩增等经典耐药机制,还在5例患者中发现了亚克隆扩增驱动的新耐药突变(如ESR1、FGFR2、FGFR4),这些突变在初始组织活检中并未被检出,仅在耐药发生后的ctDNA中被动态捕捉到,在发生脑转移的患者中,Wnt信号通路相关基因显著富集,这条通路上的多个靶点都具有潜在的临床应用价值,值得后续进一步探索。
另一篇由比利时Christine Desmedt研究团队发表在《Nature Communications》的研究[7],则着眼于“液体活检虽常依赖血液中的ctDNA开展无创监测,但其他体液中ctDNA的转移灶代表性及临床价值尚未明确”这一研究点,对20例尸检的转移性乳腺癌女性患者的216份七种体液样本(血液、腹水 、脑脊液、心包液、胸水、唾液、尿液)和745份转移组织样本开展低通量全基因组测序,同时对11例患者的86份体液样本进行全外显子测序以分析突变信息,结果发现七种体液均能检出ctDNA,其中血液检出率最高,腹水、胸水、脑脊液紧随其后,且不同体液对转移灶的代表性存在差异,非血液体液还能提供独有的临床相关突变和基因拷贝数信息,该研究提示多体液联合检测的策略有望进一步提升转移性乳腺癌的监测与特征分析水平。
、脑脊液、心包液、胸水、唾液、尿液)和745份转移组织样本开展低通量全基因组测序,同时对11例患者的86份体液样本进行全外显子测序以分析突变信息,结果发现七种体液均能检出ctDNA,其中血液检出率最高,腹水、胸水、脑脊液紧随其后,且不同体液对转移灶的代表性存在差异,非血液体液还能提供独有的临床相关突变和基因拷贝数信息,该研究提示多体液联合检测的策略有望进一步提升转移性乳腺癌的监测与特征分析水平。
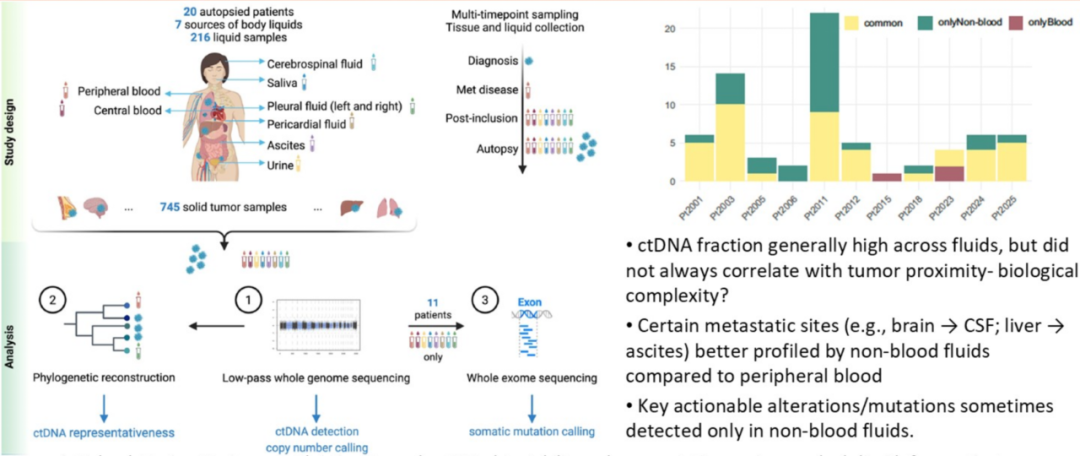
图4 研究设计及其目标,体液中检测到突变[7]
患者来源类器官(PDO)
患者来源类器官(PDO)近年来发展迅猛,一篇发表于《Nature Cancer》的研究“Circulating tumor cell plasticity determines breast cancer therapy resistance via neuregulin 1-HER3 signaling”[8]着眼于CTC来源的类器官,即循环肿瘤细胞衍生类器官(CDO),旨在探讨CTCs的可塑性如何通过特定信号通路导致乳腺癌治疗耐药。CTC在血液中含量极低,难以培养和研究,因此亟需可靠的扩增方法来解析其与疾病进展、治疗反应的关联。研究团队成功建立了转移性乳腺癌患者的长期CTC衍生类器官平台,解决了CTCs难以大量培养的难题,为后续研究提供了重要工具。通过多组学分析和动物模型验证,研究发现NRG1-HER3信号通路是维持CTCs存活、生长和扩散的关键;进一步的基因筛选显示,FGFR1信号通路可作为“后备力量”在NRG1-HER3通路功能不足时进行补偿,反之NRG1-HER3通路激活会让CTCs对FGFR1抑制剂产生耐药,联合阻断这两条通路能有效抑制CTCs生长。两条通路的动态互作揭示癌细胞可塑性分子基础为临床提供了可行的靶向治疗策略;同时CTC类器官平台能精准识别患者个体的肿瘤弱点。总体而言,该研究整合先进技术与研究探索,为乳腺癌研究指明了未来发展的重要方向。
变异等位基因频率(VAF)是指在检测到的DNA序列中,携带肿瘤特异性突变的等位基因占总等位基因的比例。其数值的高低直接反映了血液中ctDNA的含量多少,间接对应体内肿瘤负荷的大小,而ctDNA变异VAF的动态变化可反映实时治疗效果,基于ctDNA VAF及时调整治疗方案,有望精准筛选出最优疗法,应对乳腺癌不断演变的耐药问题。一项中国团队发表在《Cancer Research》上的研究[9]开发了一种整合ctDNA动态监测与序贯类器官药物筛选的乳腺癌治疗优化方案。研究人员对71例乳腺癌患者的血浆样本进行靶向深度测序,结果显示ctDNA清除与患者无病生存期改善显著相关,证实了ctDNA动态监测在疗效评估中的核心价值。同时对40个乳腺癌类器官模型的分析表明,类器官培养上清液可用于全面的基因突变分析和药物敏感性检测,为个体化用药提供可靠依据,将ctDNA动态监测与类器官药物筛选相结合,能够为乳腺癌治疗方案的调整提供精准指导,是优化患者治疗结局的一种极具潜力的策略。
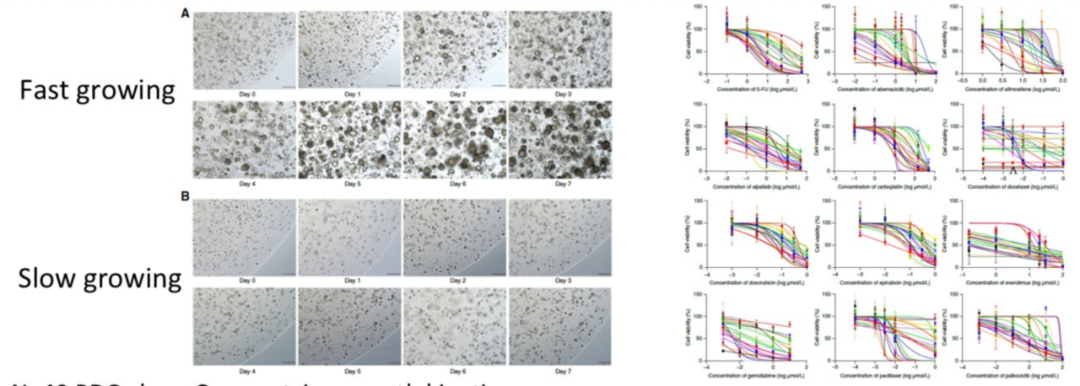
图5 患者来源类器官快速及缓慢生长的代表性明场图像和药物测试的剂量反应曲线[9]
病毒感染与疫苗接种
一篇由科罗拉多大学研究人员在《Nature》发表的文章“呼吸道病毒感染可唤醒肺部休眠的转移性乳腺癌细胞”[10]解析了打破休眠播散癌细胞(DCCs)静息状态的机制,这一机制是攻克乳腺癌转移进展的关键。流感 、新冠病毒等呼吸道病毒感染,会引发局部及全身性炎症反应。这项研究通过小鼠模型证实流感和新冠病毒感染会使肺部的乳腺癌休眠DCCs丧失促休眠表型:感染后数天内这些休眠癌细胞就会开始增殖,两周内便会大量扩增为转移性病灶,这一表型转变和细胞扩增过程均依赖白细胞介素6。DCCs还会抑制肺部T细胞的活化,流感感染后CD4+T细胞会通过抑制CD8+T细胞的活化与杀伤功能维持肺部转移灶的负荷。研究进一步对英国Biobank(涵盖所有癌症类型)和FlatironHealth(乳腺癌专项)数据库中癌症幸存者进行分析,结果显示与未感染的癌症幸存者相比,感染新冠病毒的患者,其癌症相关死亡风险和肺转移风险均显著升高;确诊乳腺癌后感染COVID-19的女性患者,其肺转移风险(经年龄、种族、族裔调整)显著增加,风险比为1.44。这些结果显示,COVID-19确实增加了乳腺癌女性患者肺转移的风险。该研究揭示了呼吸道病毒感染对转移性癌症复发的重大影响,为阐明感染性疾病与癌症转移之间的关联提供了全新见解。
、新冠病毒等呼吸道病毒感染,会引发局部及全身性炎症反应。这项研究通过小鼠模型证实流感和新冠病毒感染会使肺部的乳腺癌休眠DCCs丧失促休眠表型:感染后数天内这些休眠癌细胞就会开始增殖,两周内便会大量扩增为转移性病灶,这一表型转变和细胞扩增过程均依赖白细胞介素6。DCCs还会抑制肺部T细胞的活化,流感感染后CD4+T细胞会通过抑制CD8+T细胞的活化与杀伤功能维持肺部转移灶的负荷。研究进一步对英国Biobank(涵盖所有癌症类型)和FlatironHealth(乳腺癌专项)数据库中癌症幸存者进行分析,结果显示与未感染的癌症幸存者相比,感染新冠病毒的患者,其癌症相关死亡风险和肺转移风险均显著升高;确诊乳腺癌后感染COVID-19的女性患者,其肺转移风险(经年龄、种族、族裔调整)显著增加,风险比为1.44。这些结果显示,COVID-19确实增加了乳腺癌女性患者肺转移的风险。该研究揭示了呼吸道病毒感染对转移性癌症复发的重大影响,为阐明感染性疾病与癌症转移之间的关联提供了全新见解。
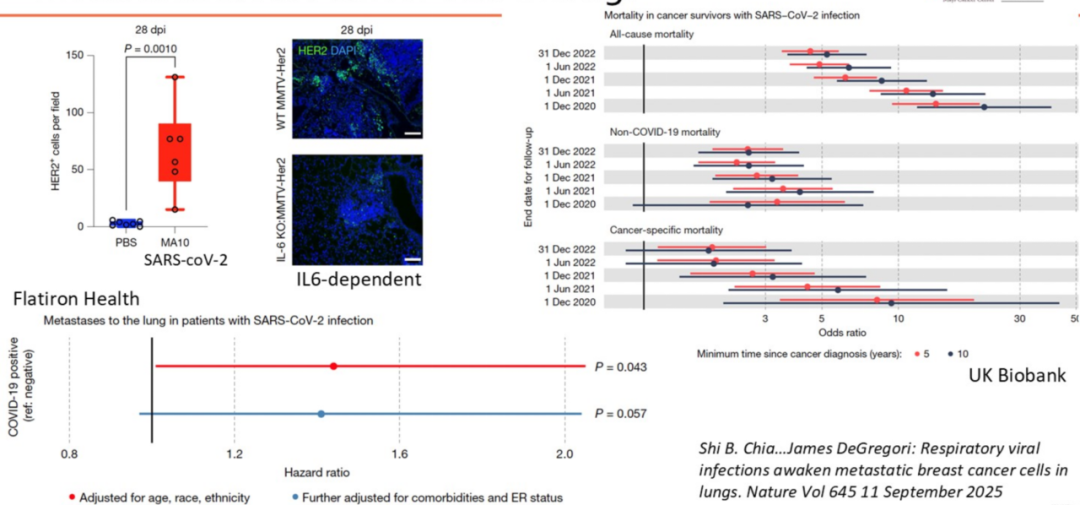
图6 SARS-CoV-2感染后癌症进展、肺部转移和死亡率[10]
另一篇发表于《Nature》的“SARS-CoV-2 mRNA vaccines sensitize tumors to immune checkpoint blockade”研究[11],则首次揭示COVID mRNA疫苗作为广谱免疫激活剂,可通过激活免疫反应显著提高晚期癌症对免疫疗法的敏感性。研究发现靶向非肿瘤抗原的mRNA疫苗 (COVID mRNA疫苗) 会刺激干扰素-γ在内的细胞因子,从而驱动天然免疫激活,而这种激活的天然免疫细胞会启动T细胞激活并浸润到肿瘤中。尽管肿瘤细胞会通过上调PD-L1表达来逃避T细胞攻击,但COVID mRNA疫苗与免疫检查点抑制剂(ICI)的联合使用能够克服这种代偿反应,从而抑制肿瘤生长并提高癌症患者生存率。该发现为开发广谱型mRNA癌症疫苗打开了新的思路,并且为免疫疗法弱响应的癌症患者带来新的治疗曙光。
人体试验也观察到了一致的疫苗应答特征:在未接种疫苗、最近100天内接种过疫苗以及超过100天前接种过疫苗的个体中,近期接种疫苗个体肿瘤的PD-L1表达水平更高。健康志愿者体内出现I型干扰素水平升高及髓系-淋巴系细胞活化等免疫应答特征,非小细胞肺癌患者的肿瘤组织则表现为PD-L1表达上调。就此,研究者开展了一系列动物实验进行机制探索。此外多项大型回顾性队列研究显示,在启动ICI治疗的100天内接种新冠mRNA疫苗的患者,其中位总生存期和3年总生存期均得到显著改善,且这种获益在免疫“冷肿瘤”患者中同样存在。该研究证实,这款临床上已广泛应用的、靶向非肿瘤相关抗原的mRNA疫苗是一种强效的免疫调节剂,能够增强肿瘤对免疫检查点抑制剂的敏感性,这项研究进一步揭示了病毒感染和疫苗接种影响肿瘤微环境,涉及转移部位或原发部位的免疫系统的机制。
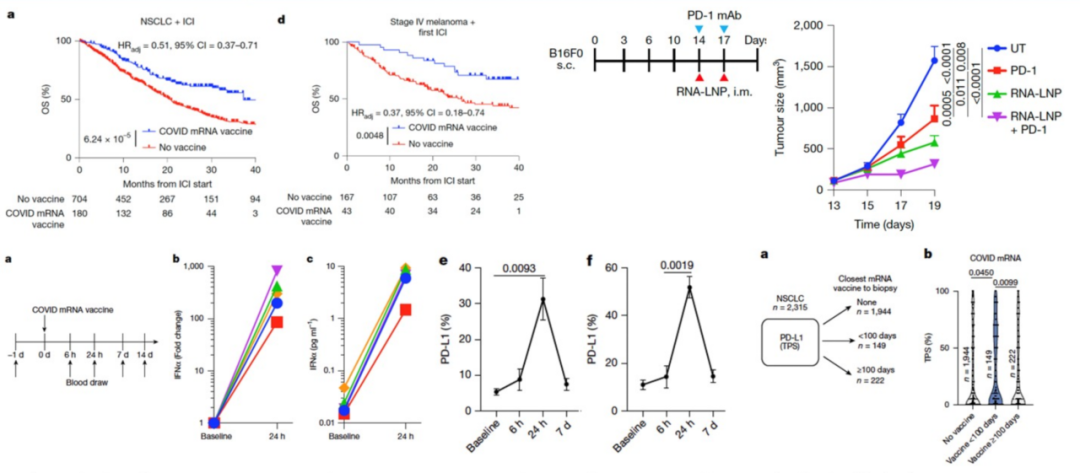
图7 接受免疫治疗的NSCLC或转移性黑色素瘤患者的生存率[11]
在此基础上,一个新的问题也由此产生:类似的免疫激活效应是否也可由自然的生理过程触发?一篇来自Sherene Loi团队的研究[12]探索了妊娠对乳腺癌免疫系统的影响,既往研究已证实怀孕或生育会降低乳腺癌的风险,该研究则通过结合临床样本分析与动物实验,进一步揭示了其中的关键机制:在人类正常乳腺组织中,有过妊娠史的女性体内CD8+T细胞数量会明显增多,其中还包含具有组织驻留记忆样表型的细胞亚群。在小鼠模型中,经历“妊娠-哺乳-乳腺复旧”完整周期后乳腺组织内会大量聚集CD8+T细胞;同时小鼠的肿瘤生长受到抑制,肿瘤组织内的免疫细胞浸润程度也显著提升,而如果将小鼠体内的CD8+T细胞清除,这些抑癌效果就会完全消失。值得注意的是,这种依赖CD8+T细胞实现的肿瘤控制作用,仅在完成完整的哺乳与乳腺复旧周期后才会出现。临床数据也验证了这一结论:有过生育史女性的原发性TNBC,表现出更强的T细胞浸润水平,患者的临床结局也相应更好。该研究整合了临床前动物模型数据与超过1000例患者样本的分析结果,阐明了生育史如何塑造乳腺局部的免疫状态——这一过程可能源于乳腺癌退化过程中已经发生的免疫激活,明确了CD8+T细胞是介导妊娠相关乳腺癌保护作用的核心角色,为乳腺癌的预防与治疗策略开发提供了全新思路。
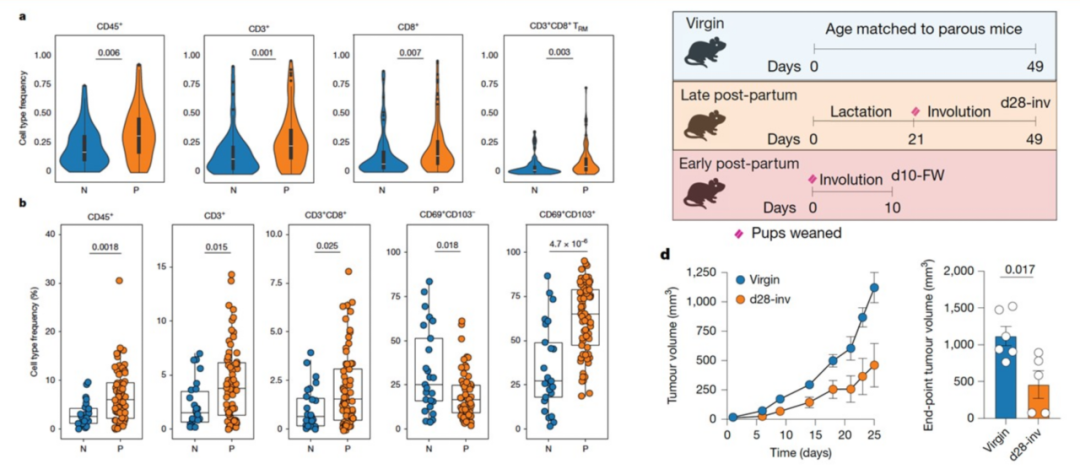
图8 胎位与未受影响的癌症中T细胞增加情况[12]
总之,人工智能驱动的计算方法、单细胞与空间组学分析技术再加上液体活检,让我们能以前所未有的分辨率从空间和时间维度研究乳腺癌的演化与异质性。肿瘤微环境的空间结构、免疫细胞间的相互作用,还有肿瘤细胞的异质性,正成为决定治疗响应和患者预后的关键因素。而循环肿瘤细胞衍生模型与ctDNA检测的结合也为个体化的动态诊疗决策提供了双重支撑,让功能性检测能与实时分子监测同步开展。同时还有新的研究证据显示气候变化、炎症反应与肿瘤休眠唤醒存在关联;而疫苗疗法也展现出了意料之外的保护效果,并能与其他治疗产生协同作用。这些技术和研究的突破,让我们离精准肿瘤学更近一步——以肿瘤生物学机制为核心导向,以前沿技术为赋能手段,更以患者的实际临床需求为根本驱动力,这一多维融合的格局,正在推动着乳腺癌诊疗从“被动应对”走向“主动规划”。
专家简介
毛晓韵 教授
主任医师 博士生导师
中国医科大学附属一院乳腺外科行政副主任
中国抗癌协会乳腺癌专业委员会青年专家
中华医学会肿瘤学分会乳腺肿瘤青年学组委员
中国老年保健乳腺癌专委会委员
中国抗癌协会肿瘤精准治疗专业委员会青年专家
中国抗癌协会乳腺癌整合防筛专委会常务委员
陈广洲
中国医科大学2024级
临床医学本科
撰稿:毛晓韵教授、陈广洲
审校:Oean
排版:Oean
执行:Oean
医脉通是专业的在线医生平台,“感知世界医学脉搏,助力中国临床决策”是平台的使命。医脉通旗下拥有「临床指南」「用药参考」「医学文献王」「医知源」「e研通」「e脉播」等系列产品,全面满足医学工作者临床决策、获取新知及提升科研效率等方面的需求。
本平台旨在为医疗卫生专业人士传递更多医学信息。本平台发布的内容,不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议。如该等信息被用于了解医学信息以外的目的,本平台不承担相关责任。本平台对发布的内容,并不代表同意其描述和观点。若涉及版权问题,烦请权利人与我们联系,我们将尽快处理。


