
IgA肾病伴系膜区Ⅲ 型胶原沉积2例
作者:黄洁波,蔡小凡,赵仲华,张志刚等,上海中医药大学附属普陀医院肾内科,上海市中医药大学附属龙华医院肾病一科,复旦大学基础医学院病理学系,电子显微镜中心实验室
Ⅲ型胶原蛋白(type Ⅲ collagen,Col Ⅲ)是一种间质胶原,通常表达于肾脏间质和血管壁,在正常肾小球中并无分布。当Col Ⅲ沉积在肾小球系膜区及内皮下区域时[1],为Col Ⅲ肾小球病(简称Col Ⅲ肾病),该病于1979年由日本学者首次报道[2],是一种全球散在分布的罕见疾病。Col Ⅲ肾病偶尔会合并IgA阳性,系膜区会有电子致密物沉积。而IgA肾病的肾小球中出现Col Ⅲ沉积的相关病例更为罕见,最早的报道[3]见于1989年,其病例并无Col Ⅲ肾病的病理特征,且有Col Ⅲ沉积的肾小球数量仅占受检肾小球总数的0.14%~0.25%。本研究为国内首次报道,与Col Ⅲ肾病合并IgA肾病不同,即光镜下无Col Ⅲ肾病表现,但每个肾小球中均有Col Ⅲ沉积于系膜区。本文主要研究分析该罕见病的临床表现、病理特征、发病机制及治疗预后,总结归纳该类疾病的发病进程,为临床诊疗提供新思路。
病例资料
病例1 患者女性,68岁,因“发现蛋白尿 7年,加重1周”入院。入院时泡沫尿,无肉眼血尿
7年,加重1周”入院。入院时泡沫尿,无肉眼血尿 ,无眼睑或四肢水肿
,无眼睑或四肢水肿 ,无眼部疾患或听力障碍,亦无指(趾)甲、髌骨或其他骨骼异常。否认高血压病、糖尿病等慢性病史。个人史、婚育史、家族史无殊。入院后实验室检查,尿常规
,无眼部疾患或听力障碍,亦无指(趾)甲、髌骨或其他骨骼异常。否认高血压病、糖尿病等慢性病史。个人史、婚育史、家族史无殊。入院后实验室检查,尿常规 :蛋白(+++),红细胞(+++)。24 h尿蛋白2.55 g,尿本周蛋白(-)。血生化:白蛋白28 g/L,肌酐75 μmol/L,尿素4.9 mmol/L,尿酸315 μmol/L,肾小球滤过率(estimated glomerular filtration rate,eGFR) 70.2 mL/min,血尿免疫固定电泳、自身抗体、血轻链、补体C1q、C3、C4均在正常范围,乙肝、丙肝、梅毒
:蛋白(+++),红细胞(+++)。24 h尿蛋白2.55 g,尿本周蛋白(-)。血生化:白蛋白28 g/L,肌酐75 μmol/L,尿素4.9 mmol/L,尿酸315 μmol/L,肾小球滤过率(estimated glomerular filtration rate,eGFR) 70.2 mL/min,血尿免疫固定电泳、自身抗体、血轻链、补体C1q、C3、C4均在正常范围,乙肝、丙肝、梅毒 、HIV抗体各项阴性。2018年6月行肾活检。
、HIV抗体各项阴性。2018年6月行肾活检。
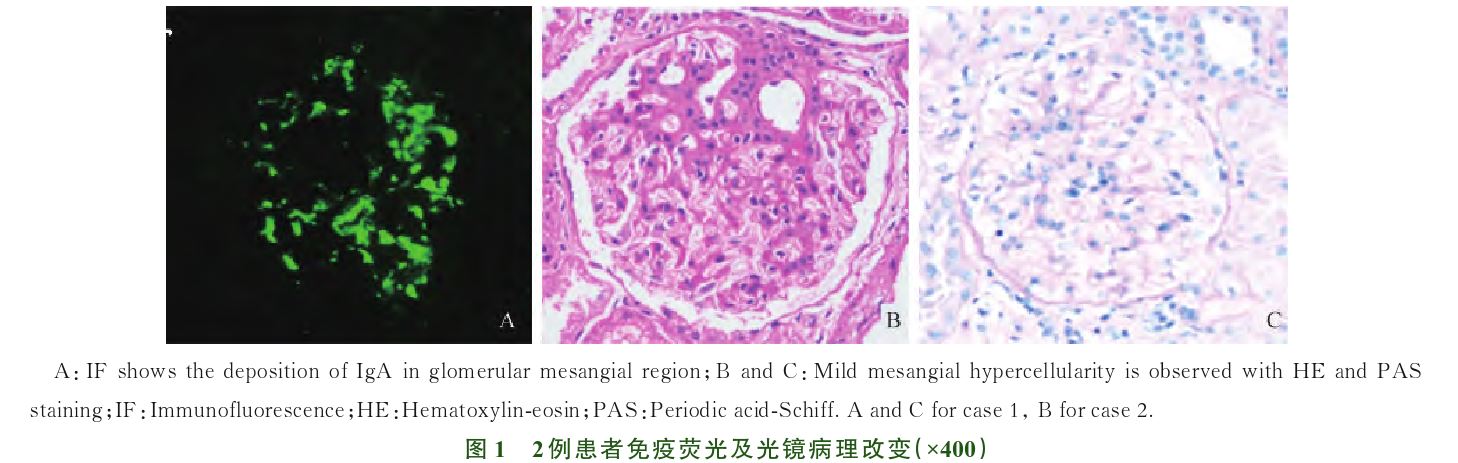
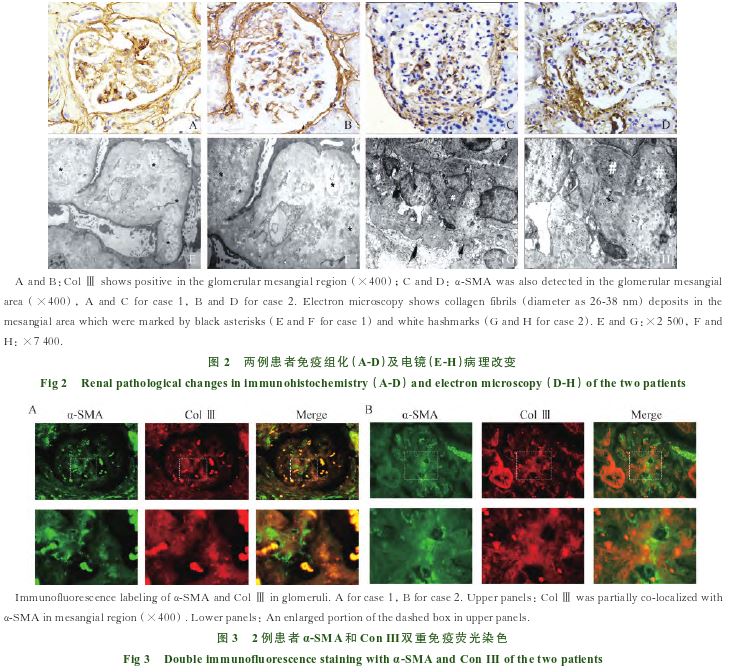
免疫荧光:6个肾小球,IgA(+++)、IgG(+~++)、IgM(+)、C1q(±)、C3(+++)、κ(+)、λ(+++)、 C4(-),阳性染色主要在系膜区呈颗粒或团块样沉积(图1A)。光镜:11个肾小球中3个硬化,其余肾小球个别节段系膜细胞轻度增生伴基质轻度增多(图1C),个别节段与球囊壁黏连;肾小管部分萎缩,部分有蛋白、颗粒或细胞管型,少数小管再生;间质中等量炎症细胞灶性或散在浸润,伴纤维组织轻度增生(10%),个别肾细动脉管壁轻度增厚。电镜:肾小球系膜区明显增宽,部分系膜区有电子致密物沉积伴基质增多,较多系膜区高倍下可见平行排列的纤维丝状结构(图2E、F),上皮足突广泛融合伴部分微绒毛形成。免疫组化:Ⅲ型胶原(Col Ⅲ)及α-平滑肌肌动蛋白(α-smooth muscle actin,α-SMA)显示少部分系膜区呈阳性(图2A、C)。病理诊断:IgA肾病(轻度局灶节段增生型;牛津分型:M0E0S1T0C0)伴系膜区Col Ⅲ沉积。
病例2 患者女性,35岁,因“发现蛋白尿1年余,乏力1周”入院。入院时有泡沫尿,腰酸乏力,无特殊阳性体征。患者既往有高血压病史,血压最高168/120 mmHg (1 mmHg=0.133 kPa,下同),目前服用替米沙坦 、比索洛尔
、比索洛尔 治疗,入院时血压控制在130/80 mmHg。否认糖尿病、慢性肾病等内科疾病病史,否认家族史。尿常规:蛋白(+++),红细胞265个/μL,24 h尿蛋白2.6 g,尿本周蛋白(-)。血生化:白蛋白40.2 g/L,血肌酐58.2 μmol/L,尿素4.78 mmol/L,尿酸335 μmol/L,胱抑素C 0.8 mg/L,eGFR-EPI 114.9 mL/min,总胆固醇6.29 mmol/L,甘油三酯1.2 mmol/L,血糖5.38 mmol/L,糖化血红蛋白
治疗,入院时血压控制在130/80 mmHg。否认糖尿病、慢性肾病等内科疾病病史,否认家族史。尿常规:蛋白(+++),红细胞265个/μL,24 h尿蛋白2.6 g,尿本周蛋白(-)。血生化:白蛋白40.2 g/L,血肌酐58.2 μmol/L,尿素4.78 mmol/L,尿酸335 μmol/L,胱抑素C 0.8 mg/L,eGFR-EPI 114.9 mL/min,总胆固醇6.29 mmol/L,甘油三酯1.2 mmol/L,血糖5.38 mmol/L,糖化血红蛋白 4.8%。其余指标无殊。
4.8%。其余指标无殊。
2018年3月行肾活检。
免疫荧光:5个肾小球,IgA(++)、C3(++)、λ(++),阳性染色在系膜区呈颗粒或团块样沉积;IgG、IgM、C1q、C4、κ(-)。光镜:10个肾小球中2个硬化,其余小球部分节段系膜细胞轻-中度增生,伴基质轻-中度增多(图1B),部分小球与球囊壁黏连,3个节段性硬化灶形成,1个细胞性小新月体形成;肾小管部分萎缩,少量小管有细胞或蛋白管型,少量小管再生;间质中等量炎症细胞小片状及散在浸润,伴纤维组织灶性增生(10%~15%);个别肾细动脉管壁增厚,玻璃样变。电镜:肾小球系膜区中等量电子致密物沉积,较多系膜区中可见排列较整齐的纤维状结构(图2G、H),直径26~38 nm,伴基膜基质中度增生,个别节段重度增生,足突较广泛融合伴部分微绒毛形成。免疫组化:Col Ⅲ及α-SMA染色在系膜区呈阳性(图2B、D)。病理诊断:IgA肾病(局灶节段增生型;牛津分型:M1E0S1T0C1)伴系膜区Col Ⅲ沉积。
双重免疫荧光染色对Col Ⅲ和α-SMA在肾小球内表达的位置进行观察,结果亦显示,两者在系膜区内均有表达,但沉积位置有部分重合(图3)。
治疗与随访
病例1 肾活检后主要予强的松龙(起始剂量30 mg逐渐至1年后停用)联合环磷酰胺 冲击治疗(0.8 g/次,共8次,总计6.4 g),另服用黄葵胶囊
冲击治疗(0.8 g/次,共8次,总计6.4 g),另服用黄葵胶囊 每日3次,每次5粒。随访1年后(2019年6月)24 h尿蛋白转阴并维持。2022年9月复查肾功能:白蛋白40 g/L,肌酐64 μmol/L,尿素5.7 mmol/L,eGFREPI:83.06 mL/min,24 h尿蛋白110 mg/1790 mL。
每日3次,每次5粒。随访1年后(2019年6月)24 h尿蛋白转阴并维持。2022年9月复查肾功能:白蛋白40 g/L,肌酐64 μmol/L,尿素5.7 mmol/L,eGFREPI:83.06 mL/min,24 h尿蛋白110 mg/1790 mL。
病例2 肾活检后查前Ⅲ型胶原肽(PⅢP)5 ng/mL(正常范围0~15 ng/mL)。治疗主要予中药汤剂益气活血补肾(杜仲、黄芪、当归等),并予缬沙坦 降压、降尿蛋白,未用激素或免疫抑制剂。随访8个月余,患者血压控制良好,尿蛋白逐渐下降。2018年11月复查肾功能:肌酐66.6 μmol/L,尿素5.62 mmol/L,eGFR-EPI 102.37 mL/min,24 h尿蛋白609 mg/1 500 mL。
降压、降尿蛋白,未用激素或免疫抑制剂。随访8个月余,患者血压控制良好,尿蛋白逐渐下降。2018年11月复查肾功能:肌酐66.6 μmol/L,尿素5.62 mmol/L,eGFR-EPI 102.37 mL/min,24 h尿蛋白609 mg/1 500 mL。
讨论
作为一种间质胶原,Col Ⅲ通常表达于肾脏间质和血管壁,在正常肾小球中并无分布,但可出现在多种肾小球疾病中。在Col Ⅲ肾病中,大量Col Ⅲ沉积于肾小球系膜区及内皮下区域[1]。甲髌综合征相关肾病则是肾小球Col Ⅲ沉积的又一常见病因[2]。IgA肾病中出现Col Ⅲ沉积的相关病例较为罕见,最早的报道[3]显示,Col Ⅲ可分布在IgA肾病肾小球系膜区、血管极、新月体及硬化小球中。
值得注意的是,尽管在后来的研究发现存在Col Ⅲ肾病合并IgA肾病的情况[4-5],表现在同时发现IgA免疫荧光的阳性及电镜下系膜区的电子致密物沉积,但IgA肾病肾小球内Col Ⅲ的沉积并不同时具备Col Ⅲ肾病的病理特征,且有Col Ⅲ沉积的肾小球数量仅占受检肾小球总数的0.14%~0.25%。此外,还对Col Ⅲ的来源进行了分析,提出了3种可能:(1)系膜细胞合成;(2)间质渗透进入肾小球;(3)血管源性。其中后两种被认为是Col Ⅲ沉积于新月体、硬化小球及肾小球血管极的原因,而系膜区的Col Ⅲ主要来源于系膜细胞的合成。此后,日本学者在1998年又曾报道了1例IgA肾病局灶节段病变伴系膜区Col Ⅲ节段性沉积的病例[6],电镜纤维宽度为23~38 nm,该报道认为Col Ⅲ的出现很可能是系膜细胞表型改变的重要标志。本研究中的2例患者与Col Ⅲ肾病合并IgA肾病不同,而与日本学者的报道类似,即光镜下无Col Ⅲ肾病表现,但每个肾小球中均有Col Ⅲ沉积于系膜区。系膜增生性肾炎的动物实验 亦发现,系膜细胞增生可引发Col Ⅲ在系膜区的沉积,该过程可通过抑制系膜细胞增生得到改善[7]。Col Ⅲ可来源于α-SMA阳性的系膜细胞,后者是一种与系膜细胞活化及细胞外基质的产生密切相关的表型标志[8]。因此,本研究对肾小球中α-SMA的表达也进行了观察,并发现其在部分系膜区呈阳性,而Col Ⅲ在同一系膜区也有沉积,并与α-SMA阳性区域部分重合,从一定程度上证实了Col Ⅲ源于系膜细胞并与α-SMA相关的观点。我们还曾怀疑IgA肾病伴系膜区Col Ⅲ沉积是否会发展成为IgA肾病合并Col Ⅲ肾病。因此我们对1例患者进行了血PⅢP检测。通常,即便是伴有免疫复合物沉积的Col Ⅲ肾病,也会出现血浆PⅢP的显著增高[9-10] ,而本例患者PⅢP检测却处于正常范围。
亦发现,系膜细胞增生可引发Col Ⅲ在系膜区的沉积,该过程可通过抑制系膜细胞增生得到改善[7]。Col Ⅲ可来源于α-SMA阳性的系膜细胞,后者是一种与系膜细胞活化及细胞外基质的产生密切相关的表型标志[8]。因此,本研究对肾小球中α-SMA的表达也进行了观察,并发现其在部分系膜区呈阳性,而Col Ⅲ在同一系膜区也有沉积,并与α-SMA阳性区域部分重合,从一定程度上证实了Col Ⅲ源于系膜细胞并与α-SMA相关的观点。我们还曾怀疑IgA肾病伴系膜区Col Ⅲ沉积是否会发展成为IgA肾病合并Col Ⅲ肾病。因此我们对1例患者进行了血PⅢP检测。通常,即便是伴有免疫复合物沉积的Col Ⅲ肾病,也会出现血浆PⅢP的显著增高[9-10] ,而本例患者PⅢP检测却处于正常范围。
因此,尚无法证实上述系膜区Col Ⅲ沉积与Col Ⅲ肾病在形成机制上存在一定联系。关于IgA肾病伴系膜区Col Ⅲ沉积病例的治疗与预后,目前鲜有报道。曾有研究显示,随着肾小球内Col Ⅲ的增多,IgA肾病患者的肌酐清除率逐渐降低[11] 。与之不同的是,本研究中的2例患者并未因Col Ⅲ的沉积而出现eGFR的显著下降。治疗上我们对2例患者采取了不同的方案。其中病例1主要接受的是免疫抑制治疗,并辅以中成药的治疗。显然,激素与环磷酰胺对系膜细胞增生的抑制作用已得到公认,而黄葵胶囊做为治疗肾小球疾病的常用中成药[12] ,其抑制系膜细胞活化的作用亦在相关研究中得到证实[13] 。该患者治疗1年后尿蛋白转阴,随访4年余未复发。病例2主要接受中药汤剂联合血管紧张素Ⅱ 受体阻断剂(angiotensin Ⅱ receptor blocker,ARB),尽管随访时间较短(8个月余),但患者的尿蛋白已出现明显下降,且肾功能稳定。本例患者的中药处方中包括杜仲、黄芪、当归等药材。有研究发现,杜仲木脂素可抑制系膜区细胞外基质括Col Ⅲ的合成[14],而当归补血汤(黄芪、当归)则可以减少系膜细胞α-SMA的表达[15],上述药物的作用可能是本例患者尿蛋白下降的原因之一。Col Ⅲ肾病治疗难度大,无论ARB或激素联合环磷酰胺[4,16] 疗效均不满意,但本研究中上述两种方案均显示有效。这也从一定程度上说明在形成机制上,IgA肾病合并系膜区Col Ⅲ沉积与Col Ⅲ肾病存在不同。
受体阻断剂(angiotensin Ⅱ receptor blocker,ARB),尽管随访时间较短(8个月余),但患者的尿蛋白已出现明显下降,且肾功能稳定。本例患者的中药处方中包括杜仲、黄芪、当归等药材。有研究发现,杜仲木脂素可抑制系膜区细胞外基质括Col Ⅲ的合成[14],而当归补血汤(黄芪、当归)则可以减少系膜细胞α-SMA的表达[15],上述药物的作用可能是本例患者尿蛋白下降的原因之一。Col Ⅲ肾病治疗难度大,无论ARB或激素联合环磷酰胺[4,16] 疗效均不满意,但本研究中上述两种方案均显示有效。这也从一定程度上说明在形成机制上,IgA肾病合并系膜区Col Ⅲ沉积与Col Ⅲ肾病存在不同。
参考文献略。
来源:黄洁波,蔡小凡,赵仲华,等.IgA肾病伴系膜区Ⅲ型胶原沉积2例[J].复旦学报(医学版),2024,51(03):426-430.
