
伴发副肿瘤性天疱疮、副肿瘤性重症肌无力的纵隔滤泡树突状细胞肉瘤1例
作者:潘红利,侯唯姝,李小虎,吴兴旺,张颖,洪文清 ,余永强,安徽医科大学第一附属医院
,余永强,安徽医科大学第一附属医院
副肿瘤性天疱疮 (paraneoplastic pemphigus,PNP)是与肿瘤并发的一种自身免疫性皮肤黏膜疾病,以血清中存在能识别表皮蛋白成分独特的IgG 自身抗体为特点,以口腔炎、多形性皮损
(paraneoplastic pemphigus,PNP)是与肿瘤并发的一种自身免疫性皮肤黏膜疾病,以血清中存在能识别表皮蛋白成分独特的IgG 自身抗体为特点,以口腔炎、多形性皮损 为主要临床表现。重症肌无力
为主要临床表现。重症肌无力 (myasthenia gravis,MG)是一种自身免疫性疾病,临床上,约15% 的MG属于副肿瘤综合征。
(myasthenia gravis,MG)是一种自身免疫性疾病,临床上,约15% 的MG属于副肿瘤综合征。
滤泡树突状细胞肉瘤 (follicular dendritic cell sarcoma,FDCS)是一类罕见的具有滤泡树突状细胞形态学和免疫表型特征的淋巴造血系统肿瘤。本研究回顾性分析2012 年1 月至2022 年12 月在本院经术后病理证实的2 例FDCS 伴发PNP 和/ 或MG 患者的临床病例资料,旨在探讨该类罕见病的临床、影像、病理特征及治疗方式与预后,从而加深对该病的理解与认识。
(follicular dendritic cell sarcoma,FDCS)是一类罕见的具有滤泡树突状细胞形态学和免疫表型特征的淋巴造血系统肿瘤。本研究回顾性分析2012 年1 月至2022 年12 月在本院经术后病理证实的2 例FDCS 伴发PNP 和/ 或MG 患者的临床病例资料,旨在探讨该类罕见病的临床、影像、病理特征及治疗方式与预后,从而加深对该病的理解与认识。
1.资料与方法
1.1 临床资料
患者1,男,41 岁,双下肢无力半年余,口腔破溃2 个月,呼吸困难 1 周持续加重入院。体检:全身红色或暗红色皮疹
1 周持续加重入院。体检:全身红色或暗红色皮疹 ,散在分布,部分融合成片,高出皮面,压之不褪色,手表面部分皮肤破溃结痂。
,散在分布,部分融合成片,高出皮面,压之不褪色,手表面部分皮肤破溃结痂。
实验室检查:抗桥粒芯蛋白1 抗体滴度检测强阳性,胆碱酯酶 2763 U/ L(4650 ~ 12220 U/ L),乙酰胆碱酯酶受体抗体阳性,新斯的明试验
2763 U/ L(4650 ~ 12220 U/ L),乙酰胆碱酯酶受体抗体阳性,新斯的明试验 阳性,糖类抗原19-972.87 U/ ml( <34 U/ ml),铁蛋白631.4 ng/ ml(30 ~ 400 ng/ml),PCO2 87.8 mmHg,其余实验室检查未见明显异常。临床诊断天疱疮、重症肌无力、Ⅱ型呼吸衰竭
阳性,糖类抗原19-972.87 U/ ml( <34 U/ ml),铁蛋白631.4 ng/ ml(30 ~ 400 ng/ml),PCO2 87.8 mmHg,其余实验室检查未见明显异常。临床诊断天疱疮、重症肌无力、Ⅱ型呼吸衰竭 。由于患者存在严重呼吸衰竭入院后一直内科维持治疗,3 个月后原有症状好转后行胸腔镜下纵隔肿瘤切除术。
。由于患者存在严重呼吸衰竭入院后一直内科维持治疗,3 个月后原有症状好转后行胸腔镜下纵隔肿瘤切除术。
患者2,男,36 岁,胸部不适、压迫感一年余,偶有咳嗽 ,全身皮疹6 月余入院。体检:全身散在红斑、丘疹、水疱等多形性损害。实验室检查:甲状腺球蛋白
,全身皮疹6 月余入院。体检:全身散在红斑、丘疹、水疱等多形性损害。实验室检查:甲状腺球蛋白 138.4 ng/ ml(3.5 ~77.0 ng/ ml),抗桥粒芯蛋白1 抗体滴度检测阳性,余未见明显异常。患者入院后行胸腔镜辅助下右经胸纵隔肿瘤切除术。
138.4 ng/ ml(3.5 ~77.0 ng/ ml),抗桥粒芯蛋白1 抗体滴度检测阳性,余未见明显异常。患者入院后行胸腔镜辅助下右经胸纵隔肿瘤切除术。
1.2 检查方法
采用GE Discovery CT 750 HD 64 排宝石能谱CT 机、GERevolution CT 256 排能谱CT 机,CT 扫描参数:管电压120kV,管电流10 ~25 mAs,扫描层厚5 mm,层间距5 mm,窗宽250 ~400 HU,窗位40 HU。增强扫描采用前臂静脉高压团注非离子型对比剂碘海醇 ,剂量为1.0 ~ 1.5 ml/ kg 体重,后行胸部动态双期扫描,薄层重组层厚1.25 mm,并结合多方位重组技术。
,剂量为1.0 ~ 1.5 ml/ kg 体重,后行胸部动态双期扫描,薄层重组层厚1.25 mm,并结合多方位重组技术。
1.3 病理检查
所有术后标本均经本院病理科4% 中性甲醛液固定、石蜡包埋、切片,行HE 染色和免疫组织化学染色,在光学显微镜下观察。
1.4 图像分析
所有影像资料均采用盲法由一名具有5 年以上及一名具有10 年以上胸部影像诊断经验的影像科医师独立分析,分别记录每例病灶的具体位置、数量、大小、形态、密度、肿块内部及边缘情况,并对肿块的强化方式及强化程度进行分类,意见不一致时经协商达成一致。所有病理切片均由两名病理科医师共同阅片确诊,最后由一名10 年以上胸部病理诊断经验的高年资病理科医师复核后作为最终病理结果。
2.结果
2.1 多层螺旋CT(MSCT)表现
患者1,首次胸部CT 平扫(图1A、B)示:后纵隔偏右侧约平气管隆突下水平见一混杂密度软组织肿块,大小约6.0cm ×4.2 cm,肿瘤实性部分平扫CT 值约45 HU,见散在边缘区分布为主的点状或粗颗粒状钙化,病灶中央见囊变和/ 或低密度坏死区。
间隔约1.5 个月后第二次胸部平扫及增强扫描(图1C、D)示:病灶大小约6.5 cm ×4.4 cm,平扫CT 值约40 HU,病灶中央囊变和/ 或低密度坏死区较前次有所增大,增强肿瘤实性成分明显持续性强化,第一期CT 值约13 2HU、第二期CT 值约120 HU。
再次间隔约1.5 个月后行第三次胸部平扫及增强扫描(图1E、F)示:病灶大小约7.1 cm×4.8 cm,平扫CT 值约35 HU,病灶中央囊变和/ 或低密度坏死区较前次明显增大,增强肿瘤实性成分仍然呈明显持续性强化,第一期CT 值约150 HU、第二期CT 值约143 HU。肿块境界清楚,与周围脂肪间隙尚清晰。
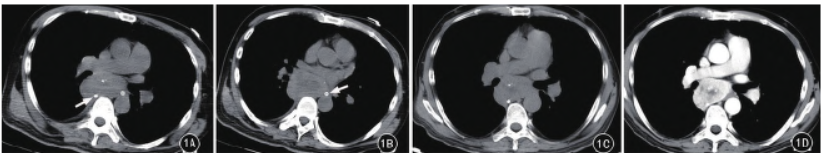
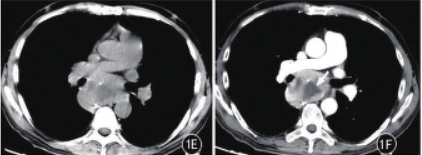
图1A ~ F。 A、B.后纵隔偏右侧约平气管隆突下水平混杂密度软组织肿块,见散在边缘区分布为主的点状或粗颗粒状钙化(白箭),病灶中央见囊变和/或低密度坏死区。C、D.第二次胸部检查病灶中央囊变和/ 或低密度坏死区较前次有所增大,增强肿瘤实性成分明显持续性强化。E、F.第三次胸部检查病灶较前明显增大,病灶中央囊变和/ 或低密度坏死区明显增多(白箭),增强后肿瘤实性成分仍然呈明显持续性强化。肿块境界清楚,与周围脂肪间隙尚清晰
患者2,胸部CT 平扫及增强扫描(图2A ~ E)示:纵隔隆突下偏右侧巨大不规则形软组织密度灶,大小约12.7 cm ×6.8 cm,局部见分支状钙化,肿瘤实性成分平扫CT 值约32HU,增强后中度渐进性强化,第一期CT 值约50 HU、第二期CT 值约64 HU,内见斑片状低密度无强化坏死区。肿块推压右肺下叶支气管,与同层食管分界欠清,食管受压移位、管腔受压狭窄,同时纵隔内见多发肿大淋巴结。
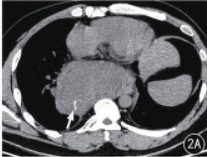
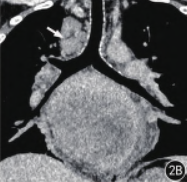
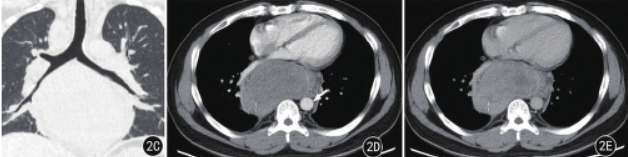
图2A ~ E。 A ~ C.CT 平扫及冠状位重组示纵隔隆突下偏右侧巨大不规则形软组织密度灶,有包膜,局部见分支状钙化(白箭),肿块推压右肺下叶支气管,与同层食管分界欠清,食管受压移位、管腔受压变窄(白箭),纵隔内见多发肿大淋巴结(白箭)。D、E.增强肿块中度渐进性强化,内见斑片状低密度无强化坏死区,包膜可见强化
2.2 病理表现
光镜下HE 表现:肿瘤细胞呈梭形、卵圆形或多边形,呈束状、“旋涡状”排列,胞质嗜酸性,胞界不清(图3A)。免疫组织化学结果:患者1 CD21( + )(图3B)、CD23(少许+ )(图3C)、CD35( + )、CD20(肿瘤细胞极少量)、EMA( + )、Vim( + )(图3D)、CD99( + )、Ki-67(约20%),Bcl-2( + )。患者2 CD21 (部分细胞+ )、CD23 (部分细胞+ )、CD35( + )、CD20(炎细胞+ )、CD117(散在+ )、Vim( + )、Bcl-2( + )。
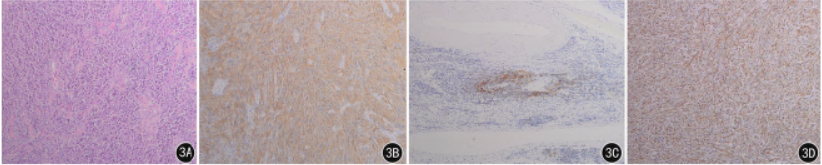
图3A ~ D 患者1 的HE 及免疫组织化学结果。A.HE 染色×50。肿瘤细胞呈梭形、卵圆形或多边形,呈束状、“旋涡状”排列,胞质嗜酸性,胞界不清。B.免疫组织化学SP 法×50。CD21 弥漫阳性,细胞质着棕黄色。C.免疫组织化学SP 法×50。CD23 散在阳性表达,细胞核、细胞质着棕黄色。D.免疫组织化学SP 法×50。波形蛋白(Vim)强阳性表达
3.讨论
3.1 定义、发病机制及临床表现
FDCS 是一种罕见的原发于滤泡树突状细胞的低度恶性肿瘤,1986 年由Monda 等首次报道,提示其具有树突网状细胞起源特征,后续有学者建议至少中度恶性。FDCS好发于成年女性,男女比例为1∶7,本组2 例FDCS 伴发PNP 患者均为男性,与文献报道不符,究其原因可能是样本量太少,亦或是FDCS 伴发PNP 与不伴PNP 的单纯FDCS 好发人群存在差异,这尚待更多的研究报道进行证实。
FDCS的病因尚不完全清楚,大多数患者无明确病因。10% ~20%的患者与先前或并发的Castleman 病相关,主要是透明血管变异型,既可先发生Castleman 病,也可两者同时发生,透明血管型Castleman 病可能通过滤泡树突状细胞(follicular dendritic cell,FDC)增生到不典型增生最后到肿瘤的这样一个发展阶段,增生的FDC 最终发展成肉瘤,提示透明血管型Castleman 病可能是FDCS 的前驱病变。
FDCS 临床表现主要为无痛性缓慢生长的界限清楚的肿块。PNP 是与肿瘤并发的一种自身免疫性大疱性皮肤病,1990 年由Anhalt 首先报道,临床罕见。伴发PNP 的潜在肿瘤主要包括非霍奇金淋巴瘤 、慢性淋巴细胞性白血病
、慢性淋巴细胞性白血病 、Castleman 病,胸腺瘤
、Castleman 病,胸腺瘤 、肉瘤等。皮肤及黏膜损害、糜烂是PNP 最典型的临床表现。副肿瘤性MG 多见于胸腺癌
、肉瘤等。皮肤及黏膜损害、糜烂是PNP 最典型的临床表现。副肿瘤性MG 多见于胸腺癌 ,也可见于乳腺癌
,也可见于乳腺癌 、肺癌
、肺癌 ,霍奇金淋巴瘤,少见于Castleman 病等,特征为肌肉易疲劳,如眼肌无力,吞咽或呼吸困难等。
,霍奇金淋巴瘤,少见于Castleman 病等,特征为肌肉易疲劳,如眼肌无力,吞咽或呼吸困难等。
FDCS 伴发MG 临床罕见,目前国内仅1 例颈部FDCS 伴发MG 的病例报告,国外仅零星几例,其中纵隔2 例。本组1例FDCS 患者同时伴发PNP 及MG 非常罕见。FDCS 形成PNP 的机制是由于FDCS 具有分泌自身抗体的病理学基础,肿瘤的病理性B 细胞能够直接分泌自身抗体,识别皮肤黏膜细胞间的连接蛋白,抗体和相应抗原在表皮等部位结合后引起皮肤黏膜损伤。FDCS 伴发MG的机制尚未明确,文献报道可能是由于对肿瘤源性抗原产生抗体,抗体可能攻击具有相同或相似表位的成分所致。Wang 等报道MG 是PNP 的一种并发症。
3.2 病理学特征
显微镜下FDCS 肿瘤细胞排列呈“巢状”、束状或“旋涡状”,肿瘤细胞呈梭形、卵圆形或多边形,胞质嗜酸性,细胞间胞界不清。胞核呈梭形或卵圆形,核仁不明显或见小核仁,有时可见核内假包涵体,还可出现多核巨细胞,瘤细胞间散在分布小淋巴细胞。FDCS 肿瘤细胞特异性表达一个或多个树突细胞标志,CD21、CD23、CD35。波形蛋白(Vim-entin)也是敏感性较高的抗体,此外上皮膜抗原(EMA)、CD68、S-100、增殖核抗原(Ki-67)等可能阳性。
3.3 影像学特点及鉴别诊断
FDCS 主要发生于淋巴结内,颈部及腋窝淋巴结是最常见发病部位,锁骨上、纵隔、肠系膜等处淋巴结也可发生,本组2 例FDCS 均发生于后纵隔。结外主要见于扁桃体、鼻咽部、肝脏、脾等处,发生于肝脾的FDCS 形态学上与炎性假瘤相似。文献报道FDCS 最大径3.5 ~ 22 cm,本组2 例FDCS 病灶最大径分别为7.1 cm、12.7 cm。FDCS 多为单发,呈圆形或椭圆形,巨大病灶可呈分叶状,多数边界清楚,部分见纤维包膜样结构,对邻近结构产生推挤,少数局部边界不清,可侵犯邻近结构。肿瘤边缘可见多发斑点状、条状或分支状钙化。
肿块实性成分在CT 平扫表现为等或稍低密度,囊变坏死区呈更低密度,出血少见,增强扫描一般呈轻中度不均匀渐进性强化,部分病灶呈明显持续性强化,笔者认为明显强化的FDCS 可能是由透明血管型Castleman 病恶变而来。本组患者1 3 个月内病灶增大,中央囊变坏死区明显增多,原因不明,目前国内外尚未有关于伴发PNP 和MG 的FDCS 短期影像变化的相关报道,因此尚需更多的相关病例报道进行总结分析。
此外,笔者通过查阅国内外文献发现目前已报道的纵隔FDCS 大多数发生于后纵隔,且多见于隆突下偏右侧水平,本组2 例病变均与之相符,因此笔者认为这一特定发病部位对纵隔FDCS 影像诊断有一定提示意义。需与纵隔FDCS 鉴别的常见疾病包括:
(1)神经源性肿瘤:主要是神经鞘瘤,是后纵隔最常见的肿瘤,脊柱旁多见,邻近椎间孔常扩大,病灶可呈“哑铃状”向椎管内延伸,边界多清晰,易囊变、出血,钙化少见,密度及强化程度与肿瘤内Antoni A 和Antoni B 区分布、比例有关,因此增强后可出现不同程度的强化,但以轻-中度强化多见。
(2)淋巴瘤:好发于前、中纵隔,常表现为多发淋巴结肿大,以血管前间隙和气管旁最常见,易融合成块,密度较均匀,囊变、钙化少见,增强呈轻-中度均匀强化,常包绕邻近血管。
(3)食管源性肿瘤:主要是平滑肌瘤和间质瘤,食管源性肿瘤较大时可出现吞咽困难 、胸骨后疼痛等症状。食管间质瘤少见,常发生于下段食管,肿块以腔内生长为主,与食管关系密切,增强后多呈中度到明显强化;食管平滑肌瘤是食管最常见良性肿瘤,多见于食管中段,其次为下段,食管气钡双重造影可见“环形征”、“双边征”,CT 常见肿瘤边缘光滑,密度均匀,偶见钙化,轻中度均匀强化。
、胸骨后疼痛等症状。食管间质瘤少见,常发生于下段食管,肿块以腔内生长为主,与食管关系密切,增强后多呈中度到明显强化;食管平滑肌瘤是食管最常见良性肿瘤,多见于食管中段,其次为下段,食管气钡双重造影可见“环形征”、“双边征”,CT 常见肿瘤边缘光滑,密度均匀,偶见钙化,轻中度均匀强化。
3.4 治疗方式及预后
目前,FDCS 最佳治疗方案仍在摸索当中,目前较为一致的看法是对于局限性病变,手术切除是首选治疗方式,术后可辅以巩固性放疗,以降低局部复发率。对于有远处转移的FDCS 或手术未能根治或术后复发患者,需要进行联合化疗。单纯型FDCS 大多预后良好,但合并PNP 和/ 或MG 的FDCS 的患者大多预后不良,首先是伴发副肿瘤综合征的FDCS 本身就具有较高侵袭性,其次虽手术切除肿瘤后,皮损可完全消退,但黏膜损害顽固,常累及呼吸道,出现闭塞性细支气管炎 ,并导致呼吸衰竭,此外术中接触肿瘤时会导致大量抗体的释放,术后大量残留的抗体仍会促进疾病的进展。
,并导致呼吸衰竭,此外术中接触肿瘤时会导致大量抗体的释放,术后大量残留的抗体仍会促进疾病的进展。
本组患者1 术后2 个月因呼吸困难、肺部感染再次入住我院,对症治疗近两月后患者要求出院,不久后死亡。患者2 术后至今约2 个月,目前整体情况尚可,其长期生存质量、肿瘤是否复发或远处转移有待进一步随访观察。
综上所述,纵隔FDCS 是罕见的低-中度恶性肿瘤,以后纵隔多见,多为单发境界清楚的实性肿块,可有包膜,内可见钙化、囊变、坏死区,出血少见,增强后多为持续性或渐进性强化。伴发PNP、MG 的FDCS 更为罕见,影像医师应该认识的FDCS 与PNP、MG 的内在联系,工作中如遇到PNP 和/ 或MG 患者,同时发现纵隔或其他部位的占位性病变,应考虑到FDCS 的可能。
来源:潘红利,侯唯姝,李小虎等.伴发副肿瘤性天疱疮、副肿瘤性重症肌无力的纵隔滤泡树突状细胞肉瘤MSCT表现及临床病理分析[J].临床放射学杂志,2024,43(02):304-308.
