
症状性非急性期大脑中动脉M2段闭塞血管内再通:附1例报道并文献复习
作者:黄晨阳,刘廷钰,山西医科大学研究生院;朱青峰,山西医科大学第二医院神经外科
大脑中动脉M2段急性闭塞机械取栓治疗的临床效果较好,也得到了指南的推荐。闭塞时间超过24 h的颅内大动脉闭塞称为非急性期闭塞,如果侧支循环代偿不良,可引起严重的神经功能障碍。大脑中动脉M2段非急性期闭塞根据侧支循环代偿的优劣,临床症状表现各异,可出现肢体偏瘫、麻木、失语,或者高级神经功能退化等,严重影响病人的生活质量。其标准的内科治疗主要是双联抗血小板治疗、降血脂、控制高血压 和高血糖
和高血糖 等以及健康生活方式干预等。
等以及健康生活方式干预等。
部分大脑中动脉M2段非急性期闭塞病人经过标准的内科治疗仍然有明显的神经功能障碍,影响病人的生活质量。近年来,随着材料学的发展以及血管内操作技术的进步,症状性非急性期大脑中动脉闭塞血管内再通治疗报道增多,也取得了较好的临床效果,但多是大脑中动脉M1段闭塞的血管内再通治疗。相对血管直径较细的大脑中动脉M2段非急性期闭塞,血管内再通治疗鲜有报道。我们对1例症状性非急性期大脑中动脉M2段闭塞病人采用血管内再通治疗,取得较好的临床效果,现报道如下。
1. 病例资料
65岁男性,因急性脑梗死 溶栓治疗复发1周于2021年4月15日入院。1月前,因左侧肢体偏瘫、语言不流利、反应迟钝在外院行头颅CT检查
溶栓治疗复发1周于2021年4月15日入院。1月前,因左侧肢体偏瘫、语言不流利、反应迟钝在外院行头颅CT检查 示急性脑梗死,给予溶栓治疗,症状缓解,可自主行走。1周前,再次出现左侧肢体无力,肌力明显变差,不能行走,语言不流利,反应迟钝,复查头颅CT示右侧半球新发脑梗死,给予拜阿司匹林
示急性脑梗死,给予溶栓治疗,症状缓解,可自主行走。1周前,再次出现左侧肢体无力,肌力明显变差,不能行走,语言不流利,反应迟钝,复查头颅CT示右侧半球新发脑梗死,给予拜阿司匹林 、氯吡格雷
、氯吡格雷 、瑞舒
、瑞舒 发他汀等药物治疗,症状稍有好转,但仍遗留左侧肢体偏瘫、语言不流利等症状。为求进一步诊治,遂来我院就诊。
发他汀等药物治疗,症状稍有好转,但仍遗留左侧肢体偏瘫、语言不流利等症状。为求进一步诊治,遂来我院就诊。
既往高血压病史13 年余,血压最高达170/105 mmHg,不规律服用降压药物,血压控制结果不详。入院体格检查:血压137/86 mmHg;神志清楚,反应迟钝,言语欠流利;双侧瞳孔等大等圆,直径约2.5 mm,对光反射灵敏;左侧鼻唇沟变浅,伸舌左偏;颈软无抵抗,腹壁反射 可引出,双侧膝腱反射存在,左侧巴氏征阳性,Kernig征、Brudzinski征阴性;左侧肢体肌力0级,感觉减退,肌张力
可引出,双侧膝腱反射存在,左侧巴氏征阳性,Kernig征、Brudzinski征阴性;左侧肢体肌力0级,感觉减退,肌张力 不高;右侧肢体肌力5级,肌张力正常。
不高;右侧肢体肌力5级,肌张力正常。
NIHSS评分18分,mRS评分5分。头颅CT未见脑出血 征象,右侧基底节区、颞叶、侧脑室体旁多发点片状低密度阴影。头颅MRI示右侧大脑半球多发梗死灶。头颅CTA检查示右侧大脑中动脉闭塞。脑灌注成像示右侧大脑半球明显低灌注。全脑血管造影
征象,右侧基底节区、颞叶、侧脑室体旁多发点片状低密度阴影。头颅MRI示右侧大脑半球多发梗死灶。头颅CTA检查示右侧大脑中动脉闭塞。脑灌注成像示右侧大脑半球明显低灌注。全脑血管造影 示右侧大脑中动脉上干、下干闭塞,大脑前动脉软膜支、大脑后动脉软膜支向大脑中动脉供血区域有部分代偿。鉴于病人有较重的神经功能障碍,决定给予右侧大脑中动脉上干(M2段)血管内再通手术。
示右侧大脑中动脉上干、下干闭塞,大脑前动脉软膜支、大脑后动脉软膜支向大脑中动脉供血区域有部分代偿。鉴于病人有较重的神经功能障碍,决定给予右侧大脑中动脉上干(M2段)血管内再通手术。
全麻后,采用Seldinger方法穿刺右侧股动脉,置入8F动脉鞘、90 cm 6F长鞘内套5F单弯造影管,在泥鳅导丝辅助下,使造影管的头端到达右侧颈内动脉起始处,而后沿造影管将长鞘头端带至颈内动脉起始处,撤出造影管,长鞘末端外接肝素 盐水持续冲洗。115 cm 5F extraflex中间导管近端连接Y阀,肝素盐水持续冲洗,在泥鳅导丝辅助下将中间导管引入长鞘内,将中间导管的头端送至右侧大脑中动脉M1段。
盐水持续冲洗。115 cm 5F extraflex中间导管近端连接Y阀,肝素盐水持续冲洗,在泥鳅导丝辅助下将中间导管引入长鞘内,将中间导管的头端送至右侧大脑中动脉M1段。
在路径图下,将SL-10微导管内套3 m长直径0.014 英寸微导丝小心通过M2闭塞处到达闭塞血管远端,撤出微导丝,通过微导管造影确认在闭塞远端血管真腔,通过微导管给路径图,在路径图下,沿微导管导入3 m长Synchro2微导丝到达闭塞血管M3段,撤出微导管,选择直径1.5 mm、长度1 mm NeuroLPSTM球囊,沿微导丝送将球囊送至闭塞段。
整个过程要保证微导丝头端在术者视野之内,避免球囊通过闭塞段时导丝回缩或弹跳至远端刺破分支血管。然后,用压力泵缓慢(40~60 s)加压至4 mmHg,可看到球囊扩张,缓慢泄压(40~60 s)进行扩张成形后造影,发现前向血流部分恢复,扩张处无造影剂外渗,遂更换直径2.0 mm、长度1.5 mm Neuro LPSTM球囊继续对闭塞处扩张,造影显示左侧大脑中动脉上干(M2)完全再通,前向血流维持良好,无残余狭窄及夹层。观察10 min,前向血流维持良好,遂结束手术。
术后立即复查头颅CT未见颅内出血 ,静脉输注替罗非班
,静脉输注替罗非班 24 h 预防急性血栓形成[0.10 μg/(kg·min)。同时控制血压,将病人的血压控制到基础血压的2/3水平,预防过度灌注出血。术后2 d停静脉用替罗非班,继续服用双联抗血小板药物。术后1周复查灌注成像示右侧半球脑灌注明显改善。术后1个月,神志清楚,语言流利,左下肢肌力5级,左上肢肌力3 级,mRS 评分2 分,病人能下地扶拐杖行走。术后3年随访,左下肢肌力5级,左上肢肌力4级,mRS评分1分。
24 h 预防急性血栓形成[0.10 μg/(kg·min)。同时控制血压,将病人的血压控制到基础血压的2/3水平,预防过度灌注出血。术后2 d停静脉用替罗非班,继续服用双联抗血小板药物。术后1周复查灌注成像示右侧半球脑灌注明显改善。术后1个月,神志清楚,语言流利,左下肢肌力5级,左上肢肌力3 级,mRS 评分2 分,病人能下地扶拐杖行走。术后3年随访,左下肢肌力5级,左上肢肌力4级,mRS评分1分。
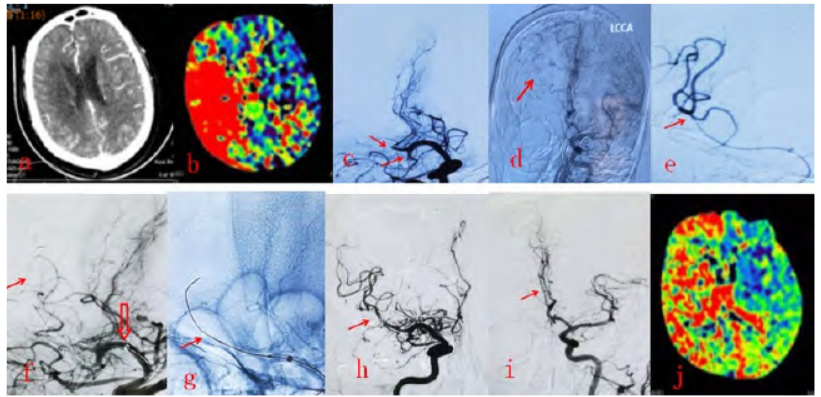
图1 右侧大脑中动脉M2段非急性闭塞血管内再通前后影像。a. 术前头颅CT示右侧基底节区、颞叶、侧脑室体旁多发点片状低密度阴影;b. 术前CT灌注成像显示右侧额颞顶脑灌注不足;c. 术前DSA示右侧大脑中动脉M2段上干、下干闭塞(红色实心↑示);d. 术前DSA显示右侧大脑中动脉负责供血的脑组织主要由大脑前动脉软膜支代偿供血(红色实心↑示);e. 术中DSA显示微导管在微导丝辅助下穿过上干闭塞节段,且微导管在M2远端血管真腔(红色实心↑示);f. 术中DSA显示5F中间导管头端达M1段(红色空心↑示),并将微导丝置于M2闭塞血管远端真腔,然后用1.5 mm×2 cm球囊扩张,然后造影显示闭塞远端血管显影(红色实心↑示),但前向血流维持不佳;g. 术中用2 mm×2 cm球囊扩张;h. 2 mm×2 cm球囊扩张后造影显示大脑中动脉上干显影良好,同时大脑前动脉也显影(红色实心↑示);i. 术后左侧颈内动脉造影显示右侧大脑前动脉显影良好(红色实心↑示);j. 术后1周灌注成像示右侧大脑半球脑灌注明显改善
2. 讨论
文献报道,一些症状性非急性大脑中动脉闭塞病人,即使经过标准的药物治疗,仍然有较重的临床症状或反复脑卒中 发作。对于这一类病人,主要治疗方法有颅内外动脉分流术治疗和血管内再通治疗。对标准内科治疗后仍然存在闭塞血管供血区域低灌注的症状性非急性期大脑中动脉闭塞病人,进行颞浅动脉-大脑中动脉皮层支血管分流术,术后脑灌注明显改善,临床症状减轻,脑卒中复发率明显降低,生活质量提高。
发作。对于这一类病人,主要治疗方法有颅内外动脉分流术治疗和血管内再通治疗。对标准内科治疗后仍然存在闭塞血管供血区域低灌注的症状性非急性期大脑中动脉闭塞病人,进行颞浅动脉-大脑中动脉皮层支血管分流术,术后脑灌注明显改善,临床症状减轻,脑卒中复发率明显降低,生活质量提高。
Mori等对6例症状性非急性大脑中动脉闭塞进行血管内再通治疗,其中闭塞时间在3个月以内的4例血管完全再通,闭塞超过3个月的2例闭塞血管未能再通,无围手术期并发症。近年来,随着介入技术的提高和材料学的进步,血管内再通治疗症状性非急性大脑中动脉闭塞逐渐增多。
黄锐等总结10个临床中心报道的115例症状性非急性大脑中动脉闭塞病人血管内再通治疗的相关资料,闭塞血管再通率高达85%(98/115),3~12个月随访显示,仅7.37%(7/95)的病人出现卒中复发或死亡。
为评估症状性非急性期大脑中动脉血管内再通的难易程度,Gao等将症状性非急性大脑中动脉闭塞脑血管造影分为3型:Ⅰ型,动脉晚期可见软膜支代偿血流逆流至M1远端或分叉处,且闭塞长度≤10 mm;Ⅱ型,动脉晚期软膜支代偿血流逆流至M1远端或分叉处,且闭塞长度>10 mm;Ⅲ型,动脉晚期软膜支代偿血流仅逆流至M2远端,分叉处及M1远端未见血液逆流。研究报道,Ⅰ型血管再通率最高(95.5%),并发症发生率最低(4.5%);Ⅱ型再通率为83.3%,并发症发生率为11.1%;Ⅲ型再通率最低(60%),并发症发生率最高(40%)。
症状性非急性期大脑中动脉闭塞血管内再通技术成功的关键在于微导丝和微导管顺利通过闭塞段到达远端血管真腔,闭塞节段短及血管较粗、平直、远端侧支代偿好能够明显增加血管再通率和降低手术并发症。
另外,术者娴熟的介入操作技巧,能够根据微导丝的走形方向、活动度、阻力大小等综合因素判断是否在血管真腔,也是增加手术成功率和降低并发症的关键。症状性非急性期大脑中动脉M2段闭塞血管内再通治疗之所以报道较少,主要是由于M2段血管管径较细,走形迂曲,血管内再通手术过程中,微导丝走形方向是否正确、是否在血管真腔、是否已经穿透血管壁不好判断,手术风险明显增加。
另外,即使微导丝能够顺利通过闭塞的M2段,达到闭塞远端血管真腔,由于球囊导管较硬,到位有时有困难,或者球囊导管到位时,M2段血管移位,导致M2、M3段的穿支血管受到牵拉移位、甚至断裂,增加了出血风险。在大脑中动脉M2、M3段急性闭塞机械取栓中,多选用适合小管径取栓的支架(比如Aperio支架)或者采用4 mm×2 cm的Solitaire支架半释放进行机械取栓,减少对血管的牵拉,降低穿支撕裂出血的风险。而在症状性非急性期大脑中动脉M2段血管内再通手术时,目前有直径匹配、顺应性、通过性良好的球囊导管。
Neuro LPSTM球囊低压球囊不仅扩张效果良好,而且相对高压球囊来讲,对血管内膜的损伤更小,降低了术后发生夹层、需要补救性置入支架的风险。本文病人血管闭塞部位位于右侧大脑中动脉的上干和下干,闭塞节段属于M2段,上干血管走形相对平直,供应额顶叶等重要功能区域,下干和M1主干成直角发出,迂曲、走形难以判断,且不是供应重要的功能区域,为降低手术风险,综合考量,只对上干进行血管内再通手术。
术中为降低手术操作风险,我们关注了以下几个环节:
一是选择8F股动脉穿刺鞘+6F长鞘+5F中间导管,“塔型支撑”能够使中间导管头端尽可能靠近病变部位,为后续微导管、微导丝通过闭塞处提供有效支撑,也为后续球囊通过闭塞处时提供足够支撑,避免球囊导管通过时微导丝后撤或撤出球囊时微导丝前窜,刺破穿支血管,所以中间导管靠近闭塞处,为微导丝提供有效支撑,增加了微导丝通过闭塞处的几率,降低了出血并发症;
二是根据对侧大脑中动脉M2段的走形方向预估患侧M2段的走形方向,增加手术的安全性,谨防微导丝穿破血管;
三是微导管、微导丝通过闭塞节段时要互相配合,必要时微导管微量、低压造影,进一步为微导丝通过闭塞处提供路径参考;
四是微导管、微导丝通过闭塞处后,一定要微导管造影,证实在闭塞远端血管真腔,交换3 m微导丝到达M3段,再进行后续操作;
五是在整个操作过程中,微导丝远端要在术者视野之内,避免操作过程中微导丝前窜;
六是选择Neuro LPSTM球囊低压球囊,减少对内膜的损伤,同时此款球囊导管为快速交换球囊,简化了操作流程,降低误操作引起手术并发症的风险。
症状性大脑中动脉非急性期闭塞球囊扩张、血管再通成功后,原闭塞处是否需要放置支架,大部分学者认为只要球囊扩张后,没有夹层,前向血流能够维持,残余狭窄<70%,就无需支架置入。Lee等认为,球囊扩张后,残余狭窄的血管上有小动脉分支时,为防止破碎的斑块堵塞穿支动脉开口,支架置入时应谨慎考虑。
本文病人使用2 mm球囊扩张后,没有残余狭窄,前向血流维持良好,就没有使用支架。由于颅内大血管闭塞血管内再通手术的围手术期都存在过度灌注的风险,灌注压突破时发生脑出血,一旦发生脑出血,就要停用抗血小板药物,没有置入支架,就没有停用抗血小板药物后支架内血栓形成的担忧。
本文大脑中动脉M2段闭塞非急性期病人血管内再通手术病人获益和风险的思考:病人虽然为右侧大脑中动脉M2段闭塞,但右侧半球明显低灌注,临床症状较重,左侧肢体肌力0 级,NIHSS 评分18分,mRS评分5分,生活不能自理。如果闭塞的血管能够成功再通,脑灌注改善,病人应该能够获益。最大的风险是术中微导丝穿破血管引起脑出血,应对措施是术中谨慎操作,如果导丝刺破血管,造影剂渗出,则立即用球囊封堵M1段近端血管,必要时可用弹簧圈栓塞出血点。
由于这两项处理措施,不会影响原有的脑侧支循环,所以只要及时止血,没有形成较大的脑内血肿,病人的临床症状不会加重。另外,如果术中微导丝反复尝试难以通过闭塞处,要及时终止手术,下一步可以考虑进行颅内外动脉分流术治疗。
血管内再通术后最严重的并发症是过度灌注脑出血,可严格控制血压、低温、镇静、脱水等对症治疗。本文病例血管再通后立即控制血压(比病人基础血压低10~20 mmHg),持续1周左右,没有出现过度灌注表现。综上所述,本文病例大脑中动脉M2段非急性期闭塞血管内成功再通,术后病人生活质量明显提高。虽然这只是个案,但如果此类病人临床症状较重,充分术前评估后,可以尝试血管内再通治疗。
来源:黄晨阳,刘廷钰,朱青峰.症状性非急性期大脑中动脉M2段闭塞血管内再通:附1例报道并文献复习[J].中国临床神经外科杂志,2024,29(06):341-346.
