
低度恶性肌纤维母细胞肉瘤的影像诊断价值
作者:杨倩,陈楠,余筱瑶,苏佳佳,湖北省肿瘤医院放射科;姚义好,华中科技大学同济医学院附属同济医院放射科
低度恶性肌纤维母细胞肉瘤 (low-grade myofibroblastic-sarcoma,LGMS)是一种罕见的间叶组织源性肿瘤,由肌纤维母细胞分化而来,约占软组织恶性肿瘤的1%。2020 年世界卫生组织(WHO)将其作为一种独立的类型,归入中间性(偶有转移)纤维母细胞/ 肌纤维母细胞肿瘤。
(low-grade myofibroblastic-sarcoma,LGMS)是一种罕见的间叶组织源性肿瘤,由肌纤维母细胞分化而来,约占软组织恶性肿瘤的1%。2020 年世界卫生组织(WHO)将其作为一种独立的类型,归入中间性(偶有转移)纤维母细胞/ 肌纤维母细胞肿瘤。
有关软组织LGMS 的影像学特征的报道较少,且无特异的临床表现,全身各部位均可发病,搜集本院经病理证实的10 例软组织LGMS 的影像资料、病理资料进行回顾性分析,总结其影像学特征,探讨术前影像学检查对其诊断价值,以提高对该病的认识及诊断水平。
1.资料与方法
1.1 一般资料
回顾性分析本院2015 年1 月至2022 年1 月病理确诊为LGMS 的患者10 例;多以逐渐增大肿块就诊,且伴不同程度的疼痛。5 例进行手术切除,5 例穿刺活检。随诊3 个月~6 年。
1.2 检查方法
7 例患者行CT 检查。使用Siemens Somatom DefinitionAS 64 排或GE Revolution CT 64 排螺旋CT 行病变部位扫描,取仰卧位,扫描参数:管电压120 kV,管电流200 mAs,层厚5mm,无间距扫描,重组层厚0.625 mm。均行增强扫描,经高压注射器静脉注射非离子型对比剂碘帕醇 370 mgI/ ml,剂量1 ~2 ml/ kg 体重,注射流率2.5 ~3.0 ml/ s。
370 mgI/ ml,剂量1 ~2 ml/ kg 体重,注射流率2.5 ~3.0 ml/ s。
7 例患者行MRI 检查。使用Siemens Verio 3.0 T 超导MR 扫描仪,采用快速自旋回波序列,行横断面、冠状面及矢状面T2 WI、横断面T1 WI、横断面T2 抑脂序列扫描,矩阵256×256;层厚5 mm,层间隔1.0 mm。均行增强扫描,对比剂为钆喷酸葡胺 (Gd-DTPA),以2.0 ~ 3.0 ml/ s 流率注射0.2mmol/ kg 体重。
(Gd-DTPA),以2.0 ~ 3.0 ml/ s 流率注射0.2mmol/ kg 体重。
1.3 图像分析
从PACS 系统中获取所有患者影像资料,由两位高年资放射科医师同时进行盲法阅片,分析病变部位、大小、形态(圆形、类圆形或不规则形)、边界(是否清晰)、密度/ 信号(是否均匀,是否出血、坏死)、强化特征(强化方式、是否均匀性)、邻近组织器官(是否侵袭、受压)。图像后处理采用多平面三维重组等方法处理。
1.4 手术及病理
手术切除标本或穿刺活检标本均常规固定、石蜡包埋、切片,HE 染色后观察,并进行免疫组织化学检查,包括:波形蛋白(Vimentin)、结蛋白(Desmin)、神经特异性蛋白(S-100)、平滑肌肌动蛋白(SMA)、血管源性物(CD117)、血管源性物(CD34)、细胞增殖标记(Ki-67)等。
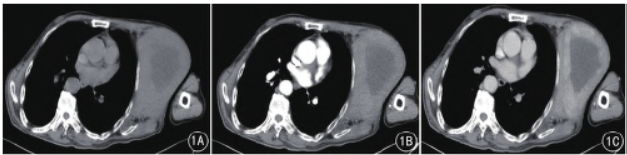
图1A ~ C 男,81 岁,LGMS。A ~ C.分别为CT 平扫、增强扫描动脉期、增强扫描静脉期,左侧胸壁巨大软组织肿块,边界不清,增强扫描病灶周边实性成分可见明显不均匀持续强化,病灶中心见大片状低密度影,增强后未见强化
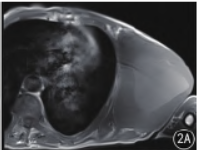
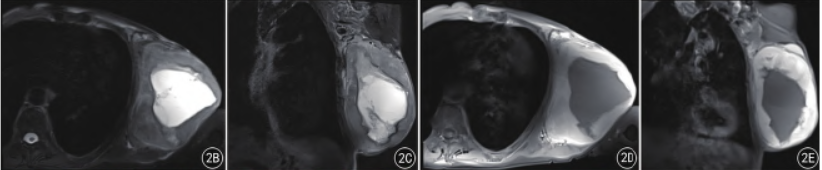
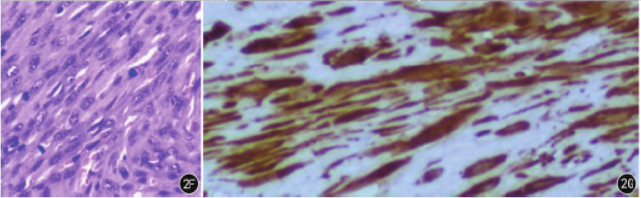
图2A ~ G 与图1 为一病例。A.为T1 WI 轴位平扫:病灶周边呈低信号,中心可见大片状高信号,呈“岛屿状”“溏心鸡蛋”样表现;B、C.为T2 WI 轴位及冠状位平扫:病灶周边呈等高信号,中心可见大片状高信号;D、E.为T1 WI 增强扫描:病灶周边明显强化,即环形强化,中心可见大片状无强化区;F.为肿瘤细胞由异形肌纤维母细胞组成,呈梭形,并呈束状排列(HE ×100);G.desmin 表达阳性,EliVision 法
2.结果
瘤体最大直径52 ~277 mm,平均约79.6 mm。9 例形态不规则,呈分叶状,1 例类圆形。10 例病灶均表现部分边界不清。肿瘤部位:1 例位于舌,3 例位于四肢,2 例位于腹壁,1 例位于腰臀部,胸壁1 例,腹腔2 例。
2.1 CT、MRI 结果
7 例CT 平扫病灶与肌肉密度相比,1 例呈低密度,1 例呈等密度,5 例等低混杂密度,以等低密度为主;CT 增强扫描2 例轻中度强化,5 例明显不均匀强化。7 例MRI 平扫与同层肌肉信号相比,T1 WI 信号不等,3 例呈低信号,4 例病灶中心T1 WI 序列上可见“岛屿状”、“溏心鸡蛋”样高信号,病灶边缘T1 WI 序列上呈低信号; T2 WI 呈混杂信号,病灶中心以高信号为主。
增强扫描8 例病灶边缘均明显不均匀强化,即呈环形强化,病灶中心均可见无强化区;其余2 例呈明显不均匀强化,强化特点无特征性(图1、2)。
2.2 病理结果
所有病例大体观:肿块切面呈灰白或灰红色,局灶质硬,局灶质软,包膜完整,部分包膜不完整,肿瘤多单发,边界不清,呈浸润性生长。镜下可见较多的巨核、多核肌纤维母细胞,瘤细胞异型性明显,呈束状或编织状、“栅栏状”、“流水样”纵横交错排列,瘤细胞胞质红染,核深染,部分细胞核呈空泡状,核染色质粗且不均匀,核分裂象可见,部分细胞疏松区域可见玻璃样及黏液样变性。肿瘤间质见丰富的薄壁血管。免疫组织化学Vimentin ( + )、desmin ( + )、α-actin( + )、SMA ( + )、Ki-67呈低增殖指数。
2.3 随访
所有患者行3 个月~ 6 年随访,随访时间不等,其中2例带瘤生存2 年后死亡,2 例术后复发,3 例带瘤生存,3 例术后无瘤生存。
3.讨论
LGMS 是一种罕见的交界性或低度恶性肿瘤,鲜有报道,其来源于间充质组织,主要由分化程度不同的肌纤维母细胞组成,兼有平滑肌分化和纤维母细胞超微结构特征,是一种少见的间叶源性肿瘤。各年龄均可发病,无明显性别差异,与Montgomery 等的研究一致,但本组主要发病年龄为中老年,且主要为男性,与文献报道一致。LGMS 可累及所有器官,最常见于四肢和头颈部皮下或筋膜下,但多数常位于深部软组织,本组均发生于软组织,与文献报道一致。LGMS 临床表现不明显,无痛性、渐进性生长是软组织LGMS 的一大临床特征,多数肿瘤界限不清楚,肿瘤沿结缔组织间隔呈不规则浸润性生长,可侵入至肌肉或骨骼。
2020 版WHO骨与软组织肿瘤 病理学分类中诊断LGMS 依据有:(1)肿瘤细胞由异形肌纤维母细胞组成,细胞呈梭形并弥漫浸润性生长;肿瘤内富含薄壁毛细血管,浆细胞
病理学分类中诊断LGMS 依据有:(1)肿瘤细胞由异形肌纤维母细胞组成,细胞呈梭形并弥漫浸润性生长;肿瘤内富含薄壁毛细血管,浆细胞 和淋巴细胞不明显;(2)肿瘤细胞呈束状或席纹状排列,间质富于胶原,部分细胞疏松区域可见微囊形成或黏液样变区;少数肿瘤细胞含量少,间质有更明显的胶原成分,并有局灶玻璃样变;(3)肿瘤细胞核至少有局灶性中度非典型性;少数肿瘤推挤边缘组织者周边可见慢性炎细胞环绕;(4)细胞核深染、不规则且增殖活性稍有增加;(5)瘤细胞常弥漫浸润至周围的软组织特别是横纹肌和脂肪;(6)免疫组织化学:Vimentin,α-actin,desmin 不同程度表达,免疫表型为:α-actin + / desmin - ,α-actin + / desmin + ,α-actin+ / desmin - 。
和淋巴细胞不明显;(2)肿瘤细胞呈束状或席纹状排列,间质富于胶原,部分细胞疏松区域可见微囊形成或黏液样变区;少数肿瘤细胞含量少,间质有更明显的胶原成分,并有局灶玻璃样变;(3)肿瘤细胞核至少有局灶性中度非典型性;少数肿瘤推挤边缘组织者周边可见慢性炎细胞环绕;(4)细胞核深染、不规则且增殖活性稍有增加;(5)瘤细胞常弥漫浸润至周围的软组织特别是横纹肌和脂肪;(6)免疫组织化学:Vimentin,α-actin,desmin 不同程度表达,免疫表型为:α-actin + / desmin - ,α-actin + / desmin + ,α-actin+ / desmin - 。
本组病例诊断LGMS 依据:形态学符合LGMS 的诊断标准,且免疫组织化学支持。CT 及MRI 对诊断LGMS 及确定其范围以及与周围组织关系具有重要意义。CT 示肿瘤体积一般较大,与肌肉相比呈等/ 低密度,MRI 平扫与同层肌肉信号相比,肿瘤实性部分T1 WI 均呈低信号,T2 WI 序列信号多变,多呈混杂信号,其典型表现为在T1 WI 序列上肿瘤中心可见大片状信号均匀的高信号,而肿瘤周边部分呈低信号。
简而言之,T1 WI 上肿瘤中心呈高信号,而周边呈低信号,即呈“岛屿状”“溏心鸡蛋”样改变。本组4 例病灶中心可见“岛屿状”“溏心鸡蛋”样高信号,病灶中心以高信号为主,这种现象可能与肿瘤细胞疏松区呈黏液样变性有关,病灶部分区域黏液样变在T1 WI 上呈高信号。而T2 WI 信号多变,可能与肿瘤细胞疏密、黏液变性或/ 和胶原纤维增生程度密切相关。
增强扫描黏液变区不强化,而周边实性部分明显强化,呈“花环状”或“环形”改变,因为肿瘤间质内含有丰富的血管,故增强扫描肿瘤实性成分可见明显强化。这些与马珑等的研究一致,即表现为肿块明显不均匀强化,且以瘤周强化明显,瘤内中心区域未见强化。本组8 例病灶表现为环形强化,剩余2 例增强后表现明显强化。关于LGMS 影像学表现的文献报道有限,但与本组病例基本符合,如肿瘤密度、信号表现等。
本研究病例也可见囊变坏死,可能是肿瘤体积较大,局部肿瘤供血异常导致,囊变坏死并不能认为是LGMS 的特征性表现。有文献报道肿瘤内可见钙化和/ 或出血,本组病例均未见明显钙化和出血,目前尚无相关文献对LGMS 内钙化的病例基础进行报道,由此笔者认为钙化对于该病的诊断无特异性。而肿瘤出血,可能与肿瘤间质内丰富的薄壁血管有关。由于对该肿瘤报道较少,其内出现钙化、出血是否对其影像诊断有一定的提示亟须更多病例的总结。
CT 与MRI可以多方位观察了解病变大小范围、内部结构,了解供血来源,与邻近组织的关系,有助于选择不同的治疗方式。LGMS 临床病程长,具有一定的侵袭性,手术是其主要治疗方法,术后辅以放化疗。然而,该肿瘤有局部复发的倾向,本组2 例复发,复发后的病理学表现和首次病理形态学相似,可能是切除不干净所致。
LGMS 远处转移较罕见,本组均未见转移,但是有2 例带瘤生存2 年后死亡,说明该肿瘤仍具有一定的恶性侵袭性,临床医师应该认真对待。有文献报道多次复发会增加恶性程度,故扩大切除和密切随访以避免复发。LGMS 需要与以下肿瘤鉴别:
(1)炎性肌纤维母细胞瘤:该肿瘤和LGMS 影像学鉴别困难,病理学虽均具有肌成纤维细胞的特性,但是在显微镜下,炎性肌纤维母细胞瘤显示出明显的炎性细胞浸润,而LGMS 则无明显炎症成分背景。
(2)神经鞘瘤:肿瘤中央可见液化、坏死,增强后肿瘤可呈环形不均匀强化,但是肿瘤中央T1 WI 呈低信号,可与之鉴别。
(3)间质瘤:发生腹腔内需与之鉴别,间质瘤易囊变坏死,增强后不均匀强化,与胃肠壁分界不清,而LGMS 增强后表现为周边强化。
综上所述,LGMS 临床罕见,影像学表现仍具有一定特征性,如肿瘤体积一般较大,大多数CT 上显示病灶中心大片状无强化低密度影,T1 WI 平扫上部分肿瘤中心可见大片状高信号,增强扫描大多肿瘤周边呈明显环形强化、瘤内中心区域未见强化。CT、MRI 能清楚显示肿瘤的部位、范围、内部结构及相邻组织关系,但是确诊仍有赖于组织病理学及免疫组织化学检查。
来源:杨倩,陈楠,余筱瑶等.低度恶性肌纤维母细胞肉瘤的影像诊断价值[J].临床放射学杂志,2024,43(02):283-287.
