
多重PCR靶向测序技术检测BRCA1基因假阴性1例报道
作者:蒋圆玲,骆嘉欢,尹欣科等,中山大学孙逸仙纪念医院细胞分子诊断中心
乳腺癌 易感基因(breast cancer susceptibility gene,BRCA)1和BRCA2是遗传性卵巢癌、乳腺癌的易感基因,其胚系突变可导致罹患相关肿瘤的风险显著提高[1] 。由于BRCA1和BRCA2基因编码序列长,传统聚合酶链反应(polymerase chain reaction,PCR)无法完成全部编码序列的检测。高通量测序技术因其检测范围大、通量高等特点,是目前BRCA1和BRCA2基因检测最常用的技术。高通量测序的文库构建方式有多种,其中基于多重PCR的靶向测序技术操作简便、实验周期短,临床应用较广泛。本研究拟对1例多重PCR靶向测序技术检测BRCA1基因假阴性的原因进行分析,旨在提高临床基因检测实验室人员对于不同方法学局限性的警惕,避免漏检的发生,为临床和患者提供更准确、全面的检测信息。
易感基因(breast cancer susceptibility gene,BRCA)1和BRCA2是遗传性卵巢癌、乳腺癌的易感基因,其胚系突变可导致罹患相关肿瘤的风险显著提高[1] 。由于BRCA1和BRCA2基因编码序列长,传统聚合酶链反应(polymerase chain reaction,PCR)无法完成全部编码序列的检测。高通量测序技术因其检测范围大、通量高等特点,是目前BRCA1和BRCA2基因检测最常用的技术。高通量测序的文库构建方式有多种,其中基于多重PCR的靶向测序技术操作简便、实验周期短,临床应用较广泛。本研究拟对1例多重PCR靶向测序技术检测BRCA1基因假阴性的原因进行分析,旨在提高临床基因检测实验室人员对于不同方法学局限性的警惕,避免漏检的发生,为临床和患者提供更准确、全面的检测信息。
1 病例资料
患者,女,26岁,右侧乳腺癌术后复发,至中山大学孙逸仙纪念医院就诊。临床考虑到患者的发病年龄较小,且母亲有卵巢癌病史、姨妈有乳腺癌病史,因此建议进行BRCA1、BRCA2基因变异高通量测序。本研究经中山大学孙逸仙纪念医院伦理委员会批准[【2022】伦申第(27)号],患者签署知情同意书。
2 实验室检测
2.1 外周血DNA提取 采集患者静脉血2 mL,乙二胺四乙酸二钾抗凝。吸取200 μL样本,采用外周血DNA提取试剂盒(货号12219092701X,厦门艾德公司)提取DNA,采用Oubit3.0核酸定量仪(美国Life公司)和QUBIT dsDNA HS Assay试剂盒(货号032856,美国Life公司)对提取的DNA进行质控,以>5 ng·μL-1为合格。
2.2 二代测序(next-generation sequencing,NGS)文库构建采用人类BRCA1基因和BRCA2基因变异检测试剂盒(货号16219111801Z,厦门艾德公司)构建文库。根据试剂盒说明书对提取的DNA进行多重PCR扩增,最后获得终文库,采用Oubit3.0核酸定量仪和QUBIT dsDNA HS Assay试剂盒对其进行质控,以>5 ng·μL-1为合格。
2.3 NGS 每份样本根据终文库浓度和上机所需的数据量计算样本体积,混样后采用MiSeq高通量测序仪(美国Illumina公司)测序,测序数据经生物信息学分析得出相应的变异位点。
2.4 多重链接探针扩增反应(multiplex ligationdependent probe amplification,MLPA)采用3500DX全自动基因分析仪(美国ABI公司)和2720PCR扩增仪(美国ABI公司)以及MLPA P002-D1检测试剂盒(荷兰MRC Holland公司)对BRCA1基因的1a、2、3和5~24个外显子的缺失和重复突变进行检测。MLPA P002-D1试剂盒包含48对不同的探针,其中10对为参照探针。严格按仪器和试剂盒说明书进行操作。
2.5 Sanger测序 针对NGS结果发现的异常区域,在其上、下游设计引物覆盖,进行PCR扩增,并采用Sanger测序进行验证。
3 结果
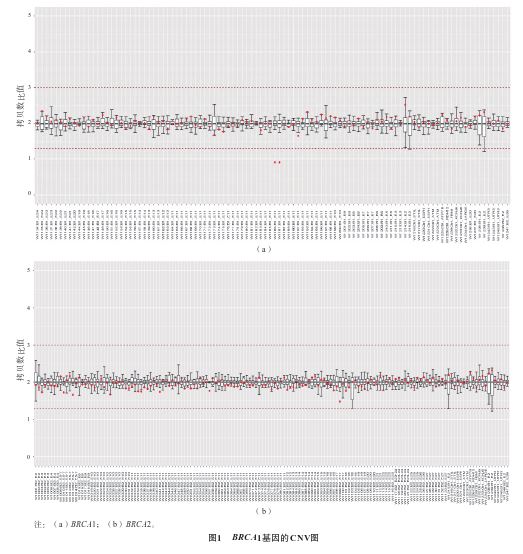
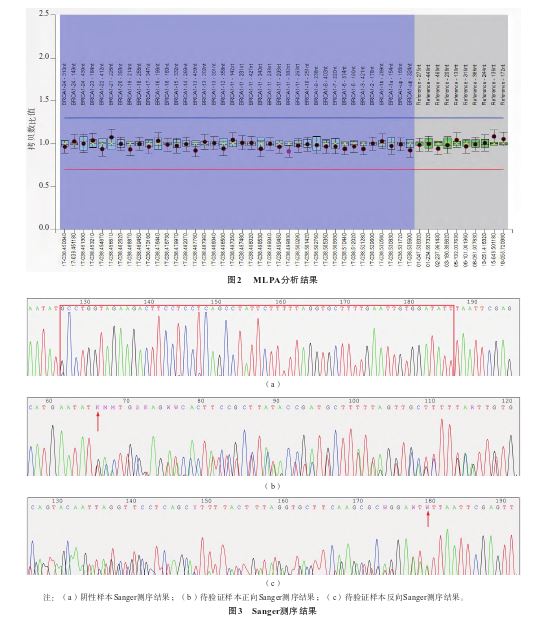
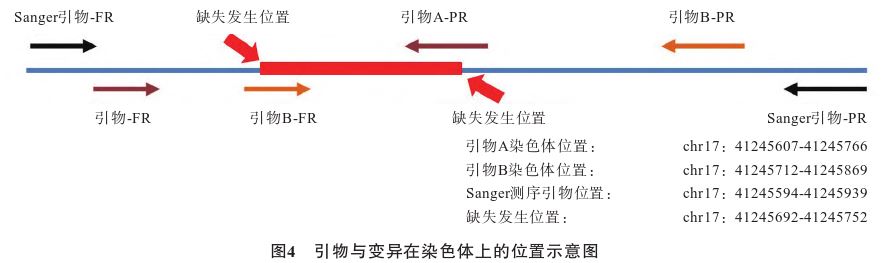
本批次共检测17份样本,其中16份为包含本例患者样本在内的临床标本,1份为阳性对照样本。NGS数据质控合格(Q30>80%,簇通过率>85%),每份样本经生物学信息学分析后各项质控参数均正常。有1份样本经生物信息学分析后未发现BRCA1、BRCA2基因中有意义未明或致病性变异,但在BRCA1基因11号外显子区中有2条相邻的扩增子引物的检测深度明显降低,见图1。采用基因组学可视化工具(integrative genomics viewer,IGV)进行变异可视化,未发现该区域有影响蛋白功能的单核苷酸变异、小片段插入缺失变异等影响蛋白功能的变异。使用MLPA技术对该样本BRCA1基因进行检测,仍为阴性,见图2。设计引物覆盖该测序深度明显降低的区域,Sanger测序验证结果显示,该区域有一个61 bp缺失的变异[NM_007294.3:c.1796_1856del(p.Asn599fs)],见图3。
4 讨论
本研究使用的NGS建库试剂是已获得国家药品监督管理局批准的人类BRCA1基因和B R C A 2基因突变检测试剂盒,其检测范围为BRCA1和BRCA2基因全编码区[包括BRCA1基因(NM_007294.3)外显子2、3、5~24,BRCA2基因(NM_000059.3)外显子2~27]、外显子-内含子连接区(编码序列邻近±20 bp以内)、非翻译区(untranslated region,UTR)和启动子区域的单核苷酸变异、20 bp以内的小片段插入缺失变异。该试剂盒的文库构建方法为多重PCR的靶向富集目的片段,即通过多对引物覆盖上述检测范围,以PCR扩增的方式富集目的片段。本研究在分析数据时发现在整批样本的reads覆盖度较为均一的情况下,有1例样本检测结果为阴性,但在BRCA1基因11号外显子的部分区域发现明显覆盖深度下降。查看该样本分析后的bam文件,未发现在该区域有任何可能影响蛋白功能的变异。在人工审核时发现,与同一批样本相比,在染色体 位置chr17:41245644-41245735的区域,本例患者样本测序深度降低约40%。该区域有2条引物,引物A针对的染色体位置为chr17:41245607-41245766;引物B针对的染色体位置为chr17:41245712-41245869。该结果提示,这2对引物覆盖区域可能存在异常,但是测序未能直接检测出变异。由于扩增子靶向测序方法依赖于PCR扩增目的片段,对于目的区域的富集效果常常受到多重PCR技术本身的影响,如扩增效率一致性问题、非特异性扩增、模版浓度限制、引物与模板结合下降导致的假阴性结果等[2] 。因该项目的检测试剂盒为成熟的商品化试剂盒,已经通过厂商与本实验室的性能验证,且本批次的其他样本并未出现异常,因此排除试剂盒本身性能的影响,结合人工审核观察到的深度变化,推测引起异常的原因为本例患者样本在BRCA1基因11号外显子区域存在变异,影响了引物的结合,导致PCR扩增效率下降,测序深度下降。
位置chr17:41245644-41245735的区域,本例患者样本测序深度降低约40%。该区域有2条引物,引物A针对的染色体位置为chr17:41245607-41245766;引物B针对的染色体位置为chr17:41245712-41245869。该结果提示,这2对引物覆盖区域可能存在异常,但是测序未能直接检测出变异。由于扩增子靶向测序方法依赖于PCR扩增目的片段,对于目的区域的富集效果常常受到多重PCR技术本身的影响,如扩增效率一致性问题、非特异性扩增、模版浓度限制、引物与模板结合下降导致的假阴性结果等[2] 。因该项目的检测试剂盒为成熟的商品化试剂盒,已经通过厂商与本实验室的性能验证,且本批次的其他样本并未出现异常,因此排除试剂盒本身性能的影响,结合人工审核观察到的深度变化,推测引起异常的原因为本例患者样本在BRCA1基因11号外显子区域存在变异,影响了引物的结合,导致PCR扩增效率下降,测序深度下降。
针对上述原因分析,采用以下实验进行验证:1)使用MLPA P002-D1检测试剂盒检测该样本的BRCA1基因;2)根据引物A、引物B在基因组上的位置,设计引物覆盖该2对引物覆盖的基因区域,进行Sanger测序检测。验证实验结果显示:1)MLPA技术检测结果为阴性,未检测出BRCA1基因有外显子缺失或重复;2)Sanger测序结果显示,该样本在17号染色体位置chr17:41245692-41245752区域发生了缺失。
《基于中国人群的BRCA胚系突变筛查专家共识(2024年版)》[3] 指出,对于NGS检测结果提示可能有拷贝数变异,或家族史明确但未测出致病/可能致病变异的个体,建议使用MLPA技术检测大片段重排;同时Sanger测序可用于先证者亲属的变异验证,或者阳性位点的验证。MLPA技术融合了DNA探针杂交和PCR的技术特点,可用于检测拷贝数变异,具有实验样本投入量低、检测范围大、耗时短等优势,不仅能检测基因外显子水平的拷贝数变异,还可以检测整条染色体的数量变化,在杜氏肌营养不良 、脊髓型肌萎缩、肿瘤等领域应用广泛。因此,MLPA技术是BRCA1和BRCA2基因高通量测序检测的重要补充。但MLPA技术对于样本DNA质量要求较高,且不能检测未知区域的变异。Sanger测序技术被视为测序技术的“金标准”,是检测目的DNA片段序列最直接、最常用的方法。Sanger测序技术的准确度高,适用于小通量的样本检测,但其敏感性较低,低于5%突变丰度的变异可能会漏检。因此,MLPA技术和Sanger测序技术是BRCA1基因和BRCA2基因高通量测序检测中非常重要的2种补充检测技术。
、脊髓型肌萎缩、肿瘤等领域应用广泛。因此,MLPA技术是BRCA1和BRCA2基因高通量测序检测的重要补充。但MLPA技术对于样本DNA质量要求较高,且不能检测未知区域的变异。Sanger测序技术被视为测序技术的“金标准”,是检测目的DNA片段序列最直接、最常用的方法。Sanger测序技术的准确度高,适用于小通量的样本检测,但其敏感性较低,低于5%突变丰度的变异可能会漏检。因此,MLPA技术和Sanger测序技术是BRCA1基因和BRCA2基因高通量测序检测中非常重要的2种补充检测技术。
多重PCR是在常规PCR技术的基础上衍生出来的一种技术,可在同一反应体系中加入多对引物,提高检测重数,实现同时对多个目的DNA片段的扩增。1988年,多重PCR技术被首次报道可用于检测杜氏肌营养不良基因座的缺失[4] ,目前该技术已广泛应用于基因检测。与常规PCR技术相比,多重PCR技术具有高效、投入量低、成本低的特点,但其也存在许多局限性,如扩增效率会受检测重数增加的影响;因此,如何平衡多对引物之间的相互影响,保证扩增的一致性、降低引物二聚体对检测结果的影响非常重要[5] 。BRCA1基因位于人类染色体17q21,编码1 863个氨基酸 ;BRCA2基因位于人类染色体13q12,编码3 418个氨基酸,基因变异可分布在基因全长,暂无热点变异[6-7] 。在基于多重PCR技术的BRCA1和BRCA2基因高通量测序检测中,对于BRCA1和BRCA2基因的靶向富集完全依赖于PCR引物的扩增,目的区域PCR引物的设计既影响着目的片段的富集,又影响着目的区域的覆盖。
;BRCA2基因位于人类染色体13q12,编码3 418个氨基酸,基因变异可分布在基因全长,暂无热点变异[6-7] 。在基于多重PCR技术的BRCA1和BRCA2基因高通量测序检测中,对于BRCA1和BRCA2基因的靶向富集完全依赖于PCR引物的扩增,目的区域PCR引物的设计既影响着目的片段的富集,又影响着目的区域的覆盖。
对于本例患者的样本,所用试剂盒在BRCA1基因11号外显子区域共设计了35对引物,该样本在11号外显子区域发生了一段61 bp的缺失,该缺失的区域正好是引物A的下游引物和引物B的上游引物的结合位点(见图4),因此导致这2对引物的目的片段PCR扩增效率下降,最终表现为测序深度降低。但由于该试剂盒基于多重PCR的方式靶向富集目的片段,对于引起目的片段扩增失败的变异无法分析,只能通过各对引物的测序深度变化来提示样本并非阴性结果,若检测人员不清楚相关技术的原理和技术局限性,在样本的各项质控参数都正常的情况下,易将该类异常 忽视。
因此,在高通量测序检测工作中如遇到有相关参数在同一批次样本中出现较大波动时,首先要仔细分析可能出现的原因,不能仅凭其他质控参数合格而忽略异常;其次根据分析的原因制定相应的验证方案,必要时借助其他技术平台进行补充检测。
总之,在临床检测工作中,对于分析结果出现异常的样本,要保持谨慎、细心的态度去分析,可通过其他技术平台来进一步验证存疑的结果。相关检测人员要深入了解技术原理和存在的局限性,从根本上发现问题、理解问题,并解决问题。此外,各项技术都有自身的局限性,在项目检测前要充分告知受检者相应的局限性,做好知情同意的工作;且要规范基因检测报告的内容,详细描述检测技术及其存在的局限性,规范临床基因检测工作的各个 流程。
参考文献略。
来源:检验医学2025年4月第40卷第4期
