
先天性颈部囊性病变的产前MRI与产后CT表现
作者:陈文俊,刘春花 ,杨朝湘等,广东省妇幼保健院放射科
,杨朝湘等,广东省妇幼保健院放射科
先天性颈部囊性病变在产前诊断工作中并不少见,超声具备无创伤性、可应用彩色多普勒观察血流情况等优点,是诊断本类疾病首选的影像学检查方法。但当病灶体积较大时,其较小的图像视野往往无法很好地显示病变的整体情况,此外胎位、孕妇体型及羊水量 等因素对超声软组织分辨率存在明显影响,使得病变的定性诊断以及与邻近结构解剖关系的观察变得困难。与超声相比,MRI不受上述因素的影响,成像视野大,软组织分辨率高,已成为超声检查的有力补充。本研究总结13例先天性颈部囊性病变的产前MRI及产后CT资料,旨在探讨先天性颈部囊性病变的影像学特点,提高诊断及鉴别诊断水平。
等因素对超声软组织分辨率存在明显影响,使得病变的定性诊断以及与邻近结构解剖关系的观察变得困难。与超声相比,MRI不受上述因素的影响,成像视野大,软组织分辨率高,已成为超声检查的有力补充。本研究总结13例先天性颈部囊性病变的产前MRI及产后CT资料,旨在探讨先天性颈部囊性病变的影像学特点,提高诊断及鉴别诊断水平。
1 资料与方法
1.1 研究资料
搜集2013年4月至2024年12月间经出生后手术病理证实的13例胎儿颈部囊性肿块病例资料,均具备产前MRI及产后CT资料。孕妇年龄19~35岁;MRI检查孕周18~36周,出生孕周36~40周。13 例中,包括6例淋巴管瘤,6例先天性梨状窝瘘(congenital pyriform sinus fistula,CPSF)及 1例结肠胰腺异位囊肿。
1.2 仪器与检查方法
9例产前MRI扫描于GE 1.5T MR355 MRI扫描仪进行,使用8通道体部相控阵线圈。扫描序列及参数:(1)快速反转恢复运动抑制(fast inversion recovery motion insensitive,FIRM)序列:TR 9.0 ms,TE 4.2 ms,矩阵320×224;(2)单次激发快速自旋回波(single shot fast spin echo,SSFSE)序列:TR 4000 ms,TE 82.9 ms,矩阵285×256;(3)快速稳态梯度回波(fast imaging employing steady‑state acquisition,FIESTA)序列:TR 4.7 ms,TE 1.8 ms,矩阵160×224;(4)扩散加权成像(diffusion weighted imaging,DWI):TR 2600 ms,TE 84.2 ms,矩阵160×160,b值1000 s/mm2。各序列采用层厚为4.0 mm,层间距为0.0 mm,FOV 48.0 cm× 48.0 cm。
4例产前MRI扫描于Philips 3.0T ingenia MRI扫描仪进行,使用16通道体部相控阵线圈。扫描序列及参数:(1)快速场回波(turbo field echo,TFE)序列:TR 10.0 ms,TE 2.6 ms,矩阵400×400,FOV 36.0 cm× 38.0 cm;(2)快速自旋回波(turbo spin echo,TSE)序列:TR 15000.0 ms,TE 188.0 ms,矩阵560×560,FOV 40.0 cm×52.0 cm;(3)平衡快速场回波(balance‑fast field echo,B‑FFE)序列:TR 3.3 ms,TE 1.7 ms,矩阵432×432,FOV 40.0 cm×35.0 cm;(4)DWI:TR 6824.7 ms,TE 60.4 ms,矩阵384×384,b值1000 s/mm2,FOV 40 cm×34 cm。各序列采用层厚为3.0 mm,层间距为0.0 mm。
CT 检 查:采用 Siemens SOMATOM 128 层MSCT。经静脉采用高压注射器注射非离子型对比剂碘海醇 (300 mgI/ml),注射剂量2 ml/kg,注射流率2 ml/s。扫描参数:管电压100 kV,管电流80 mAs,螺距1,层厚0.6 mm,层间距0.6 mm。采用动脉期、静脉期双期扫描。
(300 mgI/ml),注射剂量2 ml/kg,注射流率2 ml/s。扫描参数:管电压100 kV,管电流80 mAs,螺距1,层厚0.6 mm,层间距0.6 mm。采用动脉期、静脉期双期扫描。
1.3 图像评价
根据手术病理对病变进行分类,由2名有经验的放射科医师共同阅片,分析病变的MRI及CT表现,观察病灶部位、大小、边界、密度/信号,CT增强扫描强化特点及邻近结构改变。意见存在分歧时,经协商达成一致。
2 结果
2.1 淋巴管瘤影像学表现
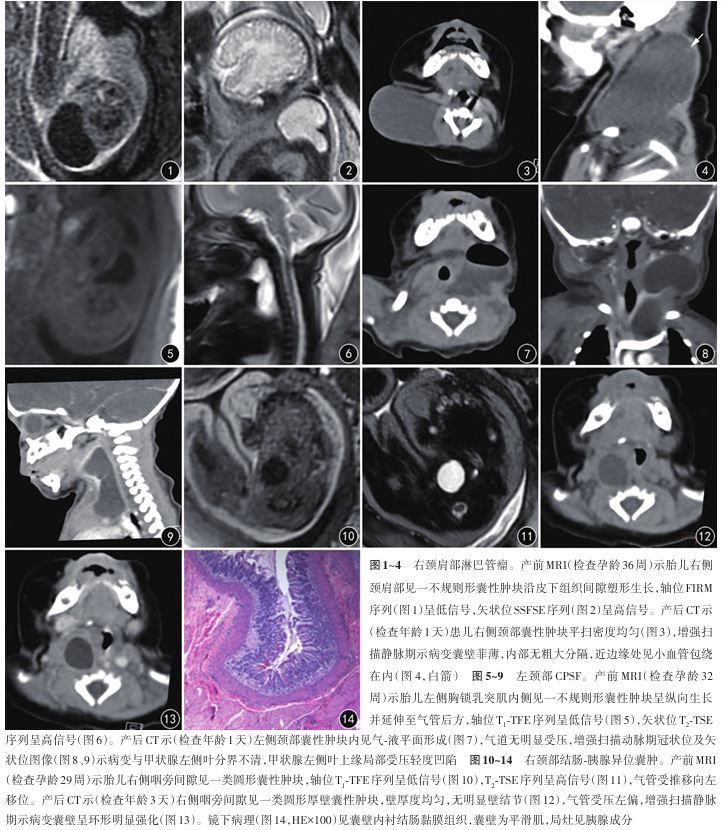
6例淋巴管瘤中,1例位于右侧腮腺间隙并腮腺受压变形;1例位于右侧颈后间隙至肩部;1例位于右侧腮腺间隙至颌下区并腮腺形态不规则改变;1例位于右颈后间隙至同侧胸壁肌肉间隙并甲状腺右侧叶受压变形;1例自左侧颈后间隙、咽后间隙至上纵隔及前上胸壁皮下间隙,左颈总动脉及颈内静脉被包绕在内,颈部气道及气管受压右移,伴右侧少量胸腔积液 ;1例位于右侧颈后间隙至咽后间隙,右侧头长肌部分被包绕在内。6例病灶均沿组织间隙侵袭性生长,形态不规则,产前MRI检查大小约3.7 cm×3.8 cm×3.4 cm~4.8 cm×3.7 cm×7.2 cm,囊内容物T1 WI呈均匀低信号(图1),T2 WI呈均匀高信号(图2),囊内分隔不明显;产后CT检查
;1例位于右侧颈后间隙至咽后间隙,右侧头长肌部分被包绕在内。6例病灶均沿组织间隙侵袭性生长,形态不规则,产前MRI检查大小约3.7 cm×3.8 cm×3.4 cm~4.8 cm×3.7 cm×7.2 cm,囊内容物T1 WI呈均匀低信号(图1),T2 WI呈均匀高信号(图2),囊内分隔不明显;产后CT检查 大小约3.2 cm×2.3 cm×2.7 cm~5.2 cm×3.2 cm×7.5 cm,2例病灶内部可见多发分隔,4例分隔未见明确显示(图3),增强扫描囊壁及内部分隔可见强化,囊内容物未见强化(图4)。
大小约3.2 cm×2.3 cm×2.7 cm~5.2 cm×3.2 cm×7.5 cm,2例病灶内部可见多发分隔,4例分隔未见明确显示(图3),增强扫描囊壁及内部分隔可见强化,囊内容物未见强化(图4)。
2.2 CPSF影像学表现
产前MRI检查可见6例均位于左侧颈前三角区,为胸锁乳突 肌深面不规则形单囊病变,内侧部分形态变薄并延伸至气道后方,大小约1.3 cm× 1.3 cm×2.4 cm~3.2 cm×2.2 cm×3.3 cm,囊壁稍厚,最厚者约0.3 cm,囊内容物信号均匀,T1 WI呈均匀低信号(图5),T2 WI呈均匀高信号(图6)。产后CT表现:6例均与甲状腺左侧叶关系密切,内上缘位于梨
肌深面不规则形单囊病变,内侧部分形态变薄并延伸至气道后方,大小约1.3 cm× 1.3 cm×2.4 cm~3.2 cm×2.2 cm×3.3 cm,囊壁稍厚,最厚者约0.3 cm,囊内容物信号均匀,T1 WI呈均匀低信号(图5),T2 WI呈均匀高信号(图6)。产后CT表现:6例均与甲状腺左侧叶关系密切,内上缘位于梨
状窝后方,并自内向外逐渐膨大气球状,病变大小2.4 cm×1.3 cm×3.7 cm~3.6 cm×2.6 cm×5.0 cm,壁稍厚,囊内见气液平面(图7),增强扫描囊壁及囊内容物未见强化(图8),甲状腺侧叶明显变薄并附着于病变前缘中下部,其中3例见甲状腺侧叶后缘形态不规整(图9)。
2.3 结肠‑胰腺异位囊肿影像学表现
1例结肠‑胰腺异位囊肿位于右侧颈部咽旁间隙内,为类椭圆形单房囊性肿块,推压气管向左前方轻度移位,产前MRI检查病灶大小约2.3 cm×1.7 cm×2.2 cm,囊壁厚约0.2 cm,囊内容物T1 WI呈均匀低信号(图10),T2 WI呈均匀高信号(图11);产后CT检查病变大小约1.7 cm×1.6 cm×2.7 cm,囊壁厚,厚度约0.2 cm,囊内无明显积气(图12),增强扫描囊壁明显环形强化,囊内容物无强化,同水平气道位置轻度左移并管腔变窄(图13)。
3 讨论
在先天性颈部囊性病变产前诊断过程中,不仅需要注意病变的定位及定性,同时需要着重观察气道的受压、移位情况。胎儿气道充满羊水,产前MRI的T2 WI序列表现为管状高信号,与表现为低信号的周边结构之间形成很好的信号对比,通过多平面成像观察可以很好地评估气道狭窄及压迫移位程度,对于分娩 方案的制定,特别是存在气道压迫的胎儿有着重要价值。MRI无辐射损伤,理论上应作为出生后首选的影像学评估手段,但扫描时间较长,对患儿制动及呼吸配合要求较高等不足限制了其出生后检查中的应用。CT扫描速度快,增强扫描利用甲状腺组织对碘剂的吸收作用,使甲状腺轮廓显示更为清晰,可以更好地观察病变与甲状腺的位置关系以及甲状腺的异常改变,目前仍作为该类疾病出生后评估的主要影像检查方法[1]。淋巴管瘤是淋巴管发育异常引起的先天畸形,理论上可发生于任何部位,胎儿及新生儿多见于颈后三角区,病理学分型包括水囊状型、毛细型、海绵状型及血管淋巴管畸形,发生在胎儿者以水囊型占大多数,其形成原因是淋巴管发育异常而无法连接静脉系统导致淋巴回流障碍,使得应正常消退的颈。本研究结果显示淋巴管部透明层不断增厚所致[2]差[3]瘤的产前MRI表现具有沿组织间隙浸润性生长,且可跨越多个间隙分布的特点,病灶内部可有粗大分隔形成,结合囊内容物的信号特点,准确诊断胎儿颈部淋巴管瘤并不困难。淋巴管瘤的产后CT表现有以下特点:(1)病变在浸润性生长的基础上,对组织结构具有一定程度破坏作用,受累及的器官(如腮腺)或肌肉正常形态消失,此征象在产前MRI上多不易显示;(2)病灶内细小分隔显示更为清楚,有研究认为病变内部存在分隔较无分隔者预后更;(3)CT增强扫描可清晰显示病变对受累大血管的侵犯程度,本组1例淋巴管瘤同时累及多个组织间隙(左侧颈后间隙、咽后间隙、上纵隔及前上胸壁皮下间隙),产后CT发现左颈总动脉及颈内静脉被包绕在病变内,手术切除难度大,因此改用引流囊液后注射硬化剂治疗,取得了良好的治疗效果。此外,本组病例中仅1例出现胸腔积液,但未见合并胎儿水肿
方案的制定,特别是存在气道压迫的胎儿有着重要价值。MRI无辐射损伤,理论上应作为出生后首选的影像学评估手段,但扫描时间较长,对患儿制动及呼吸配合要求较高等不足限制了其出生后检查中的应用。CT扫描速度快,增强扫描利用甲状腺组织对碘剂的吸收作用,使甲状腺轮廓显示更为清晰,可以更好地观察病变与甲状腺的位置关系以及甲状腺的异常改变,目前仍作为该类疾病出生后评估的主要影像检查方法[1]。淋巴管瘤是淋巴管发育异常引起的先天畸形,理论上可发生于任何部位,胎儿及新生儿多见于颈后三角区,病理学分型包括水囊状型、毛细型、海绵状型及血管淋巴管畸形,发生在胎儿者以水囊型占大多数,其形成原因是淋巴管发育异常而无法连接静脉系统导致淋巴回流障碍,使得应正常消退的颈。本研究结果显示淋巴管部透明层不断增厚所致[2]差[3]瘤的产前MRI表现具有沿组织间隙浸润性生长,且可跨越多个间隙分布的特点,病灶内部可有粗大分隔形成,结合囊内容物的信号特点,准确诊断胎儿颈部淋巴管瘤并不困难。淋巴管瘤的产后CT表现有以下特点:(1)病变在浸润性生长的基础上,对组织结构具有一定程度破坏作用,受累及的器官(如腮腺)或肌肉正常形态消失,此征象在产前MRI上多不易显示;(2)病灶内细小分隔显示更为清楚,有研究认为病变内部存在分隔较无分隔者预后更;(3)CT增强扫描可清晰显示病变对受累大血管的侵犯程度,本组1例淋巴管瘤同时累及多个组织间隙(左侧颈后间隙、咽后间隙、上纵隔及前上胸壁皮下间隙),产后CT发现左颈总动脉及颈内静脉被包绕在病变内,手术切除难度大,因此改用引流囊液后注射硬化剂治疗,取得了良好的治疗效果。此外,本组病例中仅1例出现胸腔积液,但未见合并胎儿水肿 的相关病例,可能与病例数不多有关,也可能是本组病例发现时间均为中晚孕期(孕24~36周),相对于早孕期发现者而言,合并染色体
的相关病例,可能与病例数不多有关,也可能是本组病例发现时间均为中晚孕期(孕24~36周),相对于早孕期发现者而言,合并染色体 及其他结构发育异常的几率下降,预后相对较好[4]。CPSF为第三或第四鳃弓或咽囊发育异常所形成的,系内瘘口位于梨状窝并走行于同侧甲状腺侧叶间的异常瘘管结构。Liston[5]最早就CPSF的理论走行进行描述,并一直被沿用至今,但其观点认为CPSF 并无穿行于甲状腺内部的节段,无法解析CPSF继发的甲状腺炎
及其他结构发育异常的几率下降,预后相对较好[4]。CPSF为第三或第四鳃弓或咽囊发育异常所形成的,系内瘘口位于梨状窝并走行于同侧甲状腺侧叶间的异常瘘管结构。Liston[5]最早就CPSF的理论走行进行描述,并一直被沿用至今,但其观点认为CPSF 并无穿行于甲状腺内部的节段,无法解析CPSF继发的甲状腺炎 而逐渐受到其他学者的质疑。2018年国内学者宫喜翔等[6]回顾分析90例CPSF的精细解剖,首次阐述了瘘管真实走行路径以及与毗邻结构的关系,自内上至外下将瘘管细分为甲状软骨翼板后内段、甲状软骨下角段、甲状腺腺体内段及甲状腺外下段,其研究结果明确了CPSF与甲状腺的关系,为解释甲状腺炎的形成原因提供了解剖学支持。CPSF按形态可分为囊肿型、窦道型及瘘管型,发生于胎儿或新生儿者为囊肿型,实际上为开口于梨状窝的一端膨大的窦道。在胚胎发育过程中,由于双侧第四鳃弓发育不对称,导致绝大多数CPSF发生于左侧[7,8]。因此,当产前MRI发现胎儿左侧颈前三角区胸锁乳突肌深面的单房囊性肿块,且内侧部分形态变薄并指向气管后方时,要考虑到 CPSF的可能。既往研究[9~11]对于新生儿CPSF的CT特征描述多强调病灶内气体的出现,但病变引起的甲状腺形态改变往往少有涉及。从本研究病例可见,CPSF病灶与甲状腺左侧叶的关系并非单纯外压推移,甲状腺左侧叶正常形态消失、变薄,两者分界模糊,且部分病例出现甲状腺后缘局部轮廓可不规整,此征象提示甲状腺腺体受到破坏,也证实了CPSF存在甲状腺腺体内走行节段,为本病诊断提供了另一有价值的参考依据。胃肠道上皮异位囊肿可发生于口腔至直肠的任何部位,多见于十二指肠、胆囊、胆总管、默克尔憩室
而逐渐受到其他学者的质疑。2018年国内学者宫喜翔等[6]回顾分析90例CPSF的精细解剖,首次阐述了瘘管真实走行路径以及与毗邻结构的关系,自内上至外下将瘘管细分为甲状软骨翼板后内段、甲状软骨下角段、甲状腺腺体内段及甲状腺外下段,其研究结果明确了CPSF与甲状腺的关系,为解释甲状腺炎的形成原因提供了解剖学支持。CPSF按形态可分为囊肿型、窦道型及瘘管型,发生于胎儿或新生儿者为囊肿型,实际上为开口于梨状窝的一端膨大的窦道。在胚胎发育过程中,由于双侧第四鳃弓发育不对称,导致绝大多数CPSF发生于左侧[7,8]。因此,当产前MRI发现胎儿左侧颈前三角区胸锁乳突肌深面的单房囊性肿块,且内侧部分形态变薄并指向气管后方时,要考虑到 CPSF的可能。既往研究[9~11]对于新生儿CPSF的CT特征描述多强调病灶内气体的出现,但病变引起的甲状腺形态改变往往少有涉及。从本研究病例可见,CPSF病灶与甲状腺左侧叶的关系并非单纯外压推移,甲状腺左侧叶正常形态消失、变薄,两者分界模糊,且部分病例出现甲状腺后缘局部轮廓可不规整,此征象提示甲状腺腺体受到破坏,也证实了CPSF存在甲状腺腺体内走行节段,为本病诊断提供了另一有价值的参考依据。胃肠道上皮异位囊肿可发生于口腔至直肠的任何部位,多见于十二指肠、胆囊、胆总管、默克尔憩室 、回肠、阑尾、结肠、直肠[12,13]。目前确切病因仍不清楚,有学者认为可能是异位未分化的内胚层细。有研究在胃及直肠重复畸形发现胞岛所引起[14]异位的胰腺组织[15,16],推测其形成原因可能与胰腺细胞错位进入胃肠道系统有关[17],也有观点认为可能是胰腺原基穿透胃肠壁,随肠管生长而异常种植[18]。本组1例结肠‑胰腺异位囊肿存在明显增厚的囊壁,与发生于其他部位的胃肠道重复畸形影像学表现相似,该征象在本研究其他囊性病变中很少出现,也是最主要的鉴别依据。由于本例缺乏胰腺组织,产前MRI及产后CT检查很难识别异位胰腺的存在,最终诊断仅依靠病理结果确定(图14)。综上所述,淋巴管瘤、CPSF及结肠‑胰腺异位囊肿的产前MRI及产后CT表现具有一定特征性。产前MRI的价值更多在于对病变定位定性的同时,观察气道的受压程度,协助产时及出生后处理方案的初步制定。产后CT能更好显示病变的详细特征,通过增强扫描观察病变的血供以及与周围结构(尤其是大血管、甲状腺)关系,为后续治疗提供有价值的参考意见。
、回肠、阑尾、结肠、直肠[12,13]。目前确切病因仍不清楚,有学者认为可能是异位未分化的内胚层细。有研究在胃及直肠重复畸形发现胞岛所引起[14]异位的胰腺组织[15,16],推测其形成原因可能与胰腺细胞错位进入胃肠道系统有关[17],也有观点认为可能是胰腺原基穿透胃肠壁,随肠管生长而异常种植[18]。本组1例结肠‑胰腺异位囊肿存在明显增厚的囊壁,与发生于其他部位的胃肠道重复畸形影像学表现相似,该征象在本研究其他囊性病变中很少出现,也是最主要的鉴别依据。由于本例缺乏胰腺组织,产前MRI及产后CT检查很难识别异位胰腺的存在,最终诊断仅依靠病理结果确定(图14)。综上所述,淋巴管瘤、CPSF及结肠‑胰腺异位囊肿的产前MRI及产后CT表现具有一定特征性。产前MRI的价值更多在于对病变定位定性的同时,观察气道的受压程度,协助产时及出生后处理方案的初步制定。产后CT能更好显示病变的详细特征,通过增强扫描观察病变的血供以及与周围结构(尤其是大血管、甲状腺)关系,为后续治疗提供有价值的参考意见。
参考文献
来源:临床放射学杂志2025年第44卷第8期
