
2019 ASCO 速递 | 高明教授: RET 抑制剂 BLU-667 有望“精准制导” RET 变异晚期甲状腺癌
2019年5月31日-6月4日,全球肿瘤领域的饕鬄盛会——美国临床肿瘤学会(ASCO)年会在芝加哥隆重召开。会上公布了 ARROW 研究(NCT03037385)中 BLU-667 治疗 RET 突变甲状腺癌 的进一步研究结果。结果显示, BLU-667 具有强效、持久和广泛的抗肿瘤活性,在甲状腺髓样癌(MTC)和甲状腺乳头状癌(PTC)患者中具有良好的耐受性,无论患者是否对酪氨酸激酶抑制剂(TKI)耐药,均可显著改善 RET 变异甲状腺癌患者的预后。医脉通第一时间邀请了天津医科大学肿瘤医院副院长、中国抗癌协会头颈肿瘤专业委员会主任委员高明教授对该研究进行点评。
的进一步研究结果。结果显示, BLU-667 具有强效、持久和广泛的抗肿瘤活性,在甲状腺髓样癌(MTC)和甲状腺乳头状癌(PTC)患者中具有良好的耐受性,无论患者是否对酪氨酸激酶抑制剂(TKI)耐药,均可显著改善 RET 变异甲状腺癌患者的预后。医脉通第一时间邀请了天津医科大学肿瘤医院副院长、中国抗癌协会头颈肿瘤专业委员会主任委员高明教授对该研究进行点评。

甲状腺癌是内分泌系统最常见的恶性肿瘤,其组织学及形态学分型包括乳头状癌(PTC)、滤泡状癌(FTC)、未分化甲状腺癌(ATC)和来源于滤泡旁C细胞的髓样癌(MTC)。 MTC 具有强浸润性、易发生淋巴结、远处转移、复发及预后差的特点,在确诊为 MTC 的患者中超过 70% 发生淋巴结转移和 10%-15% 发生远处转移1。受体酪氨酸激酶转染重排基因(RET)的异常激活是导致多种实体肿瘤生长和增殖的关键驱动因子。在约 10% 的 PTC 患者以及约 60% 的 MTC 患者中观察到 RET 变异。大约 90% 的不可手术或转移的 MTC 患者中发现 RET 变异。目前全球尚无选择性的 RET 抑制剂上市2。
研究概述
BLU-667 是由 Blueprint Medicines Corporation 公司开发一种口服、强效、高选择性的靶向致癌性 RET 变异的小分子抑制剂。临床前研究结果显示, BLU-667 对 RET 融合(包括 KIF5B-RET 和 CCDC6-RET 融合类型)以及 RET 激活突变(如 C634W、M918T、V804L/M )敏感,且对 VEGFR-2 抑制作用轻微。此外,在多达 371 个激酶的检测中, BLU-667 对 RET 的选择性较 96% 的激酶高出 100 倍,与已批准的多激酶抑制剂相比也有显著提高3。
ARROW 研究(NCT03037385)是 BLU-667 治疗进展期 RET 阳性患者的一项全球性的 Ⅰ 期临床试验,针对 RET 基因变异的非小细胞肺癌 (NSCLC)、MTC 和其他晚期实体瘤。试验目的包括总体缓解率、缓解持续时间、药代动力学、药效学和安全性。本次 ASCO 会议上,研究者更新了 ARROW 研究中 BLU-677 治疗 RET 突变阳性甲状腺癌患者进一步的研究结果2。
(NSCLC)、MTC 和其他晚期实体瘤。试验目的包括总体缓解率、缓解持续时间、药代动力学、药效学和安全性。本次 ASCO 会议上,研究者更新了 ARROW 研究中 BLU-677 治疗 RET 突变阳性甲状腺癌患者进一步的研究结果2。
截至 2018 年 12 月 19 日, 60 名 RET 突变 MTC 患者( 37 名 M918T,8 名C634R/S/W ,4 名 V804M, 11 名其他/待定)和 5 名 RET 融合 PTC 患者( 3 名 NCOA4 , 2 名 CCDC6 )接受 BLU-667 治疗( 37 名参加剂量递增部分研究, 28 名参加剂量扩展部分研究)。 58% 的患者先前接受过酪氨酸激酶抑制剂(TKI)的治疗。
在 49 名可评估的 MTC 患者中,客观缓解率(ORR)为 47% (95% CI=33%-62%),其中 2 例 CR , 21 例 PR , 4 例 PR 患者等待确认, 25 例 SD , 1 例 PD 。 96% 的有响应的患者(22/23)仍在治疗中,其中 15 例患者持续响应时间 ≥ 6 个月。 50% (2/4)的可评估 PTC 患者达到了 PR 。 5 名招募的 PTC 患者持续治疗时间为 8-11 个月。 MTC 患者的疾病控制率(DCR)高达 98% 。同时观察到 RET 变异体在血浆中被快速清除, CEA 和降钙素 显著降低。
显著降低。
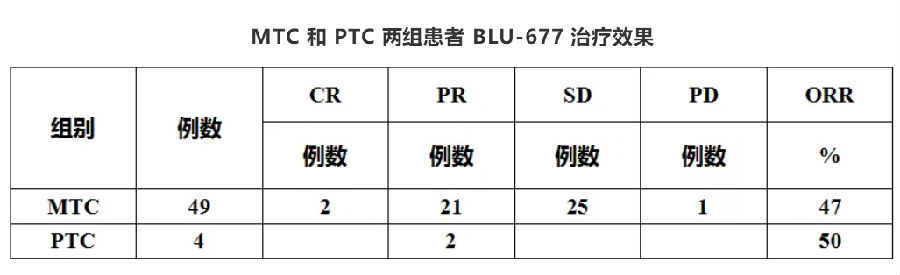
MTC 和 PTC 两组患者 BLU-677 治疗效果
此外, BLU-677 治疗 MTC 患者的响应率与 TKI 是否耐药或 RET 基因类型无关。在先前使用过卡博替尼/凡德他尼的 MTC 患者中, BLU-677 治疗的 ORR 仍高达46% (12/26), 2/3 可评估的 V804M 突变患者达到了 PR 。
安全性方面, BLU-677 治疗的相关毒性一般较低且可逆( 3 级 AEs 为 28% ,无 4/5 级 AEs ,无导致停药的 AEs ),其中包括白细胞下降(23%), AST 升高(17%), ALT 升高(15%),血肌酐和磷酸盐升高,高血压以及中性粒细胞减少(均为 15%)2。
上述结果表明, BLU-667 具有强效、持久和广泛的抗肿瘤活性,在 RET 变异晚期甲状腺髓样癌和甲状腺乳头状癌患者中具有良好的耐受性,无论患者是否对多激酶抑制剂耐药,均可显著改善RET变异晚期甲状腺癌患者的预后。
专家点评
甲状腺癌是我国高发的恶性肿瘤, 2015 年我国新发甲状腺癌患者约 20.1 万,发病率为 14.6/10 万4。其中,甲状腺髓样癌约占甲状腺恶性肿瘤的 4%~8% 。大量研究已确认 RET 变异是 MTC 发病的主要分子病因学基础,大约 90% 的不可手术或转移的 MTC 患者中发现 RET 变异,临床治疗中这类患者并不少见。
目前全球尚无选择性的 RET 抑制剂上市,临床上对于晚期不可切除或转移 MTC 的治疗方案主要是使用酪氨酸激酶抑制剂(TKI),如卡博替尼( cabozantinib )、凡德他尼( vandetanib )5。 TKI 的特点是对多个激酶靶点产生作用,最值得注意的是受体酪氨酸激酶 VEGFR-2 ,它能调节血管生成和血管内皮的通透性。但通过药物抑制 VEGFR-2 活性可能导致临床相关的由药物剂量限定的毒性,例如高血压,血栓形成和出血3。
去年 AACR 会议报道的 ARROW 研究初步结果显示, BLU-667 是一种有高度潜力的选择性 RET 抑制剂6。今年 ASCO 会议上, ARROW 研究的进一步更新结果显示, BLU-667 在 RET 变异的甲状腺癌患者(包括酪氨酸激酶抑制剂治疗失败的患者)中耐受性良好,同时表现出有前景的临床活性。基于令人鼓舞的 I 期临床试验数据,美国食品药品监督管理局(FDA)已授予 BLU-667 突破性疗法认定,用于治疗 RET 突变阳性的 MTC 。
据悉,基石药业 2018 年 6 月已和 Blueprint Medicines 达成独家合作,正在全力推进 BLU-667 在我国的临床研发。 2019 年 3 月 18 日,中国国家药品监督管理局(NMPA)已经批准了 RET 抑制剂 BLU-667 在中国的 I 期临床试验。我们期待 BLU-667 在中国的临床研发取得理想的结果,能尽早将这一候选药物带给中国患者。
参考文献
1. Moley JF et al. Medullary thyroid carcinoma: management of lymph node metastases[J].Natl Compr Canc Netw,2010:8(5):549-556.
2. Taylor M H, Gainor J F, Hu MIN,et al. Activity and tolerability of BLU-667, a highly potent and selective RET inhibitor, in patients with advanced RET-altered thyroid cancers. ASCO 2019,Abstract 6018.
3. Subbiah V , Gainor J F , Rahal R , et al. Precision Targeted Therapy With BLU-667 for RET-Driven Cancers[J]. Cancer Discovery, 2018:CD-18-0338.
4. 郑荣寿, 孙可欣, 张思维, et al. 2015年中国恶性肿瘤流行情况分析[J]. 中华肿瘤杂志, 2019, 41(1):19-28.
5. NCCN Guidelines Version 1.2019 Thyroid Carcinoma
6. Subbiah V, Taylor M, Lin J,et al. Highly potent and selective RET inhibitor, BLU-667, achieves proof of concept in a phase I study of advanced, RET-altered solid tumors.AACR 2018, Abstract CT043.
专题聚焦>>>2019年美国临床肿瘤学会年会(ASCO)

