
郭军教授:“洋为中用”,更要“中为洋用”——“恶黑”能否继续引领免疫治疗
恶性黑色素瘤(恶黑)是实体瘤免疫治疗的“Leading Tumor”,因为恶黑是全球首个抗CTLA-4和抗PD-1类药物获批治疗的恶性肿瘤,也是PD-1从晚期后线治疗向晚期一线,以及术后辅助治疗和围手术期治疗挺进最快的实体瘤。
在中国,为什么“恶黑”也是Leading Tumor
同样在国内,恶黑也是免疫治疗的“Leading Tumor", 不仅因为这是全球应用广泛的 PD-1 免疫检查点抑制剂帕博利珠单抗 在中国的首个获批适应症治疗的瘤种,也不仅因为《CSCO黑色素瘤诊疗指南》是CSCO推出的第一本指南,更是因为早在2019年,恶黑免疫治疗就诞生了引领全球的中国研究。
在中国的首个获批适应症治疗的瘤种,也不仅因为《CSCO黑色素瘤诊疗指南》是CSCO推出的第一本指南,更是因为早在2019年,恶黑免疫治疗就诞生了引领全球的中国研究。
2019年《临床肿瘤学杂志》(Journal of Clinical Oncology)在线发表由北京大学肿瘤医院郭军教授团队开展的PD-1联合阿昔替尼 一线治疗晚期黏膜黑色素瘤的Ib期研究结果。结果显示,联合治疗方案的客观缓解率(ORR)达48.3%,疾病控制率(DCR)达86.2%,远超以往治疗方案ORR不到20%的表现¹。
一线治疗晚期黏膜黑色素瘤的Ib期研究结果。结果显示,联合治疗方案的客观缓解率(ORR)达48.3%,疾病控制率(DCR)达86.2%,远超以往治疗方案ORR不到20%的表现¹。
这个研究推动了黑色素瘤的免疫治疗,彻底改变了黏膜黑色素瘤的治疗理念,让中国成为该领域的引领者。2019年,《CSCO黑色素瘤诊疗指南》就将肢端型及黏膜型黑色素瘤单独成章,且分别给出治疗建议,这是全球首创。而美国NCCN指南目前仅设立皮肤和眼黑色素瘤两个亚型,尚未加入肢端和黏膜亚型。
郭军教授在接受本平台采访时指出,外国专家十余年前曾调侃说中国对黑色素瘤诊疗发展的贡献是零,这个时代已一去不复返;当前,多数肢端型及黏膜型黑色素瘤的创新治疗方案已基本来自中国。
所以,“恶黑”有资格被称为国内免疫治疗的Leading Tumor,不仅因为它聚焦中国特色亚型,更因为国内专家能大胆创新治疗方案,革新治疗理念,并改变临床实践。
恶黑术后辅助,探寻亚洲特色之路
在今年ASCO大会上,郭军教授团队主导的一项探索替莫唑胺 联合顺铂
联合顺铂 化疗对比PD-1抑制剂用于黏膜黑色素瘤的辅助治疗疗效和安全性临床研究登上了口头报告舞台。结果显示,无论是无复发转移生存(RFS), 无远处转移生存(DMFS)还是总生存(OS),相较于免疫单药治疗,化疗在黏膜黑色素瘤的辅助治疗中均存在更优的临床获益²。
化疗对比PD-1抑制剂用于黏膜黑色素瘤的辅助治疗疗效和安全性临床研究登上了口头报告舞台。结果显示,无论是无复发转移生存(RFS), 无远处转移生存(DMFS)还是总生存(OS),相较于免疫单药治疗,化疗在黏膜黑色素瘤的辅助治疗中均存在更优的临床获益²。
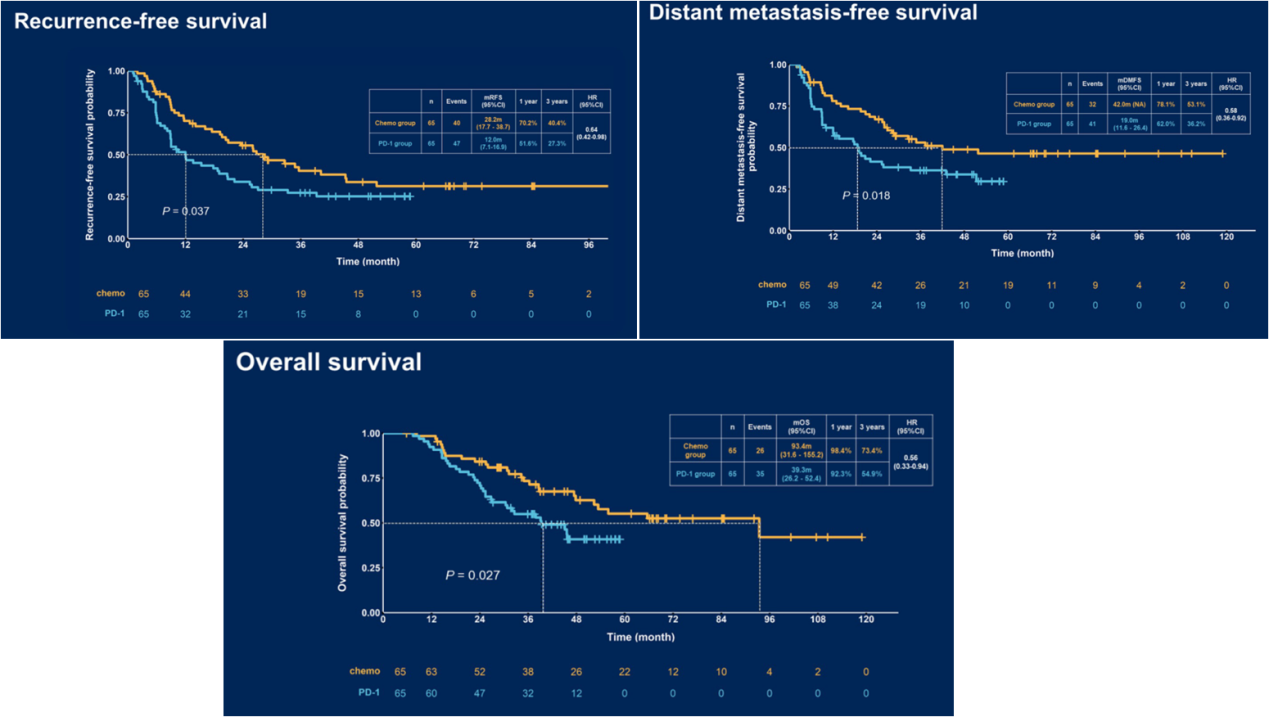
这是一个出乎欧美专家意料之外的研究结果。
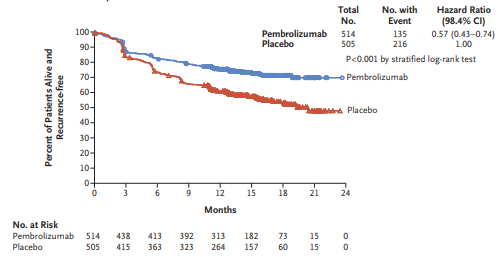
早在2018年,《新英格兰医学》就刊登了帕博利珠单抗用于高危复发的可切除III期皮肤黑色素瘤 患者术后辅助治疗的III期临床研究KEYNOTE-054,结果显示,相比安慰剂对照组,术后帕博利珠单抗辅助治疗可降低43%复发或死亡风险³。
患者术后辅助治疗的III期临床研究KEYNOTE-054,结果显示,相比安慰剂对照组,术后帕博利珠单抗辅助治疗可降低43%复发或死亡风险³。
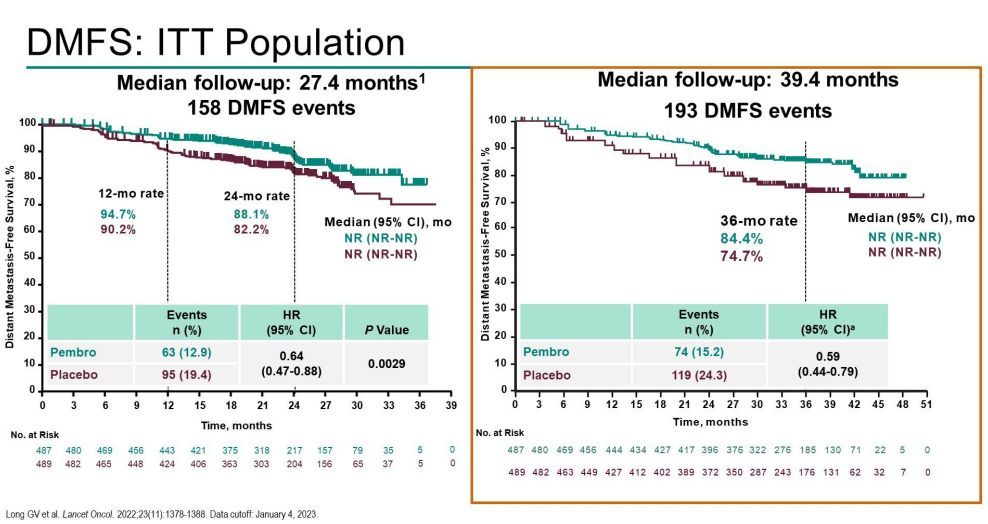
本次ASCO大会也公布了首个评估ⅡB和ⅡC期皮肤黑色素瘤辅助治疗的Ⅲ期临床研究KEYNOTE-716的更新DMFS数据结果。结果显示,中位随访39.4个月时,相比安慰剂对照组,帕博利珠单抗术后辅助治疗组可降低41%远端转移或死亡风险⁴。
郭军教授认为,在免疫治疗已在欧美国家可切除恶黑术后辅助标准治疗的今天,中国专家要保持清醒头脑,不能盲目跟风。
“往往当某一种治疗模式成为热点,我们就认为它可以战无不胜,在任何场景下都可以应用;但其实还是要因人而异,因病制宜。”
中国“恶黑”能否持续引领?
今年3月,《新英格兰医学》刊登了帕博利珠单抗新辅助(3个周期)+术后帕博利珠单抗辅助治疗(15个周期)的“三明治”围手术期治疗模式对比帕博利珠单抗单药术后辅助治疗(18个周期),用于可手术切除的IIIB-IVC期皮肤黑色素瘤的疗效和安全性II期临床研究结果。

结果显示,“三明治”模式相比单纯术后免疫辅助治疗可降低无事件发生风险,24个月的无事件生存期(EFS)提升了23%,达到72%⁵。
相比KEYNOTE-054和KEYNOTE-716的单纯术后免疫治疗模式,“三明治”模式可能是一种针对具有高危复发风险可切除皮肤黑色素瘤的创新治疗模式。
对于PD-1单药辅助治疗疗效并不尽人意的可手术切除粘膜黑色素瘤,是否也有属于自己的“三明治”治疗模式呢?
在今年ASCO, 来自郭军教授的团队也汇报了单臂、开放标签、II期研究NeoPlus的分析结果,该研究对仑伐替尼 联合帕博利珠单抗应用于可切除黏膜黑色素瘤新辅助治疗疗效和安全性进行了评估。
联合帕博利珠单抗应用于可切除黏膜黑色素瘤新辅助治疗疗效和安全性进行了评估。
患者首先接受2个周期的仑伐替尼联合帕博利珠单抗治疗,随后接受手术,并在术后继续接受15个周期的帕博利珠单抗治疗。结果显示,在15例接受手术切除的患者中,2例患者实现病理完全缓解(pCR),1例患者评估为主要病理缓解(MPR),3例获得部分病理缓解(pPR),总体病理学缓解率为40%⁶。
郭军教授认为,这个研究结果非常令人振奋,研究获得了非常高的pCR和pPR率, 对于中国最常见的黏膜黑色素瘤来说,这是非常重要的一个研究。
“我们知道黏膜黑色素瘤多发于鼻腔、口腔、食道、阴道、直肠这些部位,而对这些部位尤其是面部的黑色素瘤的手术可能造成生活质量下降。而如果新辅助治疗能够带来肿瘤明显的降期,甚至让部分患者免于手术,那就可以让这些患者得到巨大获益。”
显然,从晚期到早期恶黑治疗,中国在黏膜和肢端恶黑的免疫治疗中走出自己的道路,但同时,也必须时刻关注欧美皮肤黑色素瘤治疗模式的演变和进展。
在今年3月的AACR大会上,KEYNOTE-942研究结果首次显示帕博利珠单抗联合mRNA疫苗治疗完全切除后复发风险较高的IIIB-IV期皮肤黑色素瘤患者,与帕博利珠单抗标准治疗相比,可降低44%的复发或死亡风险⁷。
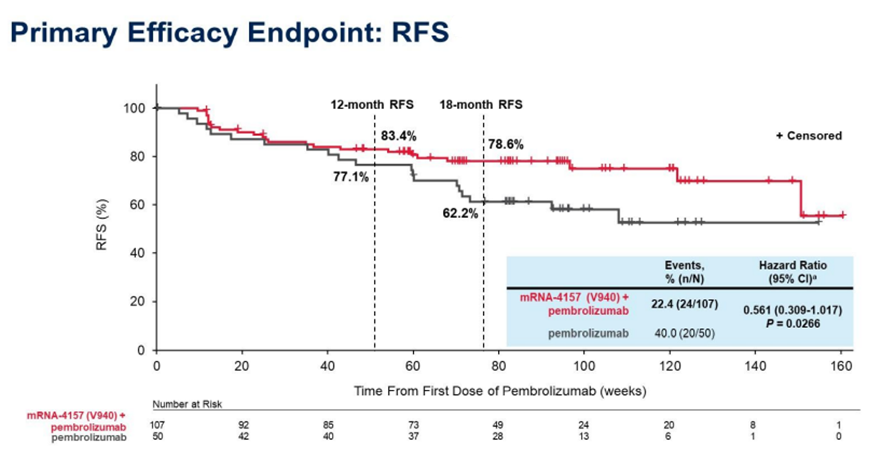
今年ASCO大会上也公布了该研究的无远端转移生存的数据,联合治疗可降低65%的远端转移或死亡风险⁸。
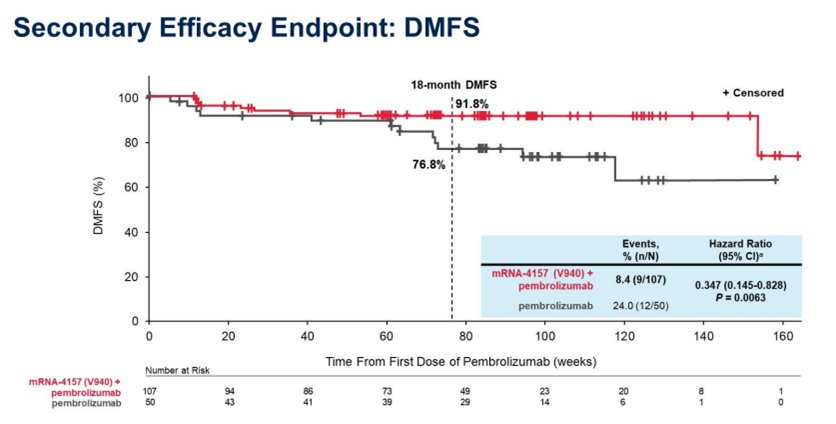
郭军教授认为,KEYNOTE-942是一个非常成功的临床研究,也为黑色素瘤的免疫辅助治疗增加了一个可期待的创新模式。但是这种模式对于中国的粘膜和肢端恶黑会有同样惊艳的疗效吗?
“在KEYNOTE-942研究中,mRNA疫苗被用于辅助治疗,这时肿瘤已经完全被切除,因此肿瘤抗原是缺乏的;而通过mRNA疫苗来提供肿瘤抗原,刺激免疫反应,同时通过PD-1来增强获得性的抗肿瘤免疫,理论上讲是应该比单药PD-1辅助治疗更有效。但是,这种模式用于免疫新辅助治疗的必要性可能就没有那么强,因为在手术前并不缺乏具有免疫原性的肿瘤抗原。”
同时,郭军教授预测,mRNA疫苗应用于黏膜恶黑治疗的挑战可能来源于是否能研发出有效的疫苗。
“皮肤黑色素瘤具有很强的免疫原性,所以也容易找到新抗原用于mRNA疫苗研发。但是,粘膜黑色素瘤肿瘤新抗原相对更缺乏。”
显然,中国恶黑继续引领未来之路怎么走,还需要中国临床研究者继续探索,不模仿,不内卷,走出一条适合东亚黏膜和肢端黑色素瘤治疗的自主创新之路,再次为世界的黑色素瘤创新治疗做出贡献。
