
2023 WCLC丨MET异常NSCLC临床研究百家争鸣,赛沃替尼一线数据脱颖而出!
前言
间质-上皮细胞转化因子(MET)是继表皮生长因子受体(EGFR)、间变性淋巴瘤激酶(ALK)以及c-ros原癌基因1(ROS1)后,人们发现的非小细胞肺癌 (NSCLC)诊疗领域又一重要驱动基因与治疗靶点。2023年9月9日-12日,由国际肺癌研究协会(IASLC)举办的2023世界肺癌大会(WCLC)顺利召开。作为全球最大的致力于肺癌和其他胸部恶性肿瘤的学术会议,2023 WCLC报道了多项MET异常NSCLC临床诊疗前沿研究。医脉通特邀北京协和医院张力教授为此次WCLC中报道的MET异常NSCLC最新进展进行盘点并分享其个人学术见解与观点。
(NSCLC)诊疗领域又一重要驱动基因与治疗靶点。2023年9月9日-12日,由国际肺癌研究协会(IASLC)举办的2023世界肺癌大会(WCLC)顺利召开。作为全球最大的致力于肺癌和其他胸部恶性肿瘤的学术会议,2023 WCLC报道了多项MET异常NSCLC临床诊疗前沿研究。医脉通特邀北京协和医院张力教授为此次WCLC中报道的MET异常NSCLC最新进展进行盘点并分享其个人学术见解与观点。
百花齐放
多项MET异常NSCLC临床研究亮相WCLC
随着NSCLC靶向治疗的不断发展,MET异常NSCLC逐渐受到越来越多的肿瘤临床工作者与患者的广泛关注。张力教授指出,此次WCLC中报道的MET异常NSCLC最新进展主要集中于MET ex14跳突与MET扩增NSCLC领域。针对MET扩增NSCLC,INSIGHT2研究数据(表1)提示,Tepotinib联合奥希替尼 治疗一线奥希替尼耐药后经组织FISH确认存在MET扩增NSCLC可有效改善患者生存时长与生活质量,且亚裔患者获益更为明显¹。
治疗一线奥希替尼耐药后经组织FISH确认存在MET扩增NSCLC可有效改善患者生存时长与生活质量,且亚裔患者获益更为明显¹。
在MET ex14跳突NSCLC领域,此次WCLC报道了颇多研究(表2-4)。张力教授表示,CHRYSALIS研究最新结果、VISION研究亚裔患者长期随访结果以及一项Tepotinib治疗MET ex14跳突或扩增实体瘤Ⅱ期研究中NSCLC患者疗效数据均在此次WCLC得到了公布²-⁴。通过相关研究数据可以看出,无论是MET酪氨酸激酶抑制剂(TKI)或是大分子单抗均可为患者带来较高的缓解率以及较长的生存时长,且初治患者的疗效获益往往优于经治患者,这提示临床医生一个常被提及的用药理念——好药先用,因此未来应考虑将靶向治疗应用到患者的一线治疗中,张力教授强调。
表1-4 2023 WCLC MET异常NSCLC相关研究数据汇总¹-⁴
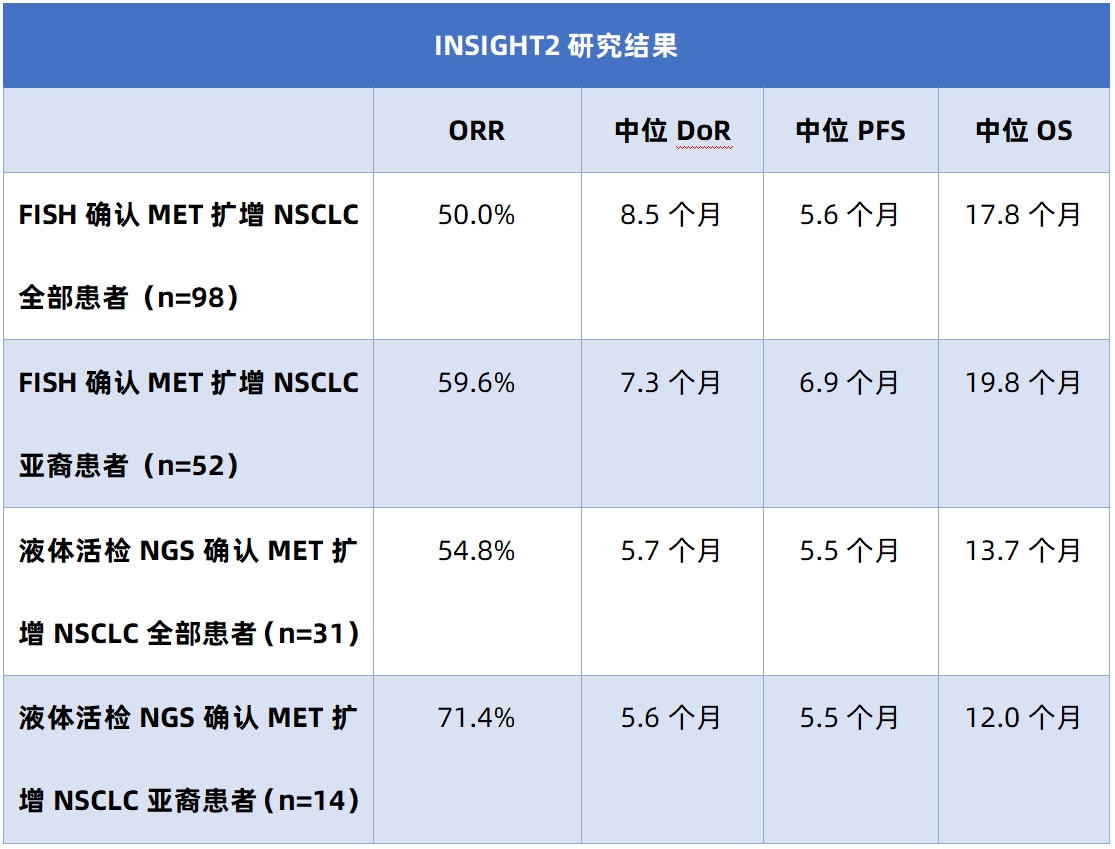
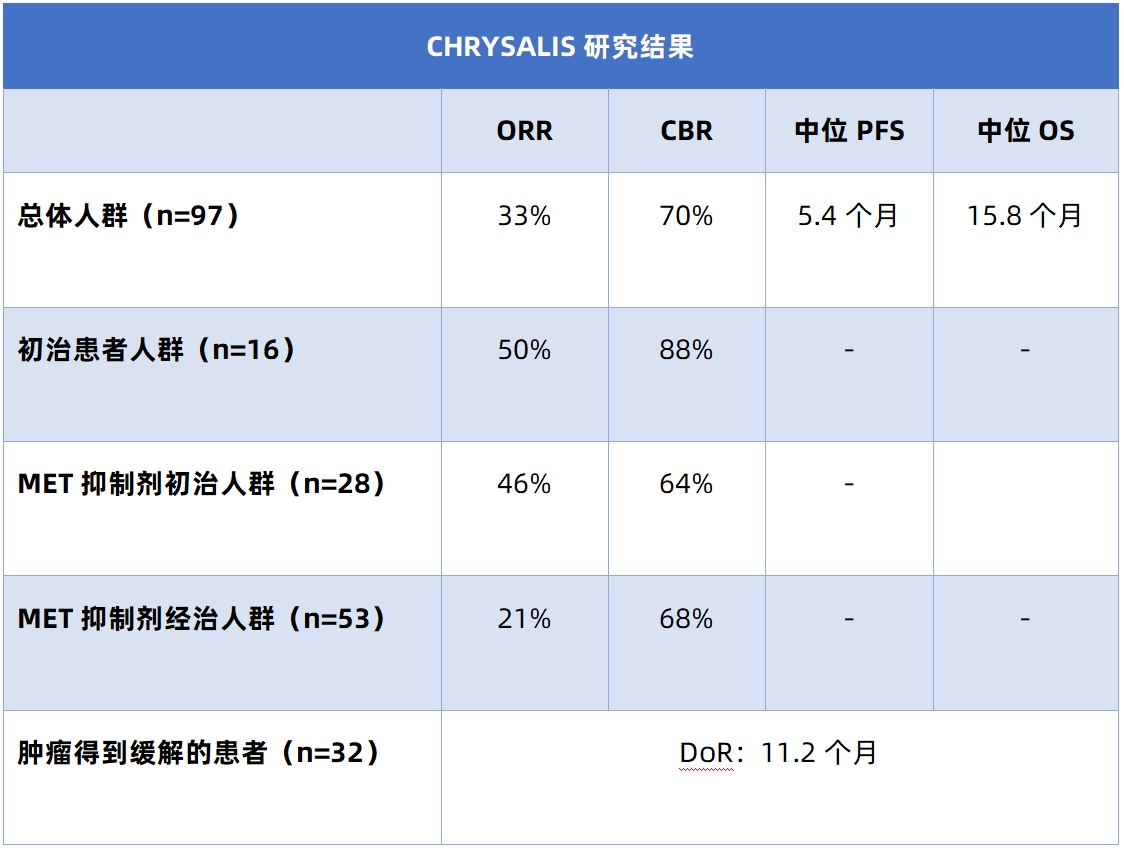
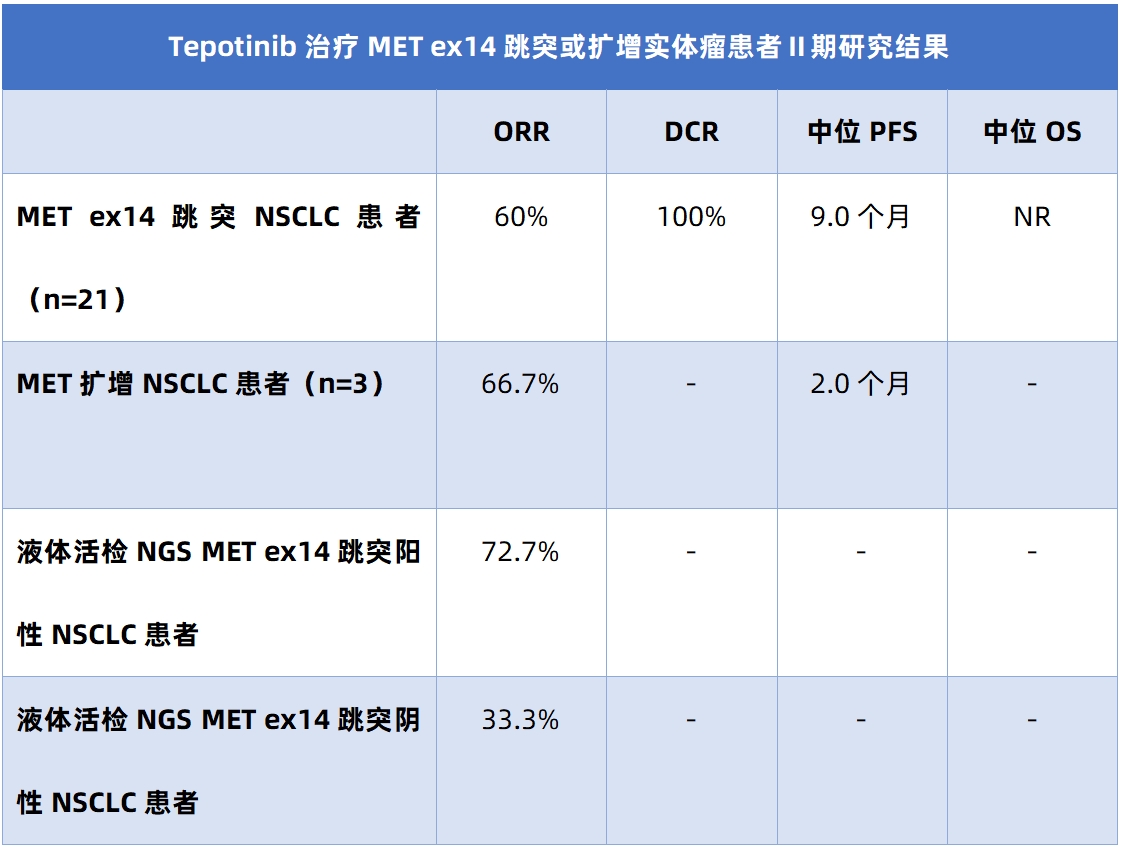
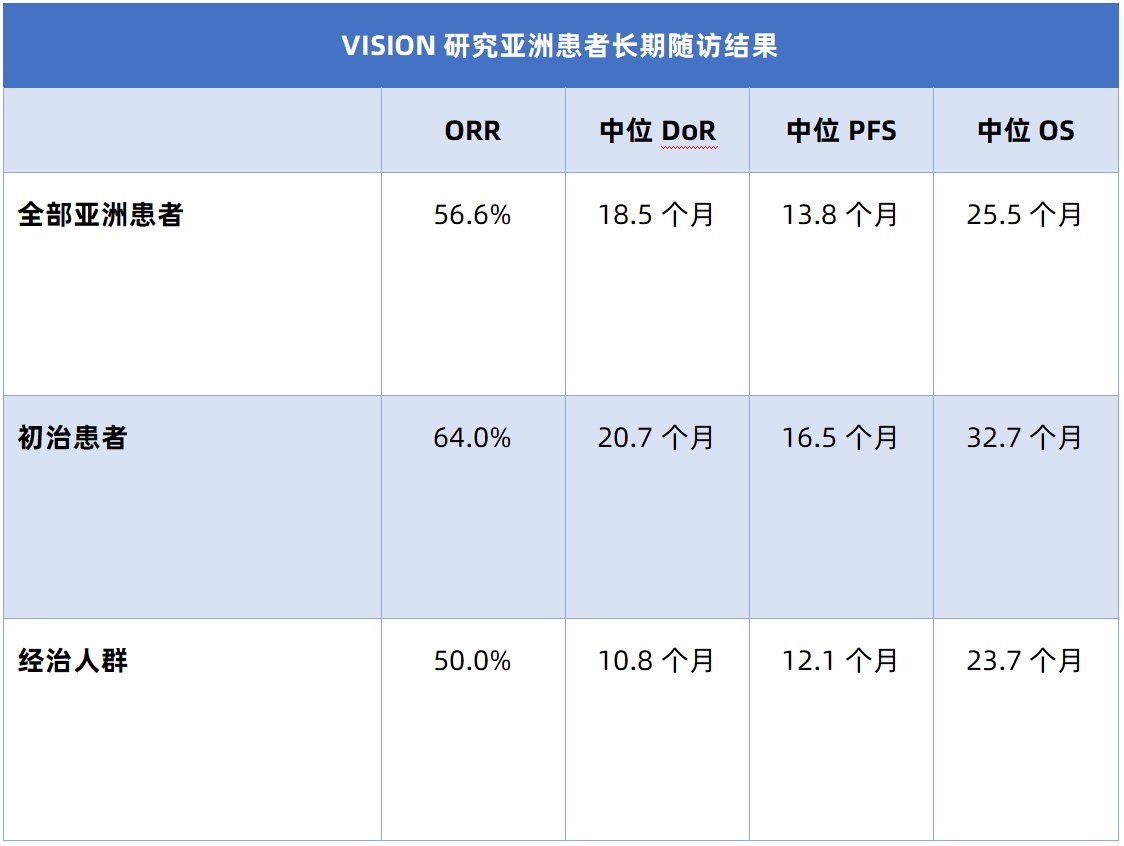
注 ORR:客观缓解率,DoR:缓解持续时间,PFS:无进展生存期,OS:总生存期,FISH:荧光原位杂交技术,NGS:二代测序技术,CBR:临床获益率,DCR:疾病控制率
在MET分子检测以及MET-TKI耐药机制方面,此次WCLC中同样报道了多项研究。VISION研究循环肿瘤(ct)DNA动态监测预后标志物及耐药机制分析显示,患者基线肝细胞生长因子(HGF)水平、治疗过程中sMET水平变化、TP53突变情况以及MET ex14突变等位基因频率(VAF)下降情况与MET ex14跳突NSCLC患者接受靶向治疗后的疗效获益存在明显相关性⁵。
另一项四川大学华西医院梁宗安教授团队汇报的评估组织NGS、ctDNA NGS与FISH在中国NSCLC患者中MET扩增检测一致性比较的研究提示,组织NGS与FISH在MET扩增检测中展示出了良好的一致性以及较高的灵敏度和特异性,但ctDNA NGS在MET扩增检测方面的敏感性仍需要进一步优化和提高⁶。
血液检测确认为MET异常的患者其肿瘤负荷通常较高,既往研究亦显示此类患者疗效相对更差。但值得注意的是,此次大会上报道的研究显示,部分液体活检NGS确认为MET ex14跳突阴性的NSCLC患者接受MET-TKI治疗,其病情亦可获得一定程度的缓解³,提示临床医生要注意血液检测发生“漏检”的可能性,张力教授补充道。
赛沃替尼 一线数据正式出炉,
一线数据正式出炉,
未来仍有更多数据值得期待!
除上述研究外,上海市胸科医院陆舜教授亦汇报了一项赛沃替尼治疗MET ex14跳突NSCLC Ⅲb期确证性临床研究中初治患者人群的结果数据⁷。该研究根据患者既往是否接受过系统治疗,以及后续赛沃替尼给药方案将其分为三个队列,此次WCLC报道了研究中队列2(1L队列)研究数据。该队列入组了87例既往未接受过任何系统治疗的MET ex14跳突晚期NSCLC患者,并给予患者赛沃替尼600mg(体重≥50kg)或400mg(体重<50kg) 每日一次(QD)进行治疗,张力教授介绍道。
结果显示,全分析集(FAS,n=87)中,独立审查委员会(IRC)评估的ORR、DCR分别为58.6%与92.0%,中位TTR为1.4个月,中位PFS为13.8个月,6个月PFS率分别为76.4%,中位DoR与OS尚未达到。经研究者(INV)评估,患者ORR为59.8%,DCR为92.0%,中位TTR与DoR分别为1.4个月与12.5个月。患者中位PFS达11.0个月,6个月PFS率为71.8%。肿瘤疗效可评估集(TRES,n=84)中,IRC评估的ORR与DCR分别为60.7%与95.2%,INV评估的ORR与DCR分别为61.9%与95.2%。值得一提的是,该研究显示,所有MET ex14跳突类型NSCLC患者均可从赛沃替尼治疗中获益,FAS中,患者12个月与18个月OS率分别达到了77.9%与53.8%。
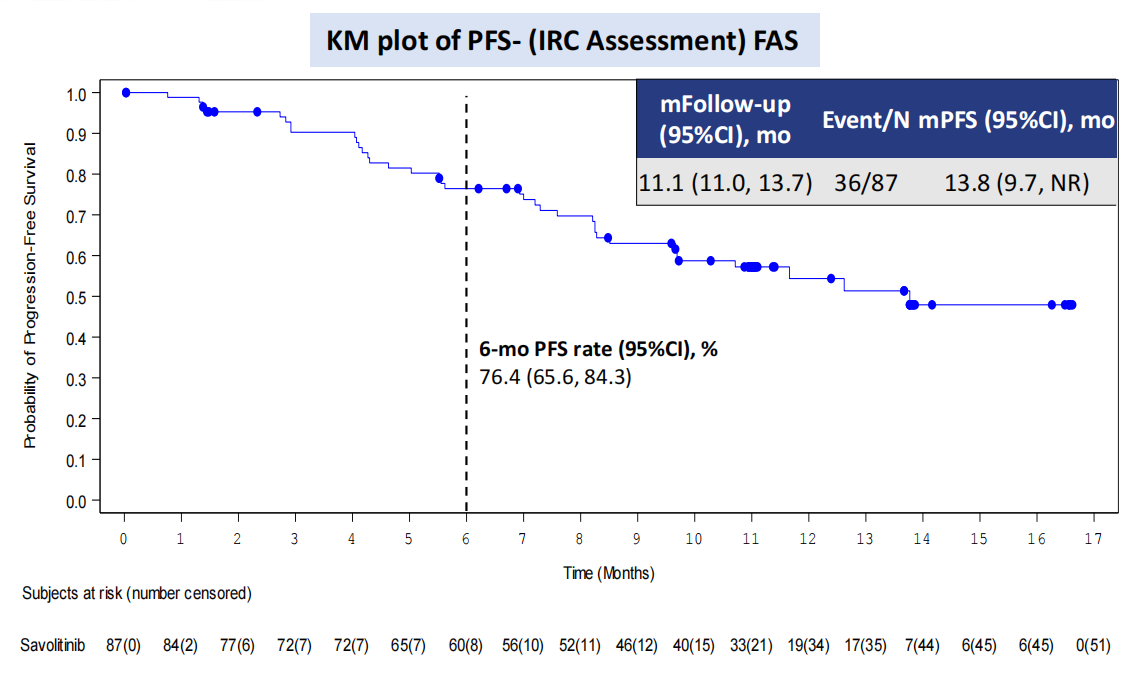
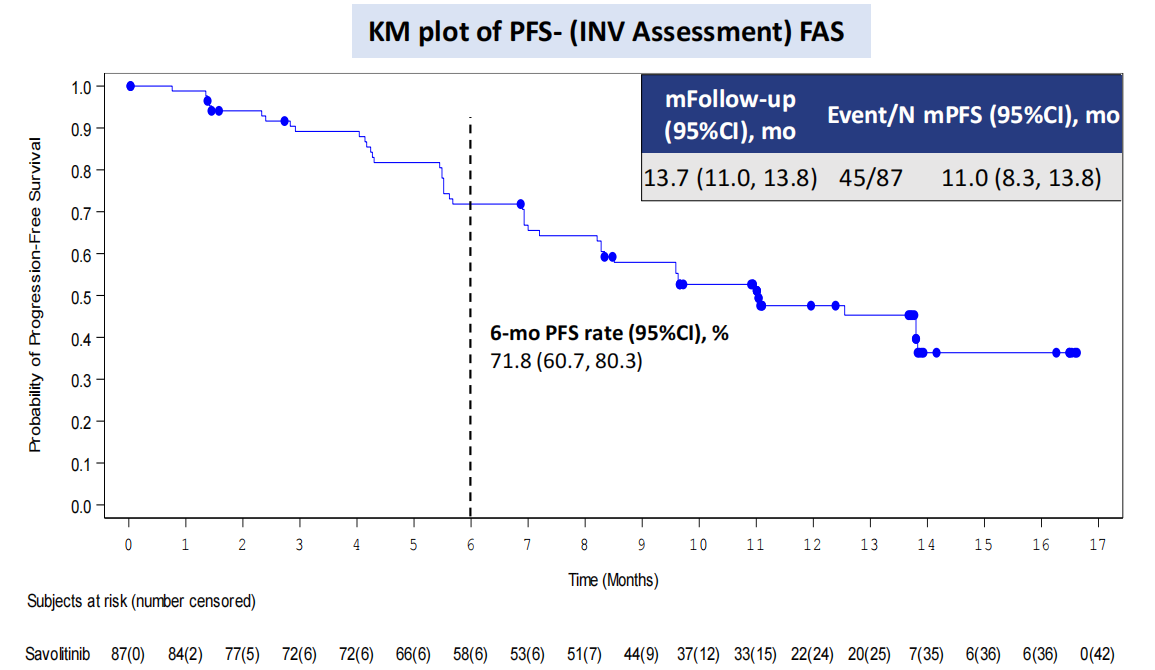
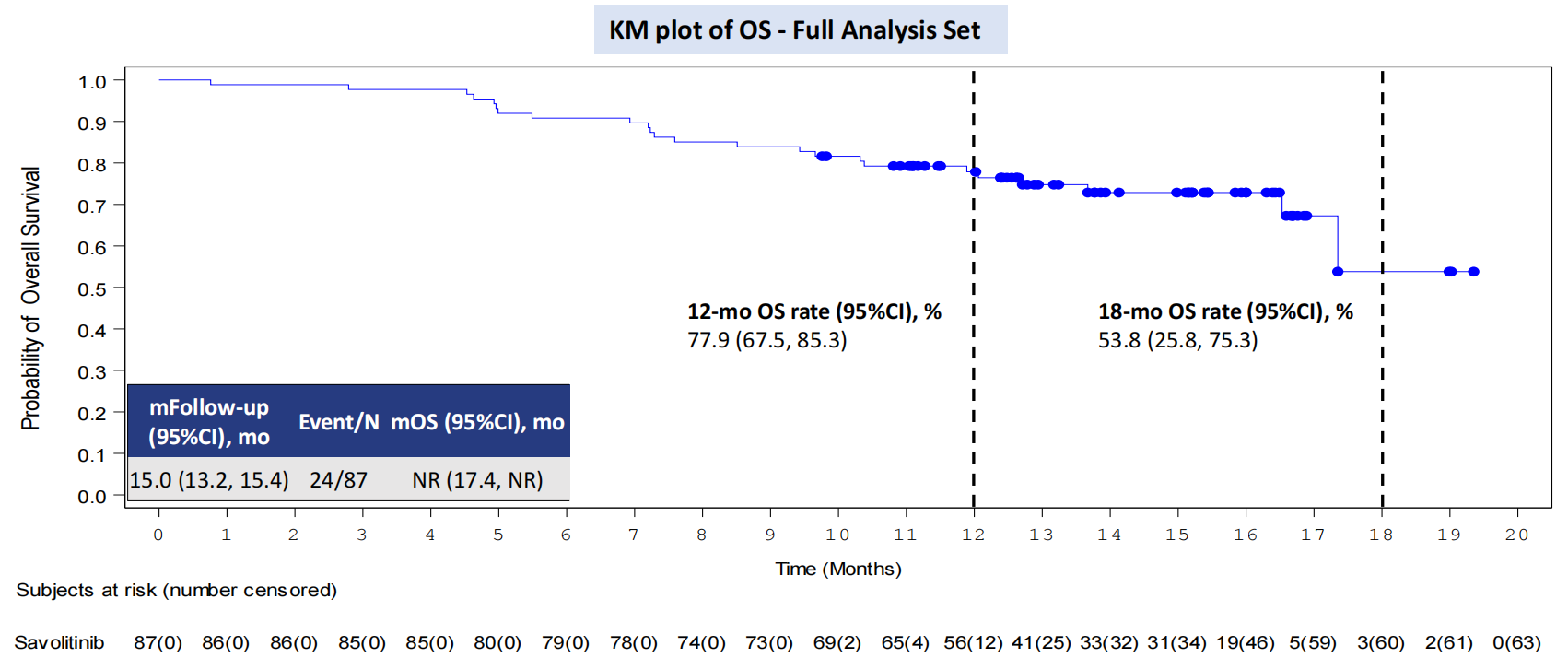
图1-3 FAS患者PFS与OS KM曲线
张力教授认为,该研究证明赛沃替尼用于MET ex14跳突NSCLC一线治疗可为患者带来显著的生存获益,与其个人临床研究及实践经验不谋而合。随后,张力教授表达了她对此研究的几点期待:
队列1、3研究数据
此项Ⅲb期研究共将患者分为三个队列,队列1纳入了既往含铂化疗方案治疗后疾病进展或毒性不耐受的患者,并给予其赛沃替尼600mg(体重≥50kg)或400mg(体重<50kg)QD进行治疗,队列3纳入了既往未接受过任何针对晚期疾病进行的系统抗肿瘤药物治疗的患者,给予其赛沃替尼300mg(体重≥50kg)或200mg(体重<50kg)每日两次(BID)进行治疗。期待未来相关研究数据的公布,进而展示出不同给药方案下赛沃替尼的疗效与安全性,为医生临床实践提供更多证据支撑。
脑转移患者数据
此前研究数据表明,以赛沃替尼为代表的Ⅰb型MET-TKI,具有较好的入脑能力,可为脑转移患者带来良好的临床获益,但由于既往多项研究中往往纳入脑转移患者数量较少,导致研究数据说服力有限。从此次陆舜教授所汇报的队列2研究数据可以发现,其中11.5%(10例)的患者基线伴有脑转移,期待未来该研究三组队列患者数据公布后,可进一步公布脑转移患者相关数据分析,从而为临床提供更多数据。
患者全程管理
随着研究的不断深入,患者生存时间的不断延长,如何在MET异常NSCLC患者治疗过程中,为其提供更好的全程管理,成为了众多医生关注的重点问题。患者MET-TKI治疗耐药后的影像、分子特征是什么?患者治疗过程中积极或不利的影响因素有哪些?如何为患者进行分子检测,制定综合治疗方案?这些问题单一研究可能无法完全回答,期待未来有更多研究进行探索并加以总结。
永无止路
MET异常NSCLC临床探索道阻且艰
既往临床研究所取得的成绩为临床解决了诸多问题,但临床医生在实践过程中所遇到的困难却要比此多得多,张力教授如是说,未来仍需肿瘤临床工作者在现有工作基础上进行进一步探索、研究,以进一步提升患者生存时长与质量,对于未来研究的探索方向可有以下几点:
完善MET检测平台与指标判读标准
众所周知,目前多项研究证明MET-TKI可显著提升MET ex14跳突与MET扩增患者生存获益,但其对于MET融合、MET其他外显子跳突等MET罕见异常NSCLC患者疗效如何,仍需进一步探索。与此同时,MET扩增患者可分为MET局部扩增患者与MET多体患者,二者接受靶向治疗的临床获益有所差异,如何界定NGS检测结果用于区隔MET局部扩增与MET多体的临界阈值,目前尚无定论。这些问题均有待临床日后完善检测平台与相关指标判读标准,才可进一步回答与解决。
MET异常NSCLC治疗方案探索
在晚期EGFR经典突变NSCLC诊疗领域,此前OPAL研究以及此次WCLC公布的FLAURA2研究证明靶向治疗联合化疗可为患者带来生存获益⁸⁻⁹。同时,ADAURA等研究也证明,靶向治疗在早期NSCLC的围术期治疗中,可为患者带来长生存获益¹⁰。未来,对于MET异常NSCLC患者能否采用靶向治疗联合化疗方案进行治疗?MET-TKI能否进军早期MET异常NSCLC患者围术期治疗值得业内学者关注、探索。除此之外,PACIFIC研究证明免疫治疗联合同步放化疗可有效延长Ⅲ期不可手术NSCLC患者生存,未来对于此类患者可否采用靶向治疗联合局部治疗亦需更多研究探索¹¹。
新型靶向药物研发
目前,除MET-TKI之外,靶向MET的单抗类药物、抗体药物偶联物(ADC)类药物等新型靶向治疗药物同样在进行积极研发,希望未来可有更多研究探索其治疗不同MET异常类型、肿瘤分期患者的疗效与安全性,从而为临床提供新的治疗选择。

