
革故鼎新,砥砺前行丨何建行教授:2023 NSCLC围术期治疗精彩盘点
肺癌是我国最常见的恶性肿瘤之一,发病率和死亡率均位列第一[1]。其中约80%-85%的肺癌患者为非小细胞肺癌 (NSCLC)患者,手术治疗是该类型患者主要的根治性治疗手段。但临床中仅约30%-40%的NSCLC患者可接受或潜在可接受手术治疗,且患者即便接受手术治疗,术后亦存在肿瘤复发、转移的风险,围术期治疗成为提升此类患者生存的重要手段[2]。回顾2023年,NSCLC围术期治疗战果颇丰,ADAURA、AEGEAN等多项研究在各大学术会议中更新、报道了最新研究数据。本文特邀国家呼吸医学中心主任、广州呼吸健康研究院院长何建行教授就此进行盘点、点评,以飨读者。
(NSCLC)患者,手术治疗是该类型患者主要的根治性治疗手段。但临床中仅约30%-40%的NSCLC患者可接受或潜在可接受手术治疗,且患者即便接受手术治疗,术后亦存在肿瘤复发、转移的风险,围术期治疗成为提升此类患者生存的重要手段[2]。回顾2023年,NSCLC围术期治疗战果颇丰,ADAURA、AEGEAN等多项研究在各大学术会议中更新、报道了最新研究数据。本文特邀国家呼吸医学中心主任、广州呼吸健康研究院院长何建行教授就此进行盘点、点评,以飨读者。
厚积薄发!AEGEAN研究引领“夹心饼”式免疫围术期治疗研究井喷式爆发
免疫治疗的出现为包括NSCLC在内的多个瘤种的临床诊疗提供了全新的治疗选择,既往多项研究证实,以PD-1/PD-L1为代表的免疫检查点抑制剂(ICI)用于晚期NSCLC临床治疗可显著改善患者生存获益。随着研究的不断深入,近年来,免疫治疗亦已逐渐成为早期可切除或潜在可切除NSCLC患者围术期治疗的“主力军”,极大地延长了患者生存,帮助患者看到了获得临床治愈的希望。
何建行教授指出,NSCLC免疫围术期治疗目前主要可分为三种模式,分别为“手术+辅助治疗”、“新辅助治疗+手术”以及“新辅助治疗+手术+辅助治疗”。在这三者之中,2023年,以AEGEAN研究为代表的NSCLC“夹心饼”式免疫围术期治疗相关研究可谓是呈井喷式的爆发,先后有5项重磅研究陆续公布研究结果。
AEGEAN研究是一项随机对照、双盲、国际多中心Ⅲ期临床试验,评估了可切除ⅡA-ⅢB(N2)期NSCLC(AJCC 第8版)患者使用度伐利尤单抗 “新辅助免疫治疗+手术切除+辅助免疫治疗”方案进行治疗的疗效与安全性,研究共纳入了802例患者,并按1:1随机接受4周期度伐利尤单抗或安慰剂联合含铂双药化疗新辅助治疗+12周期度伐利尤单抗或安慰剂辅助治疗[3]。
“新辅助免疫治疗+手术切除+辅助免疫治疗”方案进行治疗的疗效与安全性,研究共纳入了802例患者,并按1:1随机接受4周期度伐利尤单抗或安慰剂联合含铂双药化疗新辅助治疗+12周期度伐利尤单抗或安慰剂辅助治疗[3]。
2023美国癌症研究协会(AACR)大会中,研究人员首次报道了AEGEAN研究中期分析数据。结果显示,在排除表皮生长因子受体(EGFR)或间变性淋巴瘤激酶(ALK)阳性的改良意向治疗(mITT)人群中,度伐利尤单抗组和对照组患者中位无事件生存期(EFS)分别为未达到(NR)和25.9个月(HR:0.68,95%CI:0.53-0.88,P=0.0039),病理完全缓解(pCR)率分别为17.2%和4.3%,差异值为13%(95%CI:8.7%-17.6%,P=0.000036);主要病理缓解(MPR)率分别为33.3%和12.3%,差异值为21%(95%CI:15.1%-26.9%,P=0.000002),证明度伐利尤单抗联合含铂双药化疗的围术期治疗方案可有效延长患者生存[3]。
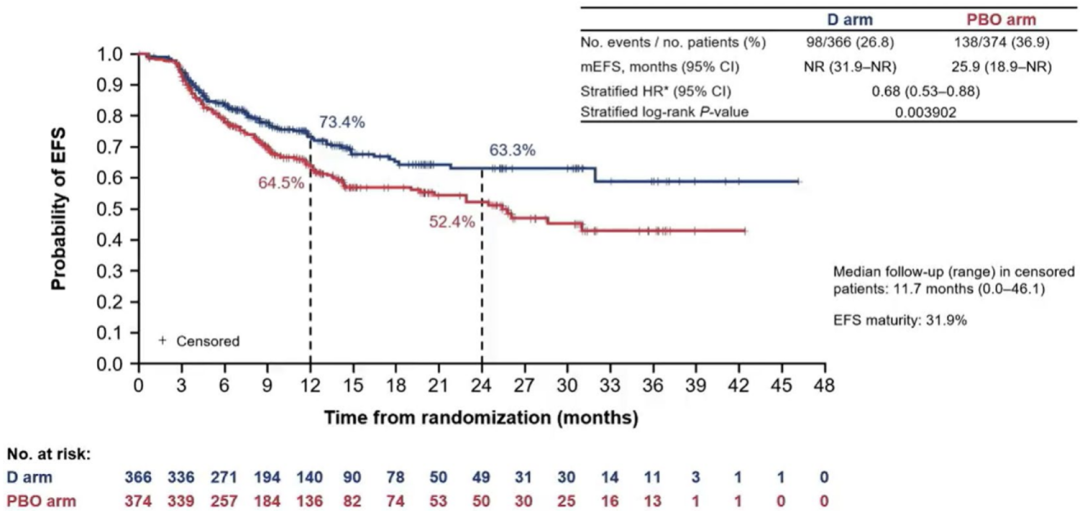
图1 AEGEAN研究中经盲态独立中心评估(BICR)的mITT人群EFS数据
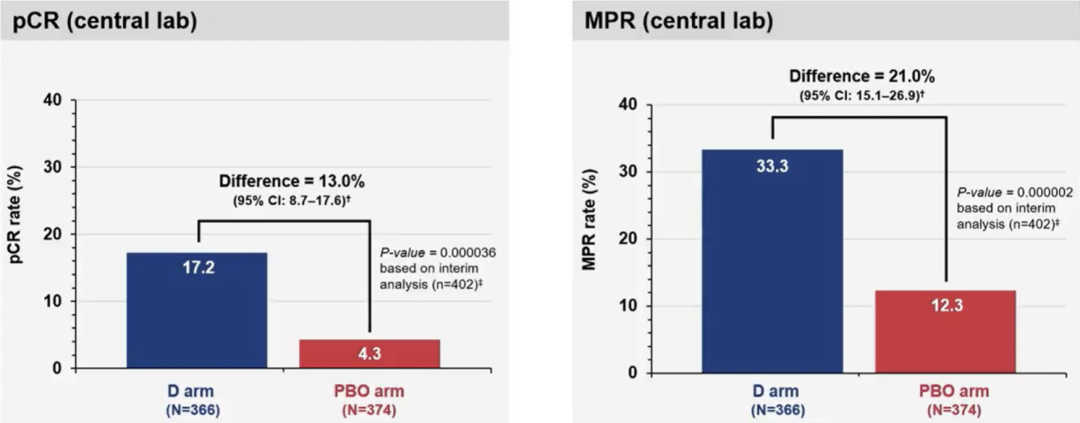
图2 AEGEAN研究中mITT人群pCR率与MPR率数据
不仅如此,在随后的2023 WCLC中,研究人员报道的AEGEAN研究手术结局探索性分析数据再一次证实,度伐利尤单抗围术期治疗方案不仅可改善患者EFS以及pCR,且不会影响患者接受手术治疗的可行性、方式、范围和时机等,并具备可控的手术安全性[4]。2023欧洲肿瘤内科学会(ESMO)报道的患者循环肿瘤(ct)DNA清除率与病理缓解相关性结果,更是提示度伐利尤单抗组患者具有更高的ctDNA清除率,其可能与患者更高的pCR率和MPR率相关[5]。未来,ctDNA清除率或有可能成为评估患者接受新辅助治疗获益情况的生物标志物。
除AEGEAN研究外,KEYNOTE-671、CheckMate-77T、NEOTORCH以及RATIONALE-315等多项探索NSCLC“夹心饼式”免疫围术期治疗相关研究,均提示该方案可为患者带来显著的获益提升[6-9]。随着越来越多的研究进行探索,“夹心饼”式免疫围术期治疗在NSCLC临床治疗中逐渐获得愈发充分循证医学证据,未来或将成为早期NSCLC的标准围术期治疗方案。
此外,IMpower010、KEYNOTE-091、CheckMate-816等免疫辅助与新辅助治疗相关研究,亦在2023年各大肿瘤学术会议中得到了更新报道[10-18]。在这之中值得关注与思考的是,目前尚没有证据可直接证明“手术+辅助治疗”、“新辅助治疗+手术”以及“新辅助治疗+手术+辅助治疗”三种常见的治疗模式究竟孰优孰劣。而对比CheckMate-816研究与CheckMate-77T研究中患者EFS获益情况亦可发现,单纯新辅助治疗与“夹心饼”式围术期治疗之间的优劣存在较大争议,且众所周知的是,术后达到pCR的患者往往具有更好的预后,因此对于此类患者术后是否有必要接受辅助治疗未来需进一步研究。
对于“夹心饼”式围术期治疗模式新辅助治疗阶段是否有进一步优化的空间亦值得探索,根据目前得到报道的NSCLC“夹心饼”式免疫围术期治疗研究可以发现,当下主流的免疫新辅助治疗用药周期为3-4周期。众所周知,手术时机与方式的选择与患者的预后密切相关,因此如何判断患者新辅助治疗阶段最佳用药周期以及手术时机与方式,将成为未来需要肺癌内外科医生共同探索的问题之一。
结束争议!ADAURA研究证实靶向辅助治疗确可为患者带来长生存获益!
除免疫治疗外,靶向治疗同样成为了降低NSCLC患者术后复发风险的重要治疗手段,相关临床研究层出不穷。纵观2023年NSCLC围术期靶向治疗相关研究,ADAURA研究与ALINA研究无疑成为了“皇冠上的明珠”,为NSCLC靶向辅助治疗提供了重要的循证医学证据。
ADAURA研究是一项全球性的Ⅲ期双盲随机对照临床研究,探索了奥希替尼 用于完全切除的,ⅠB-ⅢA期(AJCC第7版)EGFR敏感突变NSCLC患者辅助治疗的疗效和安全性[19]。此前,该研究结果证实,奥希替尼辅助治疗可显著提升ⅠB-ⅢA期EGFR敏感突变NSCLC患者无病生存期(DFS)获益(65.8个月 vs. 28.1个月,HR:0.27,95%CI:0.21-0.34),并可有效降低患者颅内疾病复发、死亡风险[中枢神经系统(CNS)-DFS HR:0.36,95%CI:0.23-0.57][20]。
用于完全切除的,ⅠB-ⅢA期(AJCC第7版)EGFR敏感突变NSCLC患者辅助治疗的疗效和安全性[19]。此前,该研究结果证实,奥希替尼辅助治疗可显著提升ⅠB-ⅢA期EGFR敏感突变NSCLC患者无病生存期(DFS)获益(65.8个月 vs. 28.1个月,HR:0.27,95%CI:0.21-0.34),并可有效降低患者颅内疾病复发、死亡风险[中枢神经系统(CNS)-DFS HR:0.36,95%CI:0.23-0.57][20]。
2023 ASCO年会公布的ADAURA研究总生存期(OS)结果显示,在ⅠB-ⅢA期患者中,奥希替尼组和安慰剂组分别经过中位时间60.4个月和59.4个月的随访后,3年OS率分别为95%和89%,5年OS率分别为88%和78%,奥希替尼为患者带来了OS显著改善(HR:0.49, 95.03%CI:0.34-0.70, p<0.0001),患者死亡风险降低51%,且不论患者在奥希替尼治疗前是否接受辅助化疗均可获得显著的OS获益提升[21]。
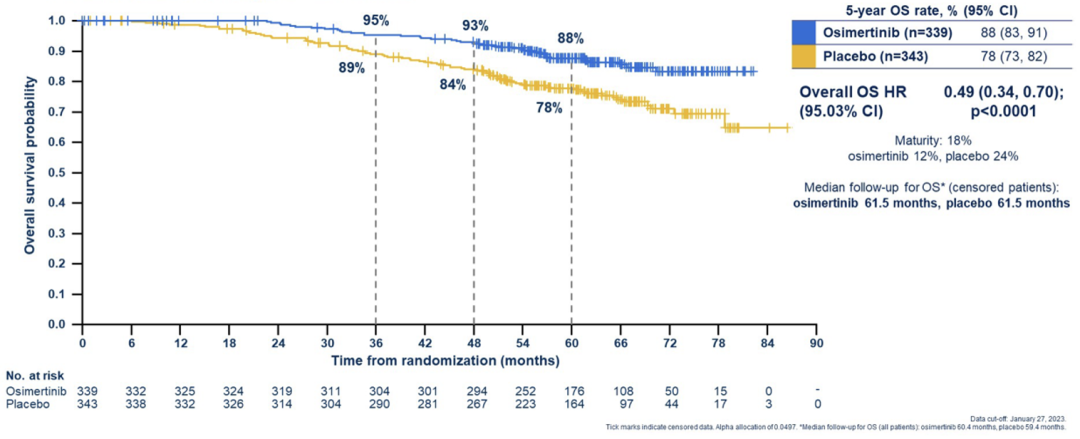
图3 ADAURA研究中ⅠB-ⅢA期患者OS数据
在Ⅱ-ⅢA期患者中,奥希替尼组和安慰剂组的中位随访时间分别为59.9个月和56.2个月,两组患者5年OS率分别为85%与73%(HR:0.49, 95.03%CI:0.33-0.73, p=0.0004)。此外,在根据患者年龄、种族、疾病分期以及化疗方案等多个因素进行的亚组分析中可以观察到,奥希替尼各亚组患者均具有与整体患者一致的获益趋势[21]。
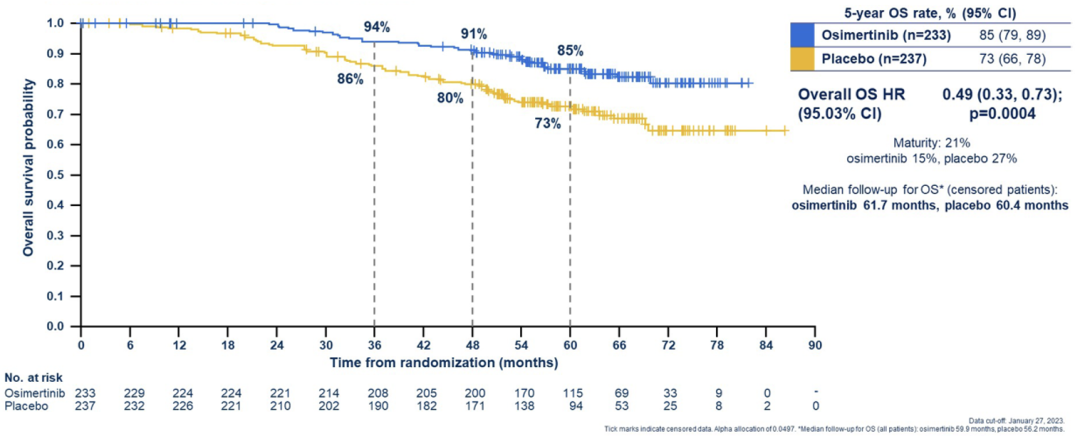
图4 ADAURA研究中Ⅱ-ⅢA期患者OS数据
ALINA研究同样探索了阿来替尼 用于早期ALK阳性NSCLC患者辅助治疗的疗效和安全性。根据研究人员在2023 ESMO与欧洲肿瘤内科学会亚洲大会(ESMO Asia)中公布的ALINA研究数据可以发现,阿来替尼辅助治疗同样可显著提升ALK阳性NSCLC患者DFS,且亚洲患者与整体患者具有相似的获益趋势[22,23]。
用于早期ALK阳性NSCLC患者辅助治疗的疗效和安全性。根据研究人员在2023 ESMO与欧洲肿瘤内科学会亚洲大会(ESMO Asia)中公布的ALINA研究数据可以发现,阿来替尼辅助治疗同样可显著提升ALK阳性NSCLC患者DFS,且亚洲患者与整体患者具有相似的获益趋势[22,23]。
何建行教授表示,ADAURA研究与ALINA研究证明,针对EGFR、ALK阳性早期NSCLC患者,奥希替尼与阿来替尼可显著提升患者DFS获益甚至是OS获益。因此针对ROS1、MET、RET等驱动基因阳性早期NSCLC患者或同样可采用对应靶向治疗药物为患者进行辅助治疗,以提升患者生存获益。
另外,EGFR作为NSCLC最先发现,同时也最为常见的抗肿瘤治疗靶点。此前,针对EGFR阳性NSCLC患者的靶向辅助治疗,肺癌临床工作者进行了诸多探索。如今,EGFR阳性NSCLC术后辅助治疗逐渐趋于标准化,但目前临床中针对ⅠA-ⅠB期NSCLC患者术后是否需要接受辅助治疗仍存在一定争议,何建行教授补充道。
此前其团队所进行的一项评估EGFR-TKI用于完全切除的Ⅰ期EGFR敏感突变NSCLC术后辅助治疗疗效及安全性的回顾性分析显示,对于Ⅰ期NSCLC患者,术后靶向辅助治疗可显著提升其生存获益,患者5年DFS率与OS率分别可提升19.8%(99.4% vs 79.6%)与6.3%(100% vs 93.7%)。其中ⅠA期与ⅠB期患者术后接受靶向辅助治疗,其5年DFS率分别从84.5%与75.3%提升至100%与98.8%,且在患者停药后的长期随访中,仍可观察到持续获益[24],何建行教授介绍道,目前一项评估奥希替尼用于完全切除的EGFR阳性ⅠA2-ⅠA3期NSCLC辅助治疗疗效和安全性的随机、双盲、安慰剂对照国际Ⅲ期研究——ADAURA2研究正在进行之中[25]。期待未来其研究数据的公布,从而给予临床医生更多指导。
何建行教授还指出,NSCLC靶向新辅助治疗以及“夹心饼”式围术期治疗能否改善患者生存获益,同样值得关注。NeoADAURA研究、ALNEO研究以及NAUTIKA1伞式研究目前正在为此进行探索[26-28]。其中,NeoADAURA研究是一项全球多中心、随机对照、三臂Ⅲ期研究,旨在比较奥希替尼单药或联合化疗对比标准化疗用于可切除Ⅱ-ⅢB期(N2)EGFR敏感突变NSCLC(AJCC 第8版)患者新辅助治疗的疗效与安全性。NeoADAURA研究预计将于2024年第三季度公布首次中期分析数据,这或将使早期NSCLC临床实践在检测、诊断、治疗等多方面产生剧变。
总结
2023年可谓是NSCLC围术期治疗的“丰收年”,多项相关研究得到报道。但需要关注的是,NSCLC围手术期治疗循证医学证据日渐丰富的同时,仍然面临着许多需进一步探索、完善的问题。但随着越来越多的研究数据出炉,可以肯定的是,早期可手术或潜在可手术NSCLC围术期治疗药物、方案选择将愈发丰富,患者生存获益亦将得到极大的改善,其EFS、DFS甚至是OS均可能得到显著提升。期待未来临床可有更多NSCLC围术期临床研究数据持续公布,从而进一步完善临床诊疗实践,提升患者综合临床获益。


