
耀新生·愈食光 研究者说 | 姜宏景教授:势不可挡,卡瑞利珠单抗联合化疗围术期治疗局晚期食管癌取得关键阳性结果
随着免疫联合化疗在晚期食管癌 一线治疗中标准地位的确立,免疫治疗在食管癌新辅助治疗中的探索如火如荼。2024 ASCO GI会议上,由李印教授牵头开展、全国24家中心共同参与的一项“卡瑞利珠单抗
一线治疗中标准地位的确立,免疫治疗在食管癌新辅助治疗中的探索如火如荼。2024 ASCO GI会议上,由李印教授牵头开展、全国24家中心共同参与的一项“卡瑞利珠单抗 联合化疗对比化疗新辅助治疗可切除局晚期食管鳞癌(ESCC)”的全国多中心、随机、平行对照III期研究(ESCORT-NEO/NCCES01)1成功入选最新突破性研究(LBA),成为全球首个食管癌围术期免疫治疗III期研究。研究结果显示,卡瑞利珠单抗+白蛋白紫杉醇
联合化疗对比化疗新辅助治疗可切除局晚期食管鳞癌(ESCC)”的全国多中心、随机、平行对照III期研究(ESCORT-NEO/NCCES01)1成功入选最新突破性研究(LBA),成为全球首个食管癌围术期免疫治疗III期研究。研究结果显示,卡瑞利珠单抗+白蛋白紫杉醇 +顺铂
+顺铂 组(A组:卡瑞利珠单抗+nab-TP)和卡瑞利珠单抗+紫杉醇+顺铂组(B组:卡瑞利珠单抗+TP)pCR率均显著优于紫杉醇+顺铂组(C组:TP)(A组 vs C组,28.0% vs 4.7%,p<0.0001;B组 vs C组,15.4% vs 4.7%,p=0.0034),两组均达到了主要终点,且未增加手术风险,安全性良好。结果表明新辅助卡瑞利珠单抗联合化疗有望成为局晚期食管癌的潜在标准治疗方案。
组(A组:卡瑞利珠单抗+nab-TP)和卡瑞利珠单抗+紫杉醇+顺铂组(B组:卡瑞利珠单抗+TP)pCR率均显著优于紫杉醇+顺铂组(C组:TP)(A组 vs C组,28.0% vs 4.7%,p<0.0001;B组 vs C组,15.4% vs 4.7%,p=0.0034),两组均达到了主要终点,且未增加手术风险,安全性良好。结果表明新辅助卡瑞利珠单抗联合化疗有望成为局晚期食管癌的潜在标准治疗方案。
为传递食管癌免疫治疗新理念,实现科研成果与临床实践相结合,“耀新生·愈食光”栏目组特别策划ESCORT-NEO/NCCES01研究PI独家专访系列活动,本期诚邀天津医科大学肿瘤医院胸外科资深专家姜宏景教授作为访谈嘉宾,对局晚期食管癌治疗模式、ESCORT-NEO/NCCES01研究结果与临床价值、食管癌未来探索方向等话题进行分享。栏目将以访谈为依托,以笔墨为媒介,开启食管癌围术期治疗新篇章。
百尺竿头,更进一步,局晚期食管癌围术期治疗仍需改进
姜宏景教授:局晚期食管癌分成可切除食管癌和不可切除食管癌,对于可切除食管癌,基于荷兰的CROSS研究2和国内的NEOCRTEC5010研究3的阳性结果,指南推荐同步放化疗作为标准新辅助治疗方案4,开启了食管癌综合治疗的新阶段。近几年,我中心的临床实践也将同步放化疗作为主流治疗模式。然而,接受同步放化疗的患者预后仍不尽如人意。首先,无论是CROSS研究还是NEOCRTEC5010研究,仍有较高的远处转移的发生率,提示放疗和手术这类局部治疗手段对肿瘤远处转移的控制力度仍不够。此外,在临床实践中,外科医生发现接受放化疗的患者常会出现严重水肿 、周围组织粘连等情况,导致手术难度提高,手术风险增加。因此,国内部分中心对同步放化疗作为新辅助治疗的态度较为谨慎,欧美地区使用该方案的比例也很低。近年来,免疫检查点抑制剂的出现与加入为局晚期食管癌围术期治疗带来了新的视角。
、周围组织粘连等情况,导致手术难度提高,手术风险增加。因此,国内部分中心对同步放化疗作为新辅助治疗的态度较为谨慎,欧美地区使用该方案的比例也很低。近年来,免疫检查点抑制剂的出现与加入为局晚期食管癌围术期治疗带来了新的视角。
全球首个,独树一帜,ESCORT-NEO研究取得关键阳性结果
姜宏景教授:为确认免疫治疗的加入对围术期治疗的意义,李印教授牵头开展了一项全国多中心、三臂、随机、平行对照III期研究(ESCORT-NEO/NCCES01),共纳入391例可切除局晚期胸段食管鳞癌患者。患者被随机分为三组进行新辅助治疗。
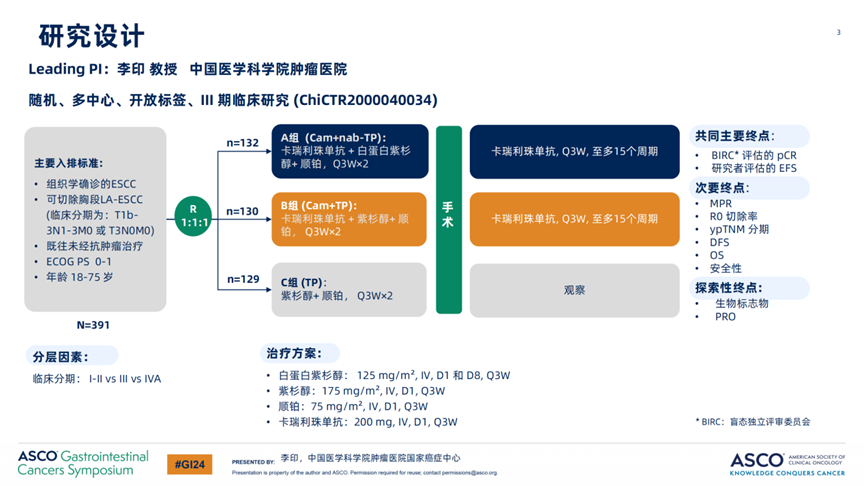
图1:ESCORT-NEO/NCCES01研究设计
结果显示,新辅助卡瑞利珠单抗联合化疗较新辅助化疗显著提高了局晚期可切除食管癌患者的pCR率。A组(卡瑞利珠单抗+白蛋白紫杉醇和顺铂)与 C组(紫杉醇和顺铂)的pCR率为28.0% vs 4.7%(p<0.0001);B组(卡瑞利珠单抗+紫杉醇和顺铂) 与C组(紫杉醇和顺铂)的pCR率为15.4% vs 4.7%(p=0.0034),两组均达到了统计学显著差异。A、B、C三组的主要病理缓解(MPR)率分别为59.1%,36.2%和20.9%1。这一数据不仅印证了卡瑞利珠单抗作为免疫药物加入的意义,也显示了白蛋白紫杉醇作为化疗药物的价值。此外,治疗过程的安全性评估较为乐观,与单纯化疗相较,卡瑞利珠单抗联合化疗在新辅助治疗期间未显著增加严重不良事件发生率,整体可耐受。
ESCORT-NEO/NCCES01研究是全球首个食管癌围术期免疫治疗III期研究,凭借其多中心、大规模的随机对照试验(RCT)设计、令人鼓舞的疗效与安全性的结果,提供了高级别的循证医学证据,为可切除的局晚期食管癌围术期使用免疫药物奠定了坚实的科学基础。
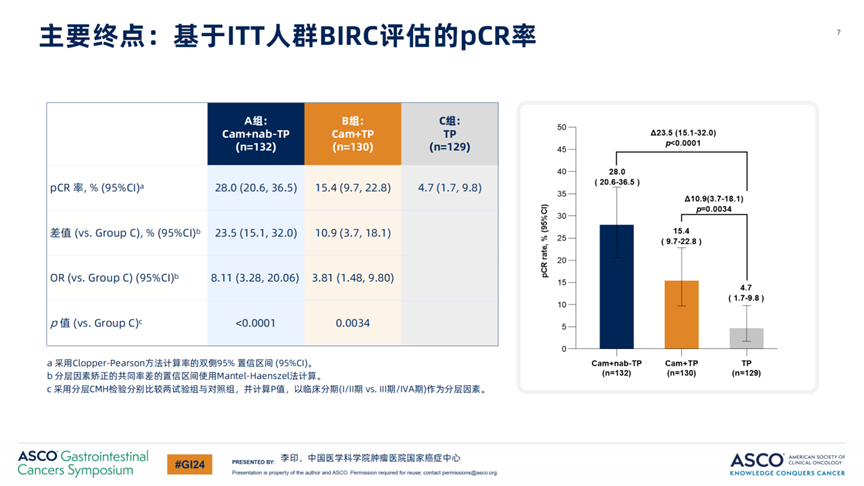
图2:ITT人群BIRC评估的pCR率
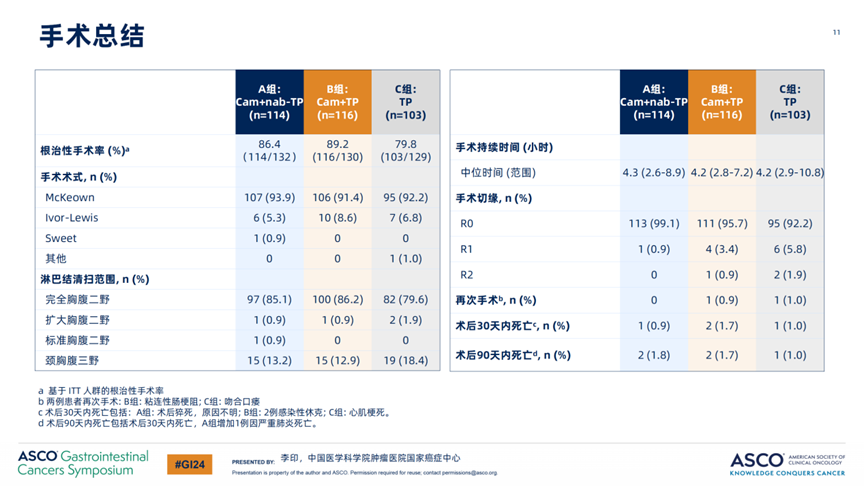
图3:A组 vs B组 vs C组手术总结
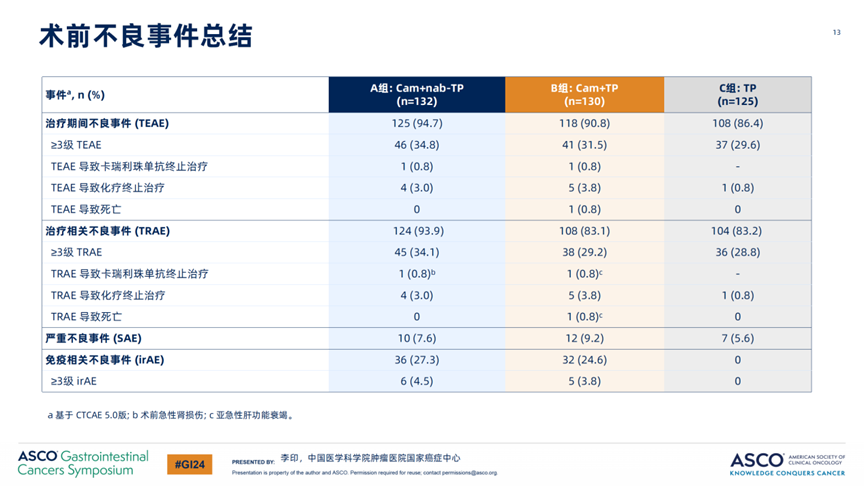
图4:A组 vs B组 vs C组术前不良事件总结
长期随访,静候佳音,卡瑞利珠单抗联合化疗围术期治疗或可实现长生存获益
姜宏景教授:ESCORT-NEO研究长期随访的无事件生存期(EFS)和总生存期(OS)的结果非常值得期待。尽管pCR率和MPR率的显著改善不能直接等同于EFS和OS显著改善,但接受免疫联合化疗围术期治疗的患者仍有潜在的长生存获益可能。既往的同步放化疗+手术是1个全身治疗+2个局部治疗的组合,而现在的免疫治疗联合化疗+手术方案则是2个全身治疗+1个局部治疗的组合,或可弥补既往方案的缺憾,降低远处转移几率,从而让患者获得较为良好的长期预后结果。
前路漫漫,曙光熹微,局晚期食管癌诊疗困境与机遇并存
姜宏景教授:一方面,食管外科是一门年轻的学科,从上个世纪30年代问世至今不足百年,尚处于起步阶段。尽管研究者在保器官、延迟手术等方向进行了诸多尝试,但大多停留于试验阶段,未能在临床推广。另一方面,食管外科正在飞速进步,ESCORT-NEO研究结果侧面印证了这一点:在不同围术期治疗下,三组R0切除率相近,均超过90%1。这一成就与外科治疗理念、技术和器材的进步密切相关。数年来,食管癌外科术式从传统的开腹手术转变为腔镜手术,并有望进一步过渡到以机器人手术为主流的精细操作时代。药物方面,免疫治疗介入新辅助治疗阶段也显示出了巨大潜力,ESCORT-NEO研究阳性结果有力证实了这一点。然而,免疫检查点抑制剂和化疗药物的用药顺序尚无定论,免疫治疗肿瘤的机制亦不明确。另外,安全性也是临床所关注的。为了降低毒性,是否需要降低化疗剂量?是否需要减少化疗药物种类,甚至去化疗?这些问题都有待进一步阐明。不过我们不能盲目地试验,而是应该通过机制的提示,有的放矢,剥开层层迷雾,从错综复杂的选项之中找到正确的道路。

