
洪天配教授:“心-肾-代谢综合征”治疗展望,“降糖”兼具“减重”获益更佳!
医脉通整理报道,未经授权请勿转载。
审核:洪天配 教授
引言:2024年5月18日,由北京大学糖尿病中心、《中国糖尿病杂志》、中国医学救援协会联合主办的“2024 北大糖尿病论坛”于首都北京盛大召开。“北大糖尿病论坛”自2005年至今,已成功举办二十届,在业内极具影响力。

2024北大糖尿病论坛会场
本届论坛以“心肾代谢”为核心议题,聚焦糖尿病及其并发症的防治策略。会上,北京大学第三医院洪天配教授以《兼具降糖和减重作用的药物治疗心血管-肾脏-代谢综合征的展望》为题发表主题演讲,对具有显著心肾及代谢获益的药物进行性深入浅出的阐述。本文将会议精要概述如下,供各位读者学习参考。

洪天配教授发言
专家介绍:北京大学第三医院内分泌科主任、二级教授、主任医师、博士生导师;
中国医师协会内分泌代谢科医师分会候任会长;
中华医学会内分泌学分会副主任委员;
ADA精粹 (DiabetesCare/Diabetes)中文版共同主编,中华糖尿病杂志、中华内分泌代谢杂志等6个中文核心期刊的副总编,Diabetology & Metabolic Syndrome副主编,Journal of Diabetes Investigation等SCI期刊的编委。
形势严峻:超重或肥胖与“心-肾-代谢综合征”密不可分
洪天配教授指出,目前流行病数据显示,全球范围内近半数2型糖尿病(T2DM)患者未能实现血糖达标,其中超重或肥胖的占比超过50%。研究数据表明,T2DM患者中血糖控制未达标(HbA1c<7%)及超重或肥胖的患者比例在美国分别为49.5%、89.7%,欧洲为46.4%、85.3%,日本为51.5%、52.7%,我国为50.6%和65.3%。与此同时,T2DM患者中超重或肥胖的比例有逐年升高的趋势(图1)。
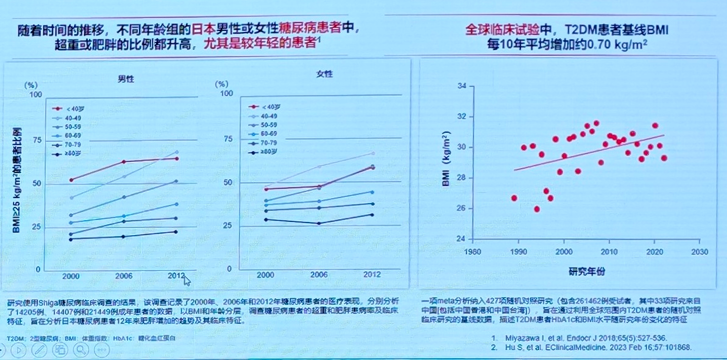
图1 T2DM合并超重或肥胖逐年增高
超重或肥胖是T2DM病理生理的关键组成部分,肥胖相关的胰岛素抵抗可加剧脂肪组织的炎症和葡萄糖转运功能的受损,最终导致胰岛β细胞功能的失代偿,并且体重或腰围的增加会加重胰岛素抵抗程度,不仅可以增加T2DM的风险,还会增加血糖管理的难度。此外,肥胖还是射血分数保留性心力衰竭(HFpEF)的危险因素,HFpEF患者中合并超重或肥胖的比例高达85%,减重措施可以有效改善HFpEF相关临床指标。
纤丝万缕:糖尿病、心血管疾病、慢性肾脏病相互关联
2017年全球疾病负担研究的系统分析表明,T2DM已成为越来越常见的慢性肾脏病(CKD)病因。与无CKD患者相比,T2DM合并CKD患者发生冠心病和脑卒中的风险显著升高。T2DM合并CKD患者的心血管死亡风险较单纯T2DM患者和单纯CKD患者分别高出2倍和1倍。此外,糖尿病合并心血管疾病(CVD)或CKD会引起加倍的寿命损失。与单纯糖尿病或CKD相比,糖尿病合并CKD会显著增加全因死亡。
由于心血管、肾脏、代谢系统相互关联,因此心血管-肾脏-代谢综合征(CKM)的概念应运而生。2023年美国心脏学会(AHA)发表了关于CKM的主席建议,对CKM的概念进行了详细阐述。CKM定义为由肥胖和糖尿病、CKD及CVD之间病理生理相互作用导致的全身性疾病。真实世界研究数据显示,T2DM合并CKM综合征的患者比例高达93.7%。
新的循证医学证据表明,肥胖和T2DM与心肾并发症之间还可能存在新的病理生理机制(图2)。
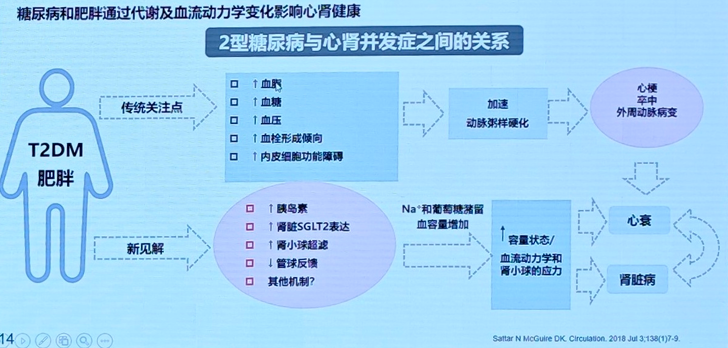
图2 2型糖尿病与心肾并发症之间的关系
应对策略:“降糖兼具减重”带来显著的心、肾、代谢获益
洪天配教授指出,钠-葡萄糖共转运蛋白2抑制剂(SGLT2i)和胰高血糖素样肽-1受体激动剂(GLP-1RA)具有降糖、减重以及显著的心肾获益。新版 ADA/EASD共识提出应将降血糖、减重、心肾保护和心血管危险因素管理作为T2DM的综合管理策略。
近些年来的研究数据显示,GLP-1RA、葡萄糖依赖性促胰岛素多肽(GIP)/ 胰高糖素样肽-1(GLP-1)双受体激动剂(如司美格鲁肽、替尔泊肽)等新型降糖药物对T2DM患者的体重管理具有较强疗效,且带来的减重效应可进一步改善T2DM患者的血糖控制。因此,ADA指南推荐,对于超重或肥胖的T2DM患者,应首选兼具减重作用的降糖药物,包括GLP-1RA和GIP/GLP-1双受体激动剂。
本文小结
洪天配教授对本次报告内容进行总结:肥胖、T2DM与心肾疾病密切相关、相互联系,应在整体层面上视为一组综合征。T2DM的综合管理应将降血糖、减重、心肾保护和心血管危险因素管理作为同等重要的地位。因此,在临床实践中,对于超重或肥胖的T2DM患者,应首选兼具降糖和减重作用的药物,并进行个性化、规范化和多学科协作的医疗照护,争取实现心血管-肾脏-代谢的全方位管理。

