
2024 ASCO 中外对话,前沿远望,CDK4/6抑制剂治疗HR+/HER2-乳腺癌面面观
当地时间5月31日至6月4日,2024年美国临床肿瘤学会(ASCO)年会于在美国芝加哥举办,本次大会公布了包括MONALEESA-3研究、NATALEE研究等多项HR+/HER2-乳腺癌 领域重磅研究进展,为CDK4/6抑制剂在HR+/HER2-乳腺癌晚期以及早期辅助治疗的应用进一步提供了宝贵循证证据。值此之际,医脉通特邀加拿大不列颠哥伦比亚大学Stephen Chia教授、北京大学人民医院王殊教授和复旦大学附属肿瘤医院张剑教授进行中外圆桌访谈,针对最新前沿研究成果为我们带来鞭辟入里的深度解读,共同探讨CDK4/6抑制剂在HR+/HER2-乳腺癌临床中的应用前景。
领域重磅研究进展,为CDK4/6抑制剂在HR+/HER2-乳腺癌晚期以及早期辅助治疗的应用进一步提供了宝贵循证证据。值此之际,医脉通特邀加拿大不列颠哥伦比亚大学Stephen Chia教授、北京大学人民医院王殊教授和复旦大学附属肿瘤医院张剑教授进行中外圆桌访谈,针对最新前沿研究成果为我们带来鞭辟入里的深度解读,共同探讨CDK4/6抑制剂在HR+/HER2-乳腺癌临床中的应用前景。
ΔctDNA的价值:MONALEESA-3研究提示,ΔctDNA可作为HR+/HER2- 晚期乳腺癌患者疗效评估与监测疾病进展的潜在指标
唯一OS显著获益:瑞波西利 是HR+/HER2-晚期乳腺癌一线治疗中唯一取得OS显著获益的CDK4/6抑制剂,其获益人群已扩展至早期患者
是HR+/HER2-晚期乳腺癌一线治疗中唯一取得OS显著获益的CDK4/6抑制剂,其获益人群已扩展至早期患者
N0患者复发风险不容忽视:NATALEE研究N0亚组患者中74%为T2N0,对照组3年iDFS率(90.6%)、DDFS率(91.5%)和DRFS率(92.5%)提示接受当前标准治疗的N0患者仍存在较高复发风险
N0亚组与总人群获益一致:NATALEE研究N0亚组分析显示,瑞波西利辅助强化治疗3年,降低复发风险28% ,(HR 0.723,93.2% vs 90.6%),与总体人群保持一致
立足生存,面向未来,瑞波西利为晚期HR+/HER2-乳腺癌患者续航希望
Q1:您在本次ASCO大会口头报告了Ⅲ期MONALEESA-3研究的最新分析结果,请您解读一下这一研究结果,并谈谈这一研究结果给我们带来了哪些临床启示?
Stephen Chia教授:MONALEESA-3研究证实,对比安慰剂+氟维司群 ,瑞波西利+氟维司群在HR+/HER2-晚期或转移性乳腺癌(ABC)一线/二线治疗中具有显著的无进展生存期(PFS)和总生存期(OS)双获益[1]。本次ASCO大会报告了MONALEESA-3研究患者治疗过程中ctDNA动态变化 (∆ctDNA)与PFS、OS和肿瘤大小的相关性,以及ctDNA可检测性与影像学进展的相关性,重点关注ctDNA是否可作为HR+/HER2- ABC早期疗效评估的潜在替代指标[2]。
,瑞波西利+氟维司群在HR+/HER2-晚期或转移性乳腺癌(ABC)一线/二线治疗中具有显著的无进展生存期(PFS)和总生存期(OS)双获益[1]。本次ASCO大会报告了MONALEESA-3研究患者治疗过程中ctDNA动态变化 (∆ctDNA)与PFS、OS和肿瘤大小的相关性,以及ctDNA可检测性与影像学进展的相关性,重点关注ctDNA是否可作为HR+/HER2- ABC早期疗效评估的潜在替代指标[2]。
研究在治疗第1周期第1天(C1D1)和第4周期第1天(C4D1)监测患者的ctDNA水平。结果显示,相对于安慰剂+氟维司群组,瑞波西利+氟维司群组从C1到C4 ctDNA水平的降幅更大(图1),并且 C1至C4的ΔctDNA与PFS/OS相关(P<0.0001,图2)。
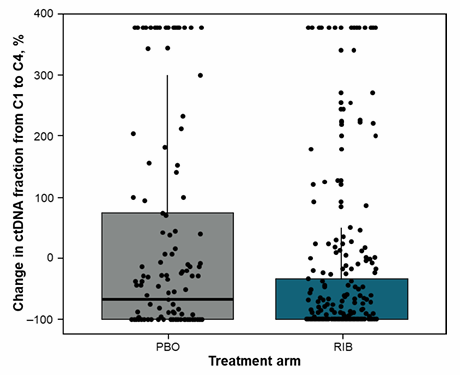
图1:安慰剂+氟维司群治疗组与瑞波西利+氟维司群治疗组从C1到C4的ctDNA水平变化
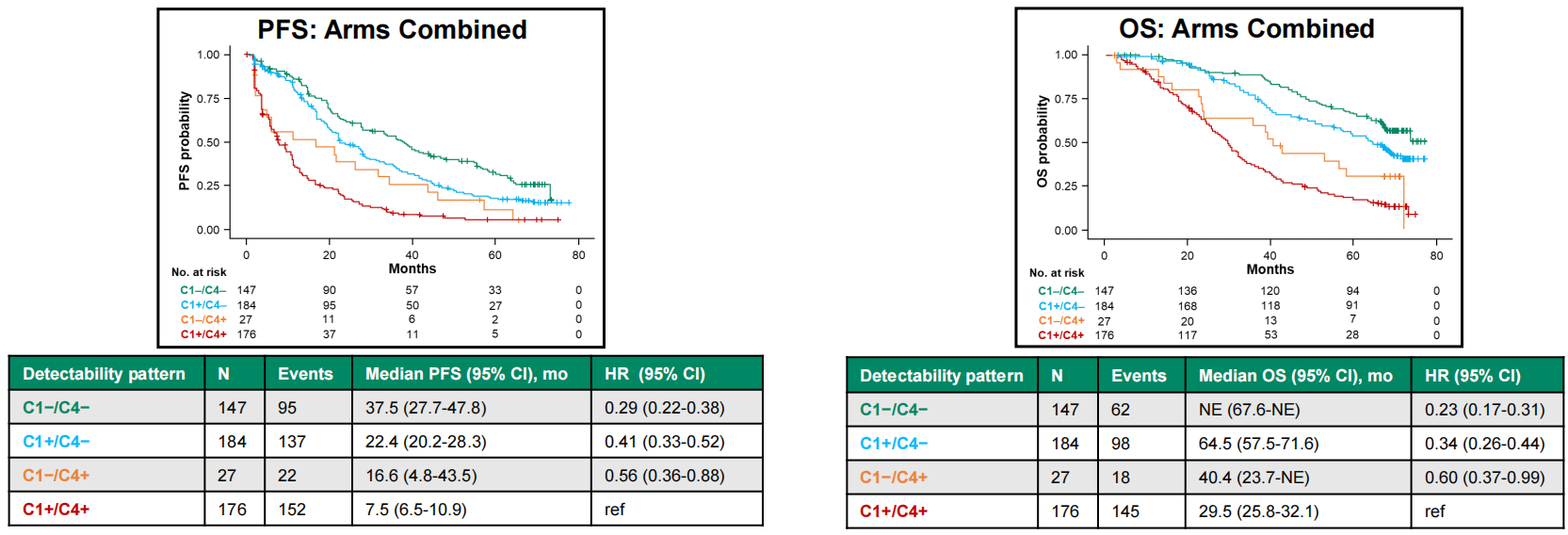
图2:从C1到C4的ctDNA水平与PFS、OS显著相关(P<0.0001)
有趣的是,如果将其作为风险分层,C1为阴性且C4仍为阴性(C1-/ C4-)的患者预后较好,PFS可达37.5个月;而C1+/ C4+的患者,PFS则较短,仅7.5个月。在达到部分缓解(PR)的患者中也出现了类似结果,C1-/ C4-的患者,中位PFS达到55.2个月;而C1+/ C4+的患者,PFS仅22.3个月(图3)。
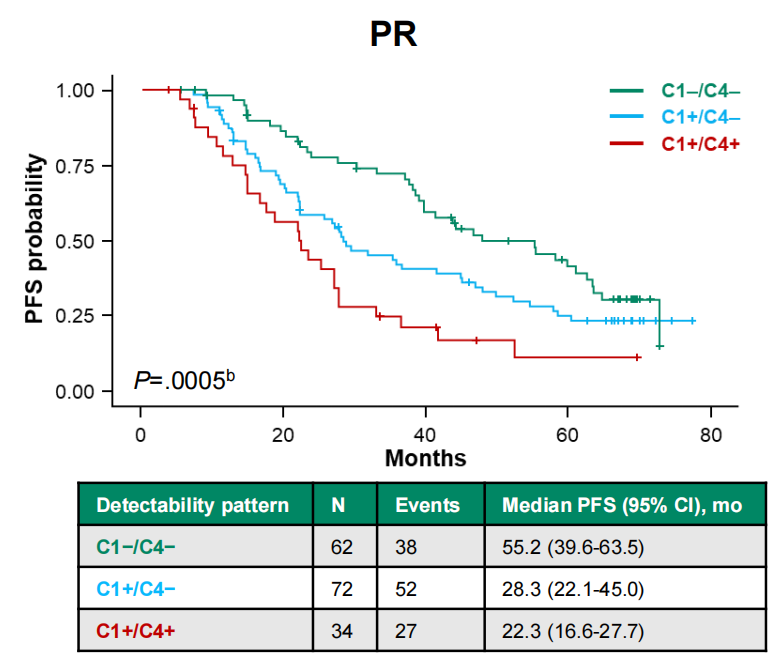
图3:PR患者从C1到C4的ctDNA水平与PFS
这一研究结果未来将如何应用于临床实践仍需进一步探索,并且需要从其他研究中得到证实。但可以设想的是,ΔctDNA可作为疗效评估与监测疾病进展的潜在指标。C1-/ C4-的患者,接受影像学检查的频率可降低;而C1+/ C4+的患者,可能需要考虑进入下一线治疗并接受更频繁的影像学检查。
Q2:请您结合研究和临床诊疗经验,谈谈目前我国不同CDK4/6抑制剂在HR+/HER2- 晚期乳腺癌一线及后线治疗中的应用现状及表现?
张剑教授:CDK4/6抑制剂是HR+/HER2-晚期乳腺癌患者的一线标准治疗方案。目前在中国有四种CDK4/6抑制剂:哌柏西利 、瑞波西利、阿贝西利
、瑞波西利、阿贝西利 、达尔西利
、达尔西利 ,但并非所有CDK4/6抑制剂都具有相同的疗效和安全性。
,但并非所有CDK4/6抑制剂都具有相同的疗效和安全性。
以OS这一临床较为关注的指标为例,目前CDK4/6抑制剂在HR+/HER2- ABC一线治疗的相关研究中,只有瑞波西利取得了OS显著获益。尤其是对于绝经前/围绝经期患者,MONALEESA-7研究是首项完全纳入绝经前/围绝经期HR+/HER2- ABC患者的Ⅲ期临床研究,结果显示相比安慰剂组,瑞波西利可显著延长患者的PFS(27.2 vs 13.0个月)和OS(58.7个月 vs 48.0个月),死亡风险降低24%(HR=0.76) [3]。而且不同CDK4/6抑制剂晚期一线治疗的副作用也各不相同,如有的CDK4/6抑制剂经常引起腹泻 ,有的则可能引起皮疹
,有的则可能引起皮疹 等。
等。
对于二线治疗,临床医生会重点关注患者一线治疗时是否接受过CDK4/6抑制剂,如未接受过,可参考MONALEESA-3研究,尝试使用CDK4/6抑制剂联合氟维司群;如果已接受过CDK4/6抑制剂治疗,则需要考虑更多因素,如通过基因检测确认通路是否改变等。目前很多药物(如PI3K/AKT/mTOR信号通路抑制剂)尚未在中国获批。CDK4/6抑制剂跨线治疗是一种不错的选择,MAINTAIN临床研究证明了瑞波西利跨线治疗的积极疗效。今年ASCO大会还公布了postMONARCH研究结果[4],该研究探索了阿贝西利二线治疗CDK4/6抑制剂一线治疗进展的HR+/HER2- ABC患者的疗效,但在研究入组的患者中,仅有8%的患者一线使用阿贝西利,并且研究者与BICR评估的PFS结果具有不一致性(研究者评估PFS:6.0个月 vs 5.3个月;BICR评估PFS:12.9个月 vs 5.6个月)。
Stephen Chia教授:目前北美市场已上市三种CDK4/6抑制剂:哌柏西利、瑞波西利、阿贝西利。如前所述,并非所有CDK4/6抑制剂都表现出OS显著获益。虽然临床很重视药物对PFS的改善结果,但患者可能更看重治疗方案能带来的OS获益,因此我认为在与患者商讨选择CDK4/6抑制剂时必须考虑到不同药物的OS表现。
Q3:瑞波西利是目前唯一一款在HR+/HER2- 晚期乳腺癌一线治疗中取得显著OS获益的CDK4/6抑制剂,您如何看待瑞波西利在晚期HR+/HER2-乳腺癌中的表现?
张剑教授:对于HR+/HER2-ABC一线治疗而言,MONALEESA-7研究证明了瑞波西利为绝经前/围绝经期患者带来的OS获益,MONALEESA-3研究也证实了一线瑞波西利+氟维司群相比安慰剂+氟维司群可带来显著OS获益(67.6个月 vs 51.8个月,HR 0.67,95%CI:0.50-0.90)[5]。亮眼的疗效数据奠定了瑞波西利在HR+/HER2-ABC一线治疗的标准地位。在临床实践中,PFS获益、生活质量获益等都是药物选择时的主要考察因素,而OS的改善是非常重要的研究指标之一。由于OS的显著获益,瑞波西利将为HR+/HER2-ABC临床实践提供重要支持。
更广人群,更广获益,瑞波西利为早期HR+/HER2-乳腺癌患者再启新篇
Q4:NATALEE研究探索了瑞波西利应用于HR+/HER2- 早期乳腺癌辅助治疗的疗效和安全性,您如何看待瑞波西利在早期HR+/HER2-乳腺癌中的表现?
王殊教授:CDK4/6抑制剂在HR+/HER2- ABC领域的研究已经获得许多阳性结果。而在HR+/HER2-早期乳腺癌(EBC)领域,目前关于CDK4/6抑制剂辅助治疗临床研究主要有三项:PALLAS研究、monarchE研究和NATALEE研究。很遗憾PALLAS研究结果为阴性 [6],monarchE和NATALEE研究则证明了CDK4/6抑制剂早期辅助治疗的获益,但两项研究入组人群不同[7,8]。monarchE研究仅纳入了部分淋巴结转移阳性(N+)早期高危患者,而NATALEE研究则纳入了更广泛的Ⅱ期/Ⅲ期患者,包括淋巴结转移阴性(N0)但具有高危因素(如G3或G2伴基因高危或伴KI67≥20%)的早期患者,与现实世界早期人群更为相似。
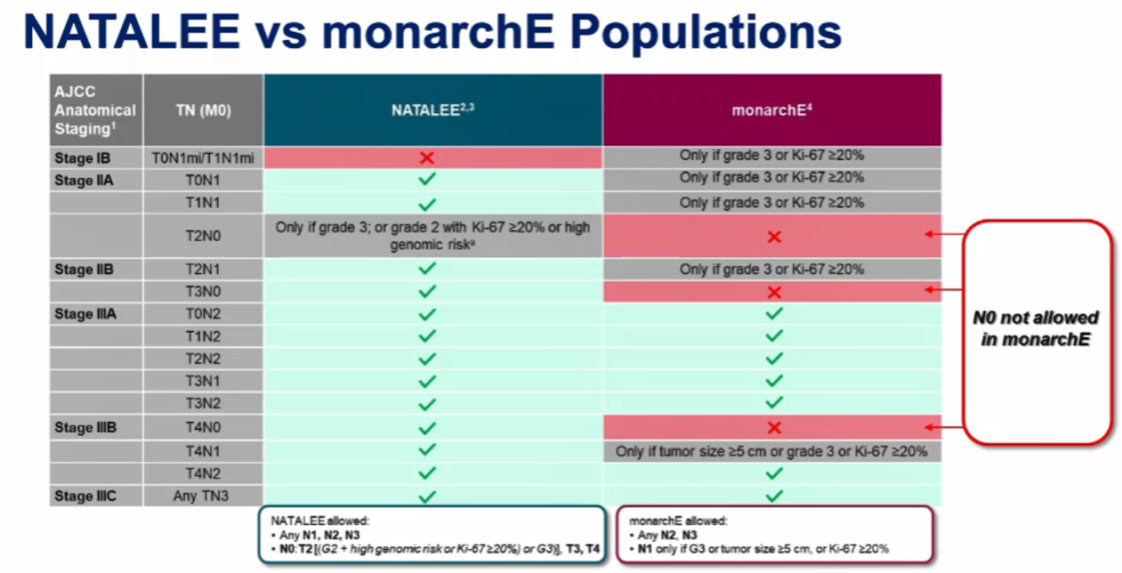
图4 NATALEE研究与monarchE研究入组人群对比
本次ASCO大会公布了NATALEE研究N0亚组研究数据[9],这部分人群在既往临床实践中普遍采用单纯内分泌治疗进行辅助治疗,但部分患者仍存在高复发风险因素,存在强化辅助治疗需求。NATALEE研究结果显示,N0亚组患者疗效获益及安全性表现与ITT人群一致,与单独内分泌治疗相比,瑞波西利联合内分泌辅助治疗 3 年,N0患者的疾病复发风险降低 27.7%(HR 0.723),远处疾病风险降低 29.7%(HR 0.703),远处复发风险降低 42%(HR 0.580);3年iDFS率(93.2% vs 90.6%)、3年无远处疾病生存(DDFS)率(94.3% vs 91.5%)和3年无远处复发生存(DRFS)率(96.3% vs 92.5%)均得到改善(图5)。本次结果为更广泛的HR+/HER2-EBC患者(包括N0患者)使用瑞波西利进行强化辅助治疗提供了循证证据。
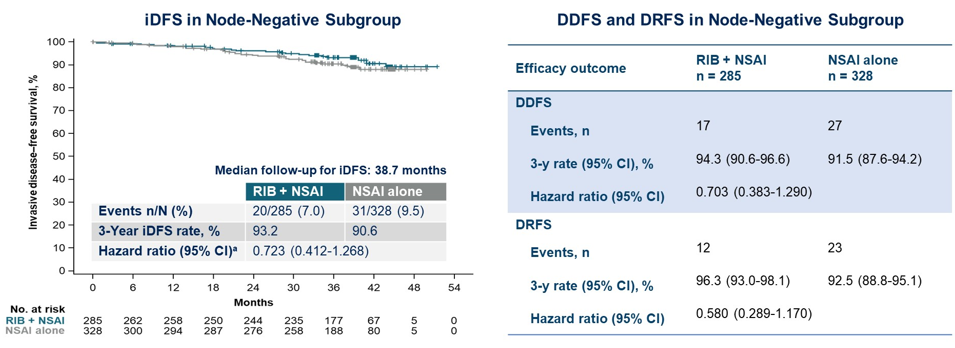
图5 NATALEE研究N0亚组主要研究结果
Q5:NATALEE研究结果支持瑞波西利+内分泌治疗作为II 期或III期HR+/HER2-早期乳腺癌患者(包括N0患者)的治疗选择,您如何看待N0患者的复发风险呢?
王殊教授:一般来说,对于患者复发风险的评估,我认为有两个重要因素值得重视。一个是患者的肿瘤负荷,另一个则是患者的分子分型。如果患者的肿瘤负荷为T1N0,临床通常认为其复发风险较低,如果患者的肿瘤负荷为T2N0,临床则认为其具有较高的复发风险。我们也会考虑患者的其他特征比如基因表达、肿瘤分型等因素,进一步确定患者属于高风险、中风险还是低风险患者。同时我们也会考虑患者组织学分级、Ki-67表达等因素。在既往临床研究中,研究者们更多关注高危患者,但多项研究提示,部分肿瘤负荷较低的患者也可能面临较高的复发风险,NATALEE研究结果提示我们,使用CDK4/6抑制剂升阶辅助治疗能够进一步降低早期患者复发风险,为这部分人群带来更多治疗获益。
Q6:NATALEE在所有淋巴结阳性(N+)患者和部分N0患者中都显著获益,若未来瑞波西利获批早期适应症,将如何改变化临床治疗决策?
张剑教授:NATALEE研究结果已经在国际著名期刊《The New England Journal of Medicine》发表[10]。瑞波西利在研究中展现了对于早期患者(包括N0患者)的显著疗效,未来如果瑞波西利能够获批早期辅助治疗适应症,在临床实践中我会特别关注N0患者。因为monarchE研究没有覆盖这类人群,但部分N0患者存在进一步降低复发风险的治疗需求,特别是伴高危因素的N0患者,瑞波西利可作为这一人群强化辅助治疗的选择。而对于monarchE研究与NATALEE研究交叉人群,我们会综合考虑药物疗效、安全性与生活质量等方面,帮助患者做出个性化的药物选择。
Stephen Chia教授:对于N0患者,临床比较常见的顾虑是早期使用CDK4/6抑制剂会不会造成过度治疗?今年ASCO大会上,我们看到NATALEE研究纳入的N0患者中,74%为T2N0(图6)。在仅接受三年随访的人群中,对照组复发的风险约为10%(iDFS率 90.6%),远处复发的风险的约为9%(DDFS 率 91.5%)(图5)。所以我认为,至少对于NATALEE研究入组的患者,复发风险是足够高的,需要考虑使用CDK4/6抑制剂瑞波西利进行强化辅助治疗。
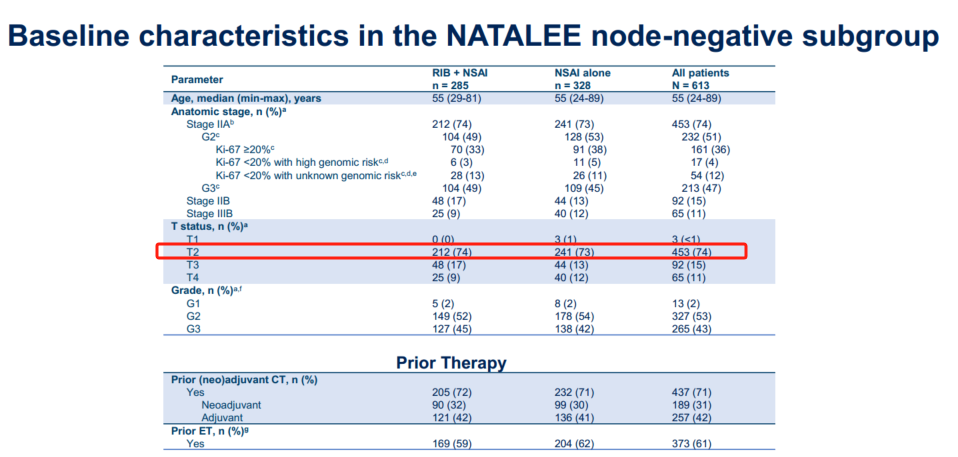
图6 NATALEE研究N0亚组入组人群特征
我们可以综合考量治疗持续时间、不良反应和治疗花费以及患者个体情况来帮助患者选择药物。如果患者≥4个转移淋巴结,monarchE研究数据已经证实了阿贝西利可以带来治疗获益,但并不是所有人都可以耐受阿贝西利治疗;如果淋巴结转移阳性的患者对阿贝西利不耐受,还可以使用瑞波西利;但对于N0患者,没有足够循证证据证明可以使用阿贝西利,则优选瑞波西利。未来我们仍需要更长时间的随访,就现在而言,能拥有更多的治疗选择对于患者而言就是好消息。
Q7:您对CDK4/6抑制剂在HR+/HER2-乳腺癌临床中的应用前景有哪些期待和展望?
Stephen Chia教授:HR+/HER2-乳腺癌是占比最多的乳腺癌,随着时间的推移,我们希望CDK4/6抑制剂能够为HR+/HER2-乳腺癌患者带来更多获益。同时我们也应该更准确地识别出哪些人群更需要CDK4/6抑制剂治疗。是否存在尚未发现的一些其它预测指标?是否需要进行基线ctDNA检测?这些问题都在研究中。就目前临床实践而言,更丰富的治疗选择会给予医生与患者更大的讨论与治疗空间,患者会根据自己的情况选择是否接受两到三年的CDK4/6抑制剂治疗。总之,对于HR+/HER2-乳腺癌,我们希望采取能够一些非化疗的治疗方案来降低复发风险。
全球合作,互为镜鉴,HR+/HER2-乳腺癌未来诊疗前景辽阔
Q8:2024年ASCO年会的主题是“癌症治疗的艺术与科学:从舒适到治愈”,肿瘤研究将改变实践并改善患者的生活。您如何看待CDK4/6抑制剂在HR+/HER2-早期乳腺癌取得的成绩,以及未来的发展前景?
王殊教授:从舒适到治愈,这是一个更宏大的目标,也是一个更复杂的过程,需要付出更多的努力。现在,早期HR+/HER2-乳腺癌患者拥有了更多CDK4/6抑制剂选择,这对于医患双方都是非常有益的。同时我们也需要更明智地选择,避免过度治疗或治疗不足。未来我们还有很长的路要走,包括探索更多生物标志物来更好地进行精准医疗,为患者找到最适合的治疗方法。在临床实践中,我们不仅需要考虑哪些患者能从早期强化辅助治疗中受益,还要权衡是否可以避免使用化疗。我们也需要综合考虑多方面因素,在不同文化背景和不同种族特征的背景下,我们更应该加强国际临床试验合作,共享研究数据,以更好地促进这一宏伟目标的实现。
Q9:随着临床研究的全球化,您认为未来各个国家有哪些相互学习或合作的方向和机会?
张剑教授:跨国研究非常重要。因为不同国家具有不同的文化背景与药物,我们应当共同进行一些新的临床试验。特别是目前在全球范围内涌现出许多以ADC为代表的新化合物,通过跨国研究,我们可以对比不同新化合物的疗效。因为大家共同的目标是令患者受益,我认为跨国研究能够令各国研究者积累更丰富的经验,并有助于我们更好地设计临床试验。同时我们也希望能够加快临床试验进程,更及时地为患者带来新的疗法,我相信跨国研究能够更快速地纳入大量患者并获得研究结果。
Stephen Chia教授:在临床研究领域,国际合作非常重要。其中种族问题值得引起我们重视。我曾参与了针对淋巴结阳性HR+/HER2-乳腺癌患者的RxPONDER试验[11],以观察是否存在基于种族的差异性结局。值得注意的是,我们发现非西班牙裔黑人患者的结局可能会更差,而在不同基因组的复发评分范围内,亚洲人群获得了具有统计学意义的显著获益。目前我们还无法确定其具体原因,可能与生物学有关,也可能与不同种族间不同的支持性环境或文化有关。未来还需要我们继续深入研究,但可以明确的是,我们不能对所有患者人群一概而论,因为在基因组多态性和环境因素方面,不同种族患者显然存在差异。





