
2024 ASCO|耿翠芝教授:瑞波西利再创佳绩,实现HR+/HER2-乳腺癌全人群获益!
瑞波西利 是国内首个获批用于绝经前/围绝经期晚期乳腺癌
是国内首个获批用于绝经前/围绝经期晚期乳腺癌 患者初始治疗的细胞周期蛋白依赖性激酶4/6(CDK4/6)抑制剂,自上市起就获得乳腺癌领域广泛关注,并迅速成为激素受体阳性(HR+)/人表皮生长因子受体2阴性(HER2-)晚期乳腺癌患者的主要治疗选择,该药物在乳腺癌领域的进展无疑是肿瘤学界的一大焦点。美国临床肿瘤学会(ASCO)年会是国际最具权威性的临床肿瘤学会议之一,致力于共享当前国际前沿发现和临床试验成果。据悉,瑞波西利在今年ASCO大会隆重亮相,带来了NATALEE研究N0亚组结果、MONALEESA-3研究ctDNA动态变化与生存获益相关性分析等多项重磅研究的最新结果。值此之际,医脉通诚挚邀请河北医科大学第四医院耿翠芝教授,为我们深入解读这些重要的研究成果,并展望瑞波西利在HR+/HER2-乳腺癌的治疗前景。
患者初始治疗的细胞周期蛋白依赖性激酶4/6(CDK4/6)抑制剂,自上市起就获得乳腺癌领域广泛关注,并迅速成为激素受体阳性(HR+)/人表皮生长因子受体2阴性(HER2-)晚期乳腺癌患者的主要治疗选择,该药物在乳腺癌领域的进展无疑是肿瘤学界的一大焦点。美国临床肿瘤学会(ASCO)年会是国际最具权威性的临床肿瘤学会议之一,致力于共享当前国际前沿发现和临床试验成果。据悉,瑞波西利在今年ASCO大会隆重亮相,带来了NATALEE研究N0亚组结果、MONALEESA-3研究ctDNA动态变化与生存获益相关性分析等多项重磅研究的最新结果。值此之际,医脉通诚挚邀请河北医科大学第四医院耿翠芝教授,为我们深入解读这些重要的研究成果,并展望瑞波西利在HR+/HER2-乳腺癌的治疗前景。
获益从晚期推进到早期:瑞波西利是 HR+/HER2-晚期乳腺癌一线治疗中唯一取得 OS 显著获益的 CDK4/6 抑制剂,多项III期试验证明瑞波西利的显著疗效,其晚期获益已拓展到早期辅助强化治疗。
ΔctDNA的潜力:MONALEESA-3研究提示,ΔctDNA与PFS/OS相关(P<0.0001),或可作为HR+/HER2-晚期乳腺癌患者疗效评估与监测疾病进展的潜在指标。
关注N0复发风险,实现全人群获益:NATALEE研究纳入的人群几乎覆盖所有需要辅助治疗的HR+/HER2-早期乳腺癌患者,结果提示N0患者复发风险不可忽视。经瑞波西利辅助强化治疗3年,N0亚组复发风险下降达28%(HR 0.723),与总体人群一致。

医脉通:HR+/HER2-乳腺癌是乳腺癌分型中最常见的一类,CDK4/6抑制剂为其诊疗格局带来了巨大变革。瑞波西利作为国内首款获批用于绝经前/围绝经期晚期乳腺癌患者初始治疗的CDK4/6抑制剂,在HR+/HER2-乳腺癌领域具有里程碑意义。请您结合临床经验谈谈瑞波西利在HR+/HER2-晚期乳腺癌中的应用现状?
耿翠芝教授:在乳腺癌领域,HR+/HER2-乳腺癌是占比最高的一种亚型,约占所有人群的70%[1]。对于HR+/HER2-晚期乳腺癌患者,目前治疗的主要目的是延长生存,改善患者生活质量。近年来,CDK4/6抑制剂的获批上市及临床应用极大地改变了HR+/HER2-乳腺癌的临床治疗模式,已获得国内外各大权威指南推荐。2024年发布的NCCN乳腺癌临床实践指南(2024. V2)显示[2],针对HR+/HER2-转移性乳腺癌患者,CDK4/6抑制剂联合芳香化酶抑制剂(AI)组合是一线治疗方案。
瑞波西利是CDK4/6抑制剂的代表药物之一,既往已开展了多项Ⅲ期研究。MONALEESA-2研究首次报告了CDK4/6抑制剂显示出显著统计学意义的长期总生存期(OS)获益[3]。瑞波西利+来曲唑 相比安慰剂+来曲唑治疗绝经后HR+/HER2–晚期乳腺癌患者中位OS延长超过12个月(63.9个月vs 51.4个月;HR 0.76;95%CI:0.63-0.93,P=0.004),取得显著OS获益。
相比安慰剂+来曲唑治疗绝经后HR+/HER2–晚期乳腺癌患者中位OS延长超过12个月(63.9个月vs 51.4个月;HR 0.76;95%CI:0.63-0.93,P=0.004),取得显著OS获益。
MONALEESA-7研究是首项完全纳入绝经前/围绝经期HR+/HER2-晚期乳腺癌的Ⅲ期临床研究,在意向治疗(ITT)人群中,瑞波西利相比安慰剂一线治疗绝经前/围绝经期人群能够显著延长患者的中位OS(58.7个月 vs 48.0个月),并且在多个亚组中(包括接受NSAI治疗的患者)均观察到较好的OS获益[4]。
RIGHT Choice研究,聚焦绝经前/围绝经期且具有侵袭性疾病特征(合并内脏转移甚至内脏危象)的HR+/HER2-晚期乳腺癌患者,结果显示对比传统的联合化疗方案,一线瑞波西利联合治疗亚洲患者显著延长中位无进展生存期(PFS)超1年(25.2个月 vs 11.2 个月;HR 0.48)[5],使HR+/HER2-乳腺癌内脏危象患者有可能免除化疗。
以瑞波西利为代表的CDK4/6抑制剂显著改善了HR+/HER2-晚期乳腺癌患者的治疗结局,为更多乳腺癌患者带来了新的希望。
医脉通:本次ASCO大会公布了瑞波西利Ⅲ期MONALEESA-3研究的最新分析结果,探索了ctDNA动态变化 (∆ctDNA)与HR+/HER2-晚期乳腺癌患者生存的相关性。请您对研究结果进行解读,并分享您对该结果的看法?
耿翠芝教授:MONALEESA-3研究是一项随机、双盲、安慰剂对照的III期临床研究,纳入726例绝经后的HR+/HER2-晚期或转移性乳腺癌患者,随机接受瑞波西利+氟维司群 或安慰剂+氟维司群一线治疗。既往结果显示,瑞波西利+氟维司群一线治疗HR+/HER2-晚期乳腺癌患者的中位OS[6](67.6个月 vs 51.8个月;HR 0.67,95%CI:0.50-0.90)和中位PFS[7](33.6个月 vs 19.2个月;HR 0.55,95%CI:0.42-0.72)均显著优于安慰剂+氟维司群。
或安慰剂+氟维司群一线治疗。既往结果显示,瑞波西利+氟维司群一线治疗HR+/HER2-晚期乳腺癌患者的中位OS[6](67.6个月 vs 51.8个月;HR 0.67,95%CI:0.50-0.90)和中位PFS[7](33.6个月 vs 19.2个月;HR 0.55,95%CI:0.42-0.72)均显著优于安慰剂+氟维司群。
本次ASCO大会报告了MONALEESA-3 研究治疗中ctDNA的变化与PFS、OS和肿瘤大小的相关性,以及ctDNA可检测性与影像学进展的相关性[8]。与安慰剂+氟维司群相比,瑞波西利+氟维司群的ctDNA水平从C1到C4的降幅更大(P=0.003,图1),并且治疗时 C1至C4的ΔctDNA与PFS/OS相关(P<0.0001,图2),这表明瑞波西利+氟维司群可能比安慰剂+氟维司群更早有效。
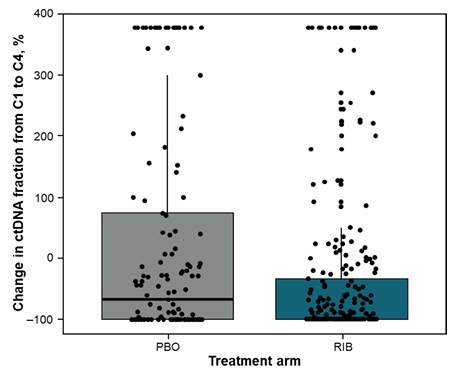
图1:安慰剂+氟维司群治疗组与瑞波西利+氟维司群治疗组从C1到C4的ctDNA水平变化
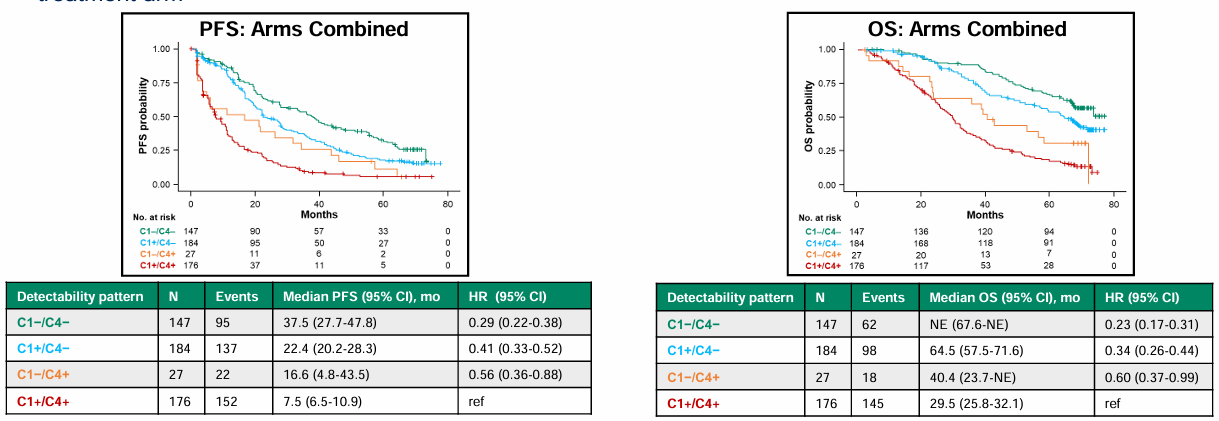
图2:从C1到C4的ctDNA水平与PFS、OS显著相关(P<0.0001)
在对C4D1(C4-)清除ctDNA的患者的纵向分析中,ctDNA进展与影像学进展之间的中位间隔时间为8.2个月(IQR,4.5-15.6)。表明检测ΔctDNA可能是一种监测疾病进展的灵敏方法,ΔctDNA可能是HR+/HER2-晚期乳腺癌患者疗效评估的潜在替代指标。
医脉通:ctDNA水平与肿瘤负荷和治疗效果的变化密切相关,ctDNA的变化在预测治疗效果方面有时甚至优于标准肿瘤标志物。正如MONALEESA-3研究中对ctDNA的分析,显示出了ctDNA的实用性,请您谈谈ctDNA监测在乳腺癌的筛查与治疗中有什么价值?您认为ctDNA是否有可能替代常用的疗效指标?
耿翠芝教授:ctDNA正越来越多地被用作指导临床决策,以实现更好的诊断、监测疾病进展和疾病复发风险等。
在乳腺癌的诊断及分型方面,ctDNA可作为辅助诊断工具。乳腺癌患者相比良性乳腺疾病或健康人群的ctDNA含量增加,并且晚期肿瘤中ctDNA浓度更高[9]。ctDNA分析还可确定PI3KCA突变状态,辅助判断乳腺癌分型[10]。在监测疾病进展方面,ctDNA可作为辅助检测手段。PIK3CA等部分热点突变在组织活检中难以发现,但在疾病进展过程中ctDNA能可靠地被发现[10]。本次大会公布的MONALEESA-3研究最新数据也表明,ctDNA的动态变化可能是一种监测疾病进展的灵敏方法。在监测疾病复发风险方面,ctDNA持续出现可检测突变与早期复发的高风险相关,可及时给出是否出现耐药性或疾病转移的判断,识别复发风险极高的患者[10]。
尽管治疗后对ctDNA的连续分析能够预测肿瘤的治疗反应,并比标准影像学方法更早发现疾病进展,但在临床实际应用中使用这些数据指导治疗决策的方案尚未确定,因此不建议在临床试验之外将ctDNA分析用于这一情况[11]。不过,随着诊疗技术的不断发展,我们对乳腺癌的了解也在不断深入,期待未来ctDNA在乳腺癌的应用能更加广泛。
医脉通:瑞波西利在HR+/HER2-晚期乳腺癌 MONALEESA 系列研究中均取得OS的阳性结果,并且光环映射到早期患者。本次ASCO大会公布了NATALEE研究N0 亚组患者的最新数据,您如何看待这一结果?能否结合该数据与您的实际管理经验,谈谈对于N0伴高危复发风险因素患者的临床治疗管理策略?
耿翠芝教授:NATALEE是一项III期研究,旨在评估瑞波西利联合内分泌治疗对于存在复发风险的HR+/HER2- 早期乳腺癌广泛患者人群的疗效。与阿贝西利 的monarchE研究相比,NATALEE研究纳入了更广泛的Ⅱ期和Ⅲ期HR+/HER2-早期乳腺癌患者(包括无淋巴结转移),几乎涵盖了所有需要进行辅助治疗的乳腺癌患者(Ⅱ期,T2N0[Grade 2且基因检测高复发风险或Ki67超过20%,Grade3],Ⅲ期)。2023年SABCS大会披露了NATALEE研究最终无浸润性疾病生存期(iDFS)数据[12],与单独内分泌治疗相比,瑞波西利联合内分泌治疗的3年iDFS率显著更优(3年iDFS率:90.7% vs 87.6%,HR 0.749;95%CI:0.628-0.892;P=0.0006),复发风险显著降低25.1%。
的monarchE研究相比,NATALEE研究纳入了更广泛的Ⅱ期和Ⅲ期HR+/HER2-早期乳腺癌患者(包括无淋巴结转移),几乎涵盖了所有需要进行辅助治疗的乳腺癌患者(Ⅱ期,T2N0[Grade 2且基因检测高复发风险或Ki67超过20%,Grade3],Ⅲ期)。2023年SABCS大会披露了NATALEE研究最终无浸润性疾病生存期(iDFS)数据[12],与单独内分泌治疗相比,瑞波西利联合内分泌治疗的3年iDFS率显著更优(3年iDFS率:90.7% vs 87.6%,HR 0.749;95%CI:0.628-0.892;P=0.0006),复发风险显著降低25.1%。
本次大会更新报告了N0亚组患者的疗效和安全性[13]。数据显示N0亚组患者与ITT人群获益一致,与单独内分泌治疗相比,瑞波西利联合内分泌辅助治疗3年,N0患者的疾病复发风险降低27.7%(HR 0.723),远处疾病风险降低29.7%(HR 0.703),远处复发风险降低42%(HR 0.580);3年iDFS率(93.2% vs 90.6%)、3年无远处疾病生存(DDFS)率(94.3% vs 91.5%)和3年无远处复发生存(DRFS)率(96.3% vs 92.5%)率均更高(图3)。安全性分析显示,N0亚组患者的安全性与ITT人群一致。本次结果支持在复发风险增加的HR+/HER2-早期乳腺癌患者(包括N0患者)中使用瑞波西利。
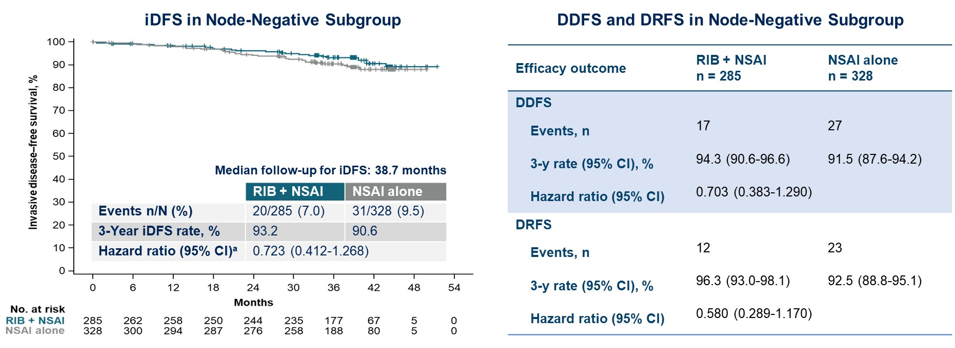
图3:N0亚组患者的iDFS、DDFS和DRFS
对于HR+/HER2-早期乳腺癌患者而言,不论疾病分期和淋巴结状态如何,短期及长期复发风险始终存在。患者在术后2~3年将面临第一个复发高峰,而在完成5年内分泌辅助治疗之后,超过半数的患者仍面临长期复发风险,并且其复发风险随时间延长递增。NATALEE研究对照组结果(图3)同样提示,即使是N0乳腺癌患者,其复发风险也不容忽视。但在临床决策中,早期患者的复发风险往往被低估,未来临床医生需重视这部分患者的复发风险,给予必要的辅助强化治疗。
总的来说,CDK4/6抑制剂改写了HR+/HER2-晚期乳腺癌的治疗格局,随着monarchE、NATALEE等研究结果的不断公布,CDK4/6抑制剂在早期乳腺癌患者中的应用前景也愈加广阔。NATALEE研究将瑞波西利的获益人群从晚期阶段前移至早期辅助治疗阶段,本次ASCO公布的N0亚组则提示更广泛的Ⅱ期和Ⅲ期HR+/HER2-早期乳腺癌患者能够从瑞波西利辅助治疗中获益。未来,随着诊疗技术的不断进步以及CDK4/6抑制剂在乳腺癌领域的深入探索,我们期待乳腺癌获益人群能够进一步扩大,整体治疗效果能够进一步提升!

