在一起 成就治愈丨赵欣教授解读:全能6边形战士,阿来替尼多维实力“名列前茅”,助力患者全方位获益!
我国是世界上肺癌负担较重的国家之一,2022年,肺癌新发与死亡患者数分别约为106.06万例与73.33万例,高居所有癌症首位,不仅对国民生命健康产生了极大威胁,也为患者带来了巨大的生活负担。其中,间变性淋巴瘤激酶(ALK)阳性肺癌是非小细胞肺癌(NSCLC)的独特分子亚型,约占NSCLC发病的3%-7%[1,2]。ALK-酪氨酸激酶抑制剂(TKI)的出现使得ALK阳性晚期NSCLC患者生存得到显著延长,晚期患者亦看到了获得“治愈”的曙光。作为目前临床一线应用最为广泛的ALK-TKI,阿来替尼 究竟有何特点与优势?其又是如何获得临床众多医生与患者青睐的?且看江苏省人民医院赵欣教授为我们娓娓道来。
究竟有何特点与优势?其又是如何获得临床众多医生与患者青睐的?且看江苏省人民医院赵欣教授为我们娓娓道来。
实践出真知,6年中国临床实践经验
为患者铸造生存传奇
ALK突变又被称为“钻石突变”,不仅因为其发生率相对较低,更是因为此类型患者预后往往较好。ALEX、ALESIA等多项研究显示,以阿来替尼为代表的二代ALK-TKI显著延长了患者生存,不仅使阿来替尼成为了ALK阳性患者的“优先选择”,也正式拉开了ALK阳性晚期NSCLC“慢病化管理”时代的序幕[3-6]。但随着研究的不断深入,新型药物的不断研发,ALK阳性晚期NSCLC临床诊疗策略也在随之发生着变化。
前不久2024美国临床肿瘤学会(ASCO)年会于芝加哥顺利召开,会上CROWN研究五年PFS数据得以公布,再一次激起了业内关于如何为ALK阳性晚期NSCLC患者制定临床治疗方案的激烈讨论[7]。如今,国内临床已先后有7款ALK-TKI获批上市,并呈现出了“三代同堂”的局面,而不同代际药物间各有特点,ALK阳性晚期NSCLC一线治疗药物如何选择是当下临床医生与患者所关注的焦点。
为使患者获得最佳生存获益,一线治疗药物的选择至关重要,这不仅为患者临床诊疗奠定了基础,也会对患者后续治疗产生深远影响,“2+X”方案与“3+X”方案究竟孰优孰劣是目前ALK阳性晚期NSCLC临床诊疗领域最具争议的话题,随着抗肿瘤治疗药物的不断研发,患者生存必然将会不断得到延长,因此为确保患者可长期稳定的接受药物治疗并帮助患者可以拥有“高质量长生存”,医生为患者所选择的治疗药物须同时兼顾“疗效”、“安全性”与“可及性”。
2024 ASCO年会上所公布的CROWN研究五年PFS数据显示,洛拉替尼 用于ALK阳性晚期NSCLC一线接受治疗,可为患者带来60%的5年PFS率,使患者看到了获得“临床治愈”的希望[7]。不过值得一提的是,相关Meta分析显示,在ALK阳性晚期NSCLC一线治疗中,阿来替尼可为亚洲患者带来了不输于洛拉替尼的无进展生存(PFS)获益,且在目前所有ALK-TKI中可为患者带来最大的总生存(OS)获益趋势,是目前唯一相较于一代ALK-TKI,在III期研究中表现出明显的5年OS率获益趋势的ALK-TKI[8,9]。
用于ALK阳性晚期NSCLC一线接受治疗,可为患者带来60%的5年PFS率,使患者看到了获得“临床治愈”的希望[7]。不过值得一提的是,相关Meta分析显示,在ALK阳性晚期NSCLC一线治疗中,阿来替尼可为亚洲患者带来了不输于洛拉替尼的无进展生存(PFS)获益,且在目前所有ALK-TKI中可为患者带来最大的总生存(OS)获益趋势,是目前唯一相较于一代ALK-TKI,在III期研究中表现出明显的5年OS率获益趋势的ALK-TKI[8,9]。
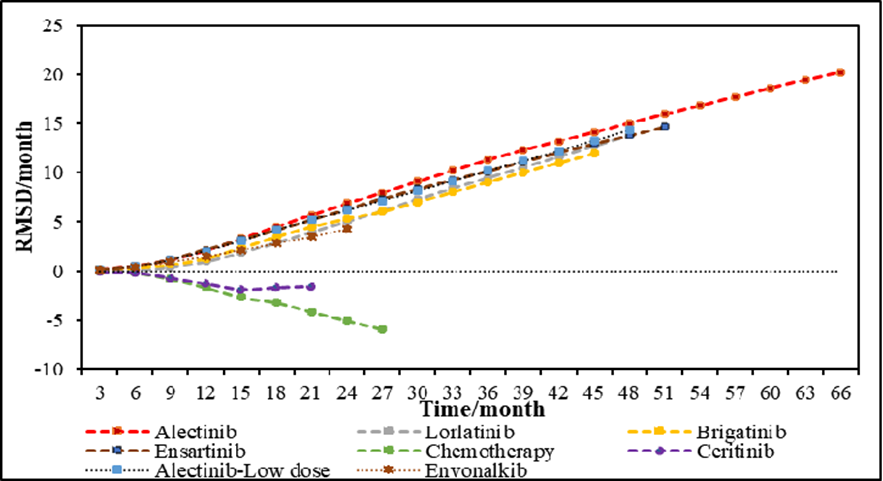
图1 阿来替尼一线治疗各时间节点PFS均优于其他ALK-TKI或化疗
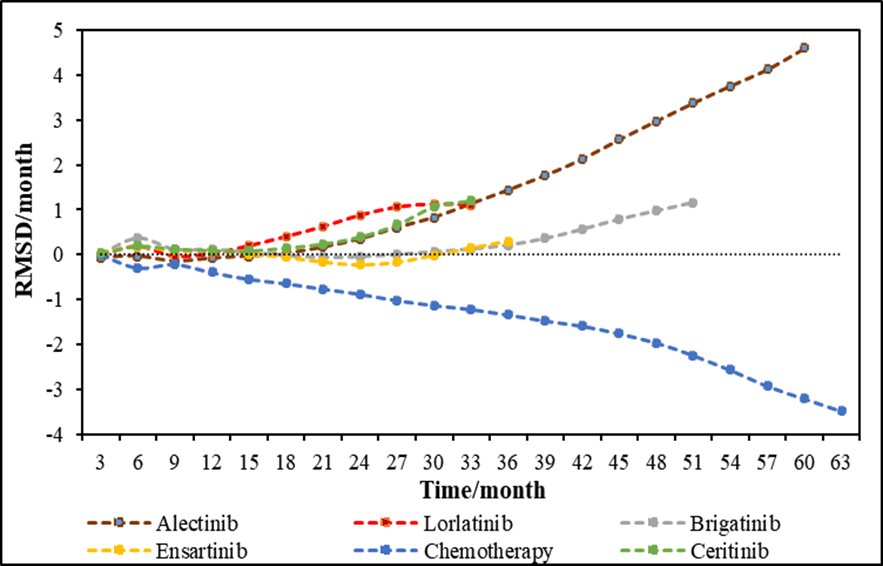
图2 阿来替尼一线治疗OS平均改善水平最高
不仅如此,作为一款上市6年的“经典”药物,其临床疗效得到了真实世界的反复验证,此前国内一项纳入127例TKI初治或经治ALK阳性晚期NSCLC患者的真实世界研究(RWS)显示,阿来替尼在总体人群中,1年与2年PFS率与临床试验结果具有一致性[10]。该研究显示,与后线治疗患者相比,接受阿来替尼一线治疗的患者具有更高的ORR且安全性良好,与多项ALK-TKI用于ALK阳性晚期NSCLC一线治疗的相关随机对照研究(RCT)数据持平或更优,证明其承受住了临床实践的检验。
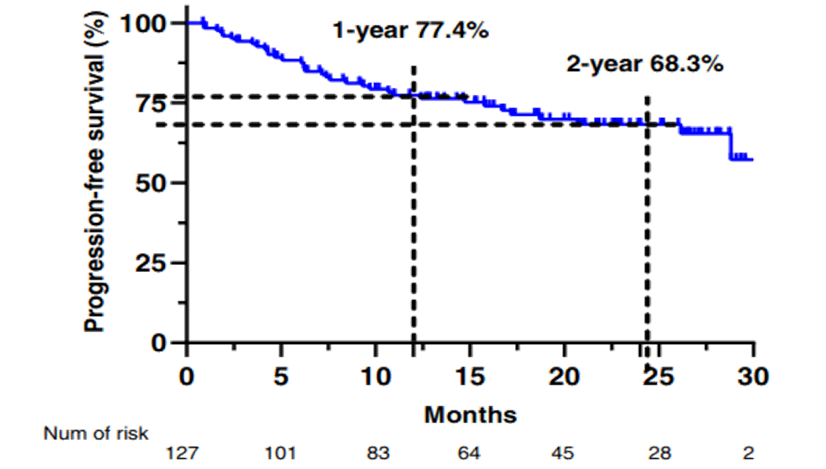
图3 真实世界患者接受阿来替尼治疗PFS数据
六边形战士全都要:
安全性、可及性兼顾方可成为临床优选
ALK-TKI“三代同堂”的盛世,不仅仅只是帮助患者PFS、OS数值得到了提升,也为患者带来了获得“治愈”的希望。虽然ALK-TKI取得了十分卓越的疗效数据,但仅凭这一点并不能够为患者制定出最佳的治疗方案,尤其是考虑到如今“延长生存”已不再是患者唯一的治疗需求,“高质量长生存”已成为患者治疗的更高目标,这便需要医生站在全程管理的角度,从药物的安全性、对患者生活质量的影响以及患者耐药后的治疗选择等多个维度进行评估从而为患者制定治疗方案,赵欣教授强调。
ALESIA研究显示,阿来替尼用于亚裔患者一线治疗3级及以上AE发生率仅为48%,不仅优于多数ALK-TKI相关在同类型研究中的所表现出的数据,也是目前唯一一个在RCT中3-4级AE发生率低于克唑替尼 的ALK-TKI,在导致患者治疗药物减少、治疗间断或治疗终止相关AE方面,阿来替尼同样表现出了优于克唑替尼的数据[5,6]。2023世界肺癌大会(WCLC)中所公布的一项匹配调整间接比较(MAIC)分析数据提示,阿来替尼安全性相对更好,3级及以上AE发生风险明显更低[11]。
的ALK-TKI,在导致患者治疗药物减少、治疗间断或治疗终止相关AE方面,阿来替尼同样表现出了优于克唑替尼的数据[5,6]。2023世界肺癌大会(WCLC)中所公布的一项匹配调整间接比较(MAIC)分析数据提示,阿来替尼安全性相对更好,3级及以上AE发生风险明显更低[11]。
不仅如此,相关Meta分析显示,阿来替尼在患者治疗过程中引起的呼吸系统、神经系统、心血管系统、消化系统和泌尿系统SAE发生率均相对更低[12]。此外RWS显示,与克唑替尼相比,阿来替尼可为患者带来更具优势的无主要不良事件生存期(mAEFS,NR vs. 91.3个月;HR=0.63;95%CI:0.30-1.30;P=0.224),可见阿来替尼在安全性方面具有很好的优势[13]。
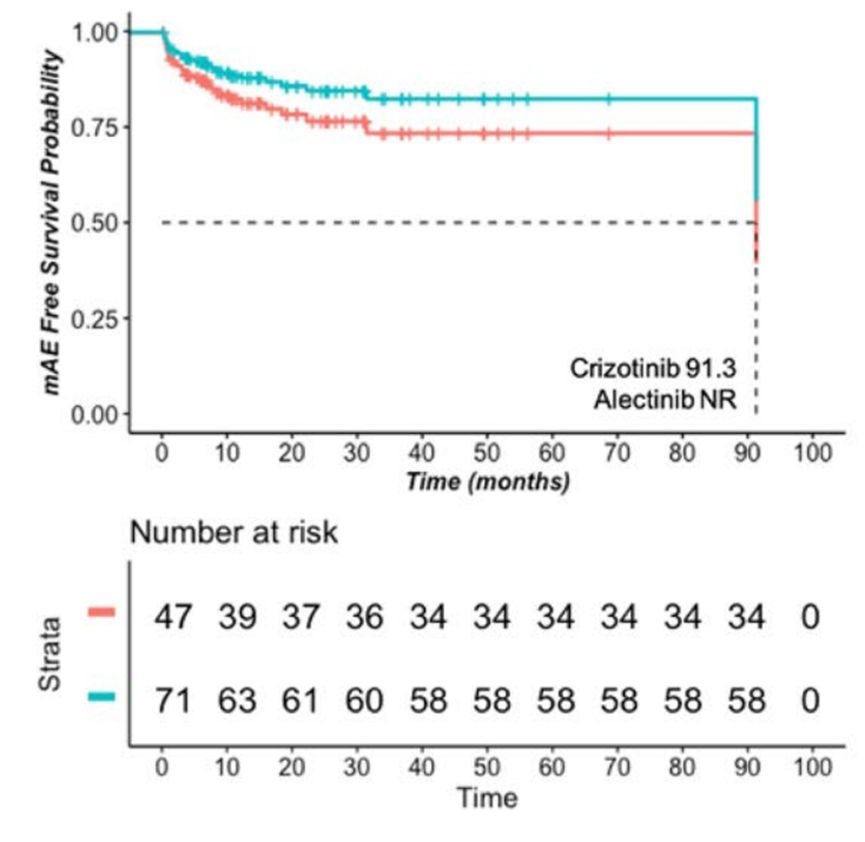
图4 真实世界患者接受阿来替尼治疗mAEFS数据
与此同时,临床中肿瘤患者往往会合并有其它慢性基础病,一项关于阿来替尼等ALK-TKI药代动力学(PK)特点总结的研究显示,与其他ALK-TKI相比,阿来替尼和其他基础疾病药物合用时安全性良好,在与CYP3A代谢的药物同用时,不需要进行过多的剂量调整,这从侧面再一次验证了阿来替尼的安全性优势[14]。现有的三代ALK-TKI,每一代药物均有其独特的AE谱以及PK特征,因此在为患者选择治疗药物时,要充分考虑患者临床特征,赵欣教授说道。
除药物疗效与安全性外,药物的可及性亦会对患者临床治疗造成较大影响,既往多项药物经济学分析显示,与一代ALK-TKI相比,阿来替尼等二代ALK-TKI经济性要显著更优,而与三代ALK-TKI相比,阿来替尼一线治疗ALK阳性晚期NSCLC同样具有一定成本-效益优势[15,16]。
有研究通过文献综述和专家访谈的形式,从疗效、安全性、经济性、适用性、可及性和创新性等多个维度,对6款一、二、三代ALK-TKI进行了定量和定性的综合评价。结果显示,阿来替尼替尼在各个方面的评估中均获得了“数一数二”的成绩,医生对其的推荐程度以及患者接受治疗时的依从性也相对更优,提示其具有更高的综合临床价值[17]。不仅如此,二代ALK-TKI的耐药机制及相对更为明确,这可使患者后线治疗拥有继续接受精准靶向治疗的可能性,进一步提升了患者的总体获益。
赵欣教授表示,同时兼具优异的疗效、出色的安全性以及亲民的可及性是国内多种慢性基础病治疗药物的最大特点,因此帮助ALK阳性晚期NSCLC实现“慢病化”最重要的一环便是使患者拥有一款或多款可以兼顾疗效、安全性与可及性,且不会对患者其它疾病治疗产生过多影响的抗肿瘤治疗药物。此外,鉴于恶性肿瘤的特殊性,越来越多的肺癌临床工作者意识到“全程管理”在患者诊疗过程中的重要性,因此从全程角度出发在为患者选择治疗药物时,优先选择耐药机制明确,可使患者最大程度接受精准靶向治疗的选项或是患者更佳的治疗方案。
总结
目前,《中国临床肿瘤学会(CSCO)非小细胞肺癌诊疗指南2024》中将阿来替尼、布格替尼 以及洛拉替尼列为ALK阳性晚期NSCLC一线治疗“优先推荐”治疗药物,其中阿来替尼更是从《中国临床肿瘤学会(CSCO)原发性肺癌诊疗指南2019》起便在所有TKI中率先获得“优先推荐”并延续至今,充分证明了临床医生对其疗效、安全性与可及性的认可[18-23]。基于此,阿来替尼也成为了临床医生更愿推荐,患者更愿使用的ALK-TKI。如今,随着临床研究的深入,ALK-TKI的临床应用边界目前也逐渐拓展到了早期NSCLC围术期治疗,相信基于ALINA研究的探索,阿来替尼在不久的将来将成为一款可覆盖ALK阳性NSCLC全病程患者,引领临床ALK阳性NSCLC临床诊疗变革。
以及洛拉替尼列为ALK阳性晚期NSCLC一线治疗“优先推荐”治疗药物,其中阿来替尼更是从《中国临床肿瘤学会(CSCO)原发性肺癌诊疗指南2019》起便在所有TKI中率先获得“优先推荐”并延续至今,充分证明了临床医生对其疗效、安全性与可及性的认可[18-23]。基于此,阿来替尼也成为了临床医生更愿推荐,患者更愿使用的ALK-TKI。如今,随着临床研究的深入,ALK-TKI的临床应用边界目前也逐渐拓展到了早期NSCLC围术期治疗,相信基于ALINA研究的探索,阿来替尼在不久的将来将成为一款可覆盖ALK阳性NSCLC全病程患者,引领临床ALK阳性NSCLC临床诊疗变革。