
董吁钢教授:防治ASCVD,LDL-C到底有没有下限 | OCC-WCC 2024
动脉粥样硬化性心血管疾病(ASCVD)是我国城乡居民死亡的主要原因,血脂异常是导致此类疾病的重要危险因素之一。低密度脂蛋白胆固醇(LDL-C)水平越高,暴露于异常LDL-C水平时间越长,罹患ASCVD的风险越高。因此,有效控制血脂异常对我国ASCVD防控具有重要意义。那么,LDL-C是否降得越低越好?在ASCVD二级预防中,LDL-C到底有没有下限?在第十八届东方心脏病学会议和世界心脏病学大会(OCC-WCC 2024)期间,中山大学附属第一医院董吁钢教授就这一问题阐述了自己的观点。
极高危人群:ASCVD风险与LDL-C控制
1.指南进展
随着循证证据的积累,对于ASCVD极高危人群,各国指南推荐的LDL-C管理目标值越来越低。
√2018 ACC/AHA指南中提到,目前的研究奠定了对于LDL-C控制“越低越好”的总体原则。
√2019 ESC/EAS指南中提到,在整个LDL-C水平范围内“越低越好”,没有最低限,至少小于1mmol/L。该指南建议,极高危人群的LDL-C水平较基线降低≥50%且目标值<1.4mmol/L(55mg/dL);如果2年内反复发生事件,可考虑将LDL-C降至<1.0mmol/L。
√中国指南在危险分层方面可能与欧美指南有所不同,即在极高危之上增加了超高危人群。根据中国血脂管理指南(2023)推荐,极高危人群LDL-C的目标值<1.8mmol/L且较基线降低幅度>50%;超高危人群LDL-C的推荐目标值为<1.4mmol/L,且叫基线降低幅度>50%。
表1 各国指南极高危人群LDL-C指南推荐目标值
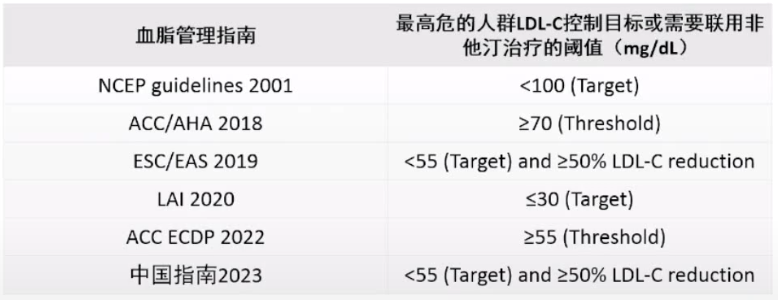
现在公认的原则是“LDL-C低一点,好一点”。那么防治ASCVD,LDL-C到底有没有下限?
2.循证证据
早年仅有他汀类药物可用于降脂,绝大多数患者达不到较低的目标值。近年来,血脂领域发展日新月异,各类新型降脂药物不断涌现。大多数患者降脂药物单药或联合治疗可达到理想的目标值。
(1)LDL-C低一些,好一些
IMPROVE-IT研究是他汀联合胆固醇吸收抑制剂依折麦布 的相关研究。该研究中,两组患者入组时的平均基线LDL-C水平均为93.8 mg/dl,1年后他汀单药治疗组和他汀+依折麦布联合治疗组的平均LDL-C水平分别为69.9 mg/dl和53.2 mg/dl(P<0.001),16.7 mg/dl的差值代表LDL-C进一步降低了24%。
的相关研究。该研究中,两组患者入组时的平均基线LDL-C水平均为93.8 mg/dl,1年后他汀单药治疗组和他汀+依折麦布联合治疗组的平均LDL-C水平分别为69.9 mg/dl和53.2 mg/dl(P<0.001),16.7 mg/dl的差值代表LDL-C进一步降低了24%。
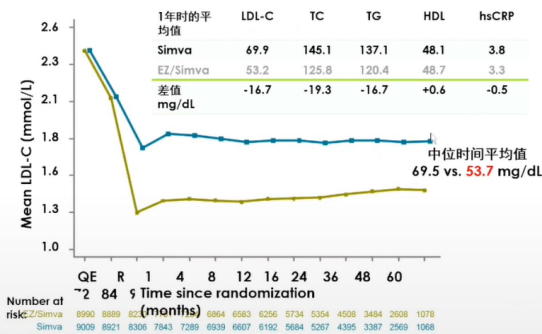
图1 IMPROVE-IT:LDL-C及血脂谱改变
在该研究的主要终点方面,联合治疗组和他汀单药治疗组的7年事件(Kaplan-Meier)曲线主要终点事件发生率分别为32.7%和34.7%(绝对风险降低2%;相对风险降低6.4%)。
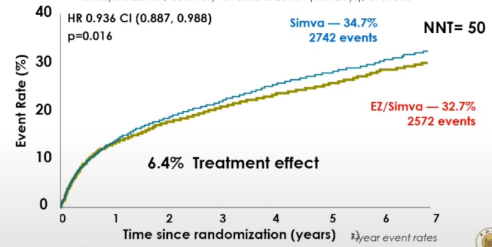
图2 主要终点分析
IMPROVE-IT研究率先催生LDL-C走向更低的基本方向,证实了LDL-C低一些好一些。
(2)极低LDL-C的心血管获益
FOURIER试验和ODYSSEY OUTCOMES试验分别在已有动脉粥样硬化心脏病患者和近期发生ACS的患者中,证实了PCSK9抑制剂在高风险ASCVD人群中的疗效,可在他汀治疗基础上进一步降低LDL-C水平达50%以上,并降低患者心血管事件风险。
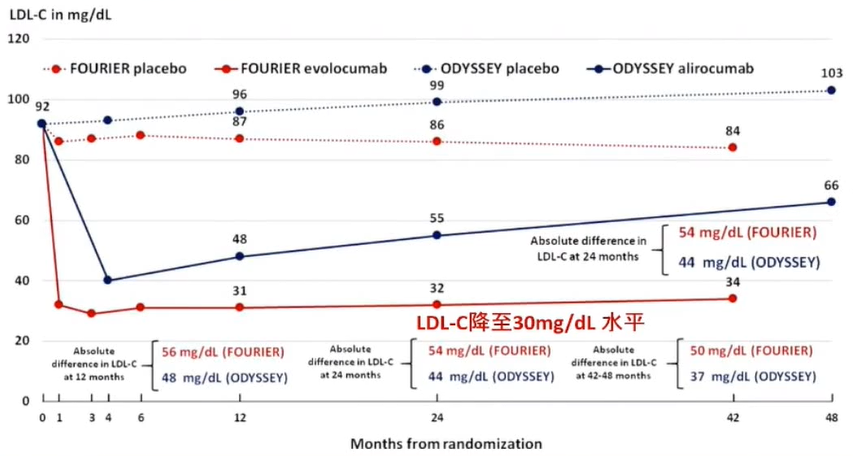
图3 FOURIER试验和ODYSSEY OUTCOMES试验中依洛尤单抗 和阿利西尤单抗
和阿利西尤单抗 降LDL-C效果
降LDL-C效果
FOURIER试验中,使用依洛尤单抗使LDL-C降至极低水平(0.5mmol/L以下),仍可带来心血管获益。将随访时间延长5年仍可见显著心血管获益。低水平LDL-C持续时间越长,心血管获益更多。
ODYSSEY OUTCOMES研究在对患者应用最大耐受剂量他汀类药物基础上,给予阿利西尤单抗,以进一步观察降低LDL-C的获益和安全性。研究显示,在他汀基础上加用PCSK9抑制剂阿利西尤单抗可以将LDL-C水平降至1.4 mmol/L(53.3mg/dL),降低心血管事件,更重要的是降低全因死亡率。而后进行的ODYSSEY OUTCOMES研究事后分析显示,在ACS患者中使用阿利西尤单抗将LDL-C短暂地降至极低与更低的心血管风险相关。
另外,不少小规模研究报道显示,LDL-C水平更低,斑块更稳定,斑块直径缩小更明显,管腔直径扩大。
对于老年人群,2020年发表于《柳叶刀》的一项研究显示,在≥75岁患者中,LDL-C每降低1mmol/L,可使主要心血管事件风险降低26%。
(3)LDL-C的极低值及潜在风险之争
目前,LDL-C的极低值及潜在风险仍然存在争议,相关研究证据较少。对于极高危人群,LDL-C降至<0.5 mmol/L或1.0 mmol/L或1.4mmol/L更好?ODYSSEY OUTCOMES研究和IMPROVE-IT研究中,结束时LDL-C<1.4mmol/L;FOURIER研究中,LDL-C<0.5 mmol/L仍可带来心血管获益;ODYSSEY OUTCOMES研究开始阶段,LDL-C<1.0mmol/L。其它研究证据较少。
在全因死亡降低方面,ODYSSEY OUTCOMES研究中阿利西尤单抗组较安慰剂组显著降低15%,但非主要终点。其它研究中未增加全因死亡。
综合以上研究结果,是否将极高危或超高危人群LDL-C维持在0.5-1.0 mmol/L更好?这一问题目前尚无定论,仍需进一步研究探索。
(4)极低LDL-C的潜在风险
LDL-C降低后的安全性是关键的问题,也是全世界所关注的问题。关于极低LDL-C的是否存在潜在风险主要涉及以下方面:是否增加出血性卒中、认知障碍、肿瘤等风险;药物安全性;多重用药的药物间相互作用。
2023发表的关于积极降低LDL-C与痴呆和出血性卒中风险影响的AHA科学声明指出,“激进”的降脂治疗未见与更高的出血、认知障碍风险相关。
➤大多数观察性研究和RCT数据不支持降LDL-C治疗与认知障碍/痴呆的关联(中位随
访时间1.6-6年)。
➤降脂治疗与出血事件风险的关联未得到证实,临床医师不应因担忧出血性卒中而选择宽松的LDL-C控制目标:
√在无脑血管疾病病史的患者中,他汀治疗与出血性卒中无显著相关;
√无PCSK9抑制剂、依折麦布增高出血风险的证据;
√目前的随机化试验、孟德尔遗传研究未提示长期低LDL-C或将LDL-C降至极低的人群更易出现出血性卒中。
➤在有出血性卒中病史的患者中,他汀治疗未见与更高的再发出血性卒中风险相关;PCSK9抑制剂在有颅内出血病史的患者中的应用风险尚未得到充分研究。
2021年发表的来自美国50岁以上普通人群注册研究提示,更低的LDL-C与认知功能降低减慢相关。该研究非降胆固醇治疗。2020年发表于《柳叶刀》的一项研究提示,降胆固醇治疗不增加癌症、出血性卒中、新发糖尿病、神经认知不良事件风险。
对于特殊人群:
➤卒中患者:2024年JAMA Neurology发表的数据来自2项中国RCT(CHANCE、CHANCE-2)的研究结果显示,在缺血性卒中或短暂性脑缺血发作 后使用双联抗血小板治疗的患者中,降LDL-C与3个月内更高的出血风险相关,但不造成严重出血。
后使用双联抗血小板治疗的患者中,降LDL-C与3个月内更高的出血风险相关,但不造成严重出血。
➤危重患者:一项针对ICU脓毒症 患者的研究(n=2542)提示,在重症患者中,低胆固醇水平与短期死亡风险增高相关。该研究也提示,胆固醇代谢在重度炎症状态下会失去适应性调节能力。董教授表示,多数情况下谈及LDL-C目标值,主要针对的是任何年龄段的正常人群,需排除虚弱患者。
患者的研究(n=2542)提示,在重症患者中,低胆固醇水平与短期死亡风险增高相关。该研究也提示,胆固醇代谢在重度炎症状态下会失去适应性调节能力。董教授表示,多数情况下谈及LDL-C目标值,主要针对的是任何年龄段的正常人群,需排除虚弱患者。
➤急性心梗患者:2022年发表的阜外医院的一项针对1224名≥80岁的急性心梗患者的研究显示,基线LDL-C<1.8mmol/L时心血管死亡风险更高。但该研究是一项观察性研究,非大样本、随机研究,证据水平不足。
总结
➤对于ASCVD极高危患者,LDL-C控制的总体原则为“越低越好”。
➤目前的多联药物治疗可使LDL-C降至低于1.0mmol/L,降幅大于70%,对于ASCVD极高危患者推荐使用药物治疗将LDL-C控制至1.0mmol/L以下以获得最大的心血管收益;对于是否将LDL-C水平控制在0.5-1.0mmol/L最佳,目前尚无定论。
➤目前尚无确切证据表明,使用药物将LDL-C降至极低会带来更高的出血性卒中、认知障碍、肿瘤等不良事件风险。
➤在特殊人群中降脂治疗的潜在风险(如老老年人)仍有待更多临床试验探索。

