
2024 ESMO中国 · E先声丨罗婷教授:方兴未艾,再添新证!吡咯替尼联合HLX02新辅助治疗HER2阳性乳腺癌
2024年欧洲肿瘤内科学会(ESMO)年会于9月13日-17日在西班牙巴塞罗那召开。本次ESMO大会上,由四川大学华西医院罗婷教授牵头开展的吡咯替尼 联合白蛋白紫杉醇
联合白蛋白紫杉醇 和曲妥珠单抗
和曲妥珠单抗 (HLX02)新辅助治疗HER2阳性早期或局部晚期乳腺癌
(HLX02)新辅助治疗HER2阳性早期或局部晚期乳腺癌 的全国多中心II期研究1,取得了令人惊喜的结果。
的全国多中心II期研究1,取得了令人惊喜的结果。
研究背景
吡咯替尼是一种口服、不可逆的酪氨酸激酶抑制剂(TKI),同时具有抗EGFR/HER1、HER2以及HER4活性。目前吡咯替尼已具有HER2阳性乳腺癌新辅助治疗适应证。
既往罗婷教授团队开展的21例HER2阳性乳腺癌II期临床研究(NCT04152057)结果显示2,3,吡咯替尼联合白蛋白紫杉醇(周疗)和曲妥珠单抗的三联用药4周期方案病理完全缓解(tpCR)率可达57.1%。基于该结果,罗婷教授团队进一步扩大样本量,拟再次验证吡咯替尼联合白蛋白紫杉醇和曲妥珠单抗在新辅助治疗中的疗效,并同时评估循环肿瘤细胞(CTCs)检测在HER2阳性局部晚期乳腺癌患者中预测pCR的价值。
研究方法
该项开放标签的Ⅱ期临床研究入组了初治Ⅱ-III期HER2阳性乳腺癌患者,给予6周期吡咯替尼联合曲妥珠单抗(HLX02)和白蛋白紫杉醇新辅助治疗,每日口服吡咯替尼(400 mg)一次,联合曲妥珠单抗(HLX02,初始负荷剂量 8mg/kg,随后每周期 6mg/kg)和白蛋白紫杉醇(260 mg/m2,每周期第1天静脉给药,21天为一个周期)。
主要研究终点为tpCR(ypT0/is N0),次要终点为ORR(RECIST 1.1)和安全性等。在基线、新辅助治疗后和术后采集患者外周血样本,并使用metafter-se-fish捕获并分析CTC,探索CTC对接受该方案治疗的HER2阳性早期和局晚期乳腺癌pCR率的预测能力。
研究结果
01、新辅助治疗疗效
在2020年12月至2023年8月期间,全国17家中心共入组216例患者,21例患者因术前退出研究而被排除分析,余下195例患者中7例提前手术。在改良意向人群(mITT)中,tpCR(ypT0/is ypN0)率为60.0%(117/195),bpCR(ypT0/is)率为63.1%(123/195)。HR阴性亚组pCR率为66.02%,HR阳性亚组为53.26%(P=0.07)(图1)。
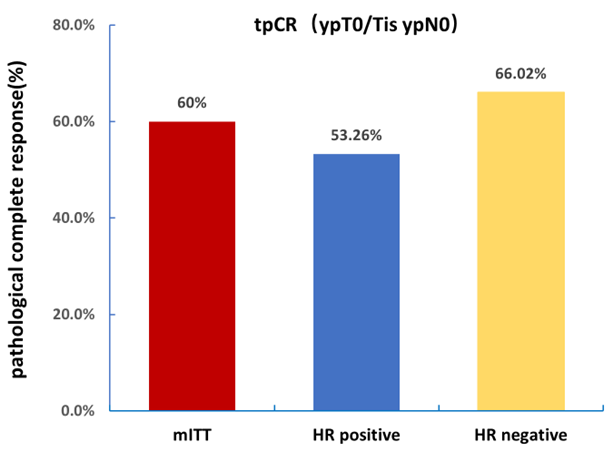
图 1. 不同激素受体状态下的tpCR
在新辅助治疗结束时进行肿瘤疗效评估,客观缓解率(ORR)达87.18%(170/195)。
02、安全性
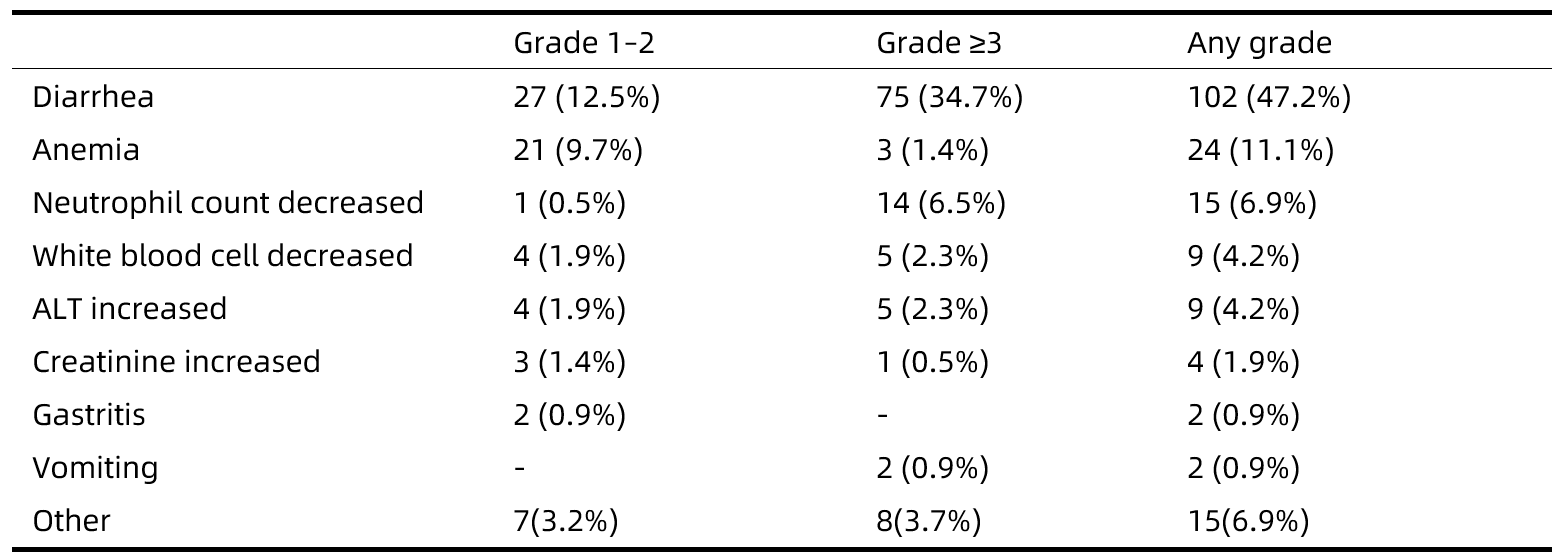
最常见的3-4级不良事件是腹泻 (34.7%)和中性粒细胞减少(6.5%)(表1)。
(34.7%)和中性粒细胞减少(6.5%)(表1)。
表1.治疗期间出现的不良事件
与未接受洛哌丁胺 和重组人粒细胞刺激因子
和重组人粒细胞刺激因子 (PEG-rhG-CSF)一级预防的患者相比,接受洛哌丁胺和PEG-rhG-CSF一级预防的患者≥3级腹泻(34.3%vs.64.3%)和≥3级中性粒细胞减少(5.7%vs.11.8%)的发生率显著降低。
(PEG-rhG-CSF)一级预防的患者相比,接受洛哌丁胺和PEG-rhG-CSF一级预防的患者≥3级腹泻(34.3%vs.64.3%)和≥3级中性粒细胞减少(5.7%vs.11.8%)的发生率显著降低。
03、循环肿瘤细胞(CTCs)检测分析
共有95例患者完成了CTC检测和分析。其中,66.32%(63/95)患者达到tpCR(图2)。在总计285份血液样本中。研究分别在基线、新辅助治疗后和手术后的CTC评估样本中检测到76/95(80.00%)、38/95(40.00%)和36/95(37.89%)≥1 CTC/5 ml。
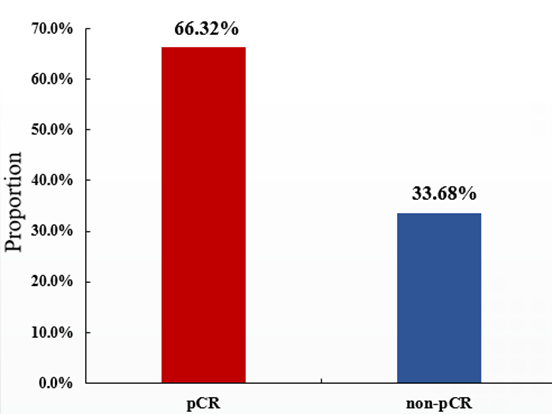
图2. CTC组中新辅助治疗的疗效
与基线相比,新辅助治疗后CTC计数显著降低(3.06±3.38vs.0.84±1.53 FU/5ml,P<0.001)。手术后CTC计数略有增加,但仍低于基线水平(3.06±3.38vs. 1.21±3.34 FU/5ml,P<0.001,图3)。
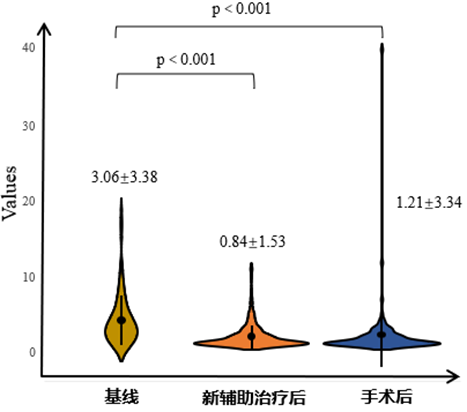
图 3. 不同治疗阶段下的CTC计数
研究结论
本研究结果显示,吡咯替尼联合白蛋白紫杉醇和曲妥珠单抗(HLX02)新辅助治疗可有效提高pCR率,表现出可控的安全性,没有发现新的安全性信号。
新辅助治疗期间对CTC进行个性化监测或许有助于实时评估治疗反应,并帮助预测pCR。
研究讨论
PHEDRA研究4显示4周期TH+Pyro方案tpCR率达41%,基于此研究成果吡咯替尼成功获批新辅助治疗适应症,并纳入国内乳腺癌指南推荐。与既往同类研究比较,NeoSphere和PEONY研究5,6新辅助4周期THP方案的tpCR率均为39.3%;NeoALTTO研究7新辅助6+12周HL-THL方案的tpCR率为46.8%;罗婷教授团队在2020年ESMO大会上报告的“一项吡咯替尼联合白蛋白紫杉醇和曲妥珠单抗新辅助治疗HER2阳性早期或局部晚期乳腺癌的Ⅱ期研究“中2,3,曲妥珠单抗+吡咯替尼+白蛋白紫杉醇(周疗)新辅助4周期方案的tpCR率达到了57.1%。该研究结果在今年ESMO BC大会上进一步报道了3年无侵袭性疾病生存期(iDFS)8,中位随访45.0个月,3年iDFS率达93.8%。这一系列研究结果提示,在化疗和曲妥珠单抗联合方案中加入吡咯替尼可进一步提高pCR率,并转化为显著的iDFS获益,证明了吡咯替尼联合曲妥珠单抗新辅助治疗HER2阳性早期或局部晚期乳腺癌有望改善患者的长期生存。本次ESMO公布的扩大样本量研究结果也进一步证实了吡咯替尼能带来pCR获益,未来将继续验证其长期生存获益。
与此同时,HER2阳性乳腺癌仍需不断优化新辅助治疗策略,尤其是对于HR+/HER2+乳腺癌患者,本研究的HR阳性亚组tpCR率达到了53.26%,表明了该新辅助治疗策略在三阳人群中的卓越疗效。未来有待进一步探索吡咯替尼联合曲妥珠单抗大小分子联合方案在HR+/HER2+早期乳腺癌中的价值。
除此之外,不良反应的管理也是临床中需要关注的问题。尽管吡咯替尼有更强、更快速的缩瘤作用,但腹泻是吡咯替尼最主要的不良反应。针对腹泻,本研究采取了积极的预防性抗腹泻措施,相比未接受一级预防的受试者,接受洛哌丁胺一级预防患者的≥3级腹泻发生率降低了30%。通过有效干预可以有效改善3级及以上腹泻的发生,提高患者的耐受性和依从性,使得治疗获益最大化。


