
樊英教授:中国晚期乳腺癌规范诊疗指南(2024版)更新,伊那利塞联合哌柏西利和氟维司群被写入HR+/HER2-乳腺癌一线治疗方案
导读:《中国晚期乳腺癌 规范诊疗指南》(简称ABCC指南)迎来了最新版本的更新,为我国晚期乳腺癌诊疗提供了重要参考和指导。值得注意的是,本次指南更新将伊那利塞+哌柏西利
规范诊疗指南》(简称ABCC指南)迎来了最新版本的更新,为我国晚期乳腺癌诊疗提供了重要参考和指导。值得注意的是,本次指南更新将伊那利塞+哌柏西利 +氟维司群
+氟维司群 作为HR+乳腺癌辅助治疗原发及继发内分泌耐药且携带PIK3CA突变的HR+/HER2-晚期乳腺癌的一线治疗方案,为HR+/HER2-晚期乳腺癌患者带来了新的希望。据此,医脉通诚邀樊英教授深入解读ABCC指南的更新要点,分享伊那利塞改写指南的循证医学证据,并展望乳腺癌未来的治疗前景。
作为HR+乳腺癌辅助治疗原发及继发内分泌耐药且携带PIK3CA突变的HR+/HER2-晚期乳腺癌的一线治疗方案,为HR+/HER2-晚期乳腺癌患者带来了新的希望。据此,医脉通诚邀樊英教授深入解读ABCC指南的更新要点,分享伊那利塞改写指南的循证医学证据,并展望乳腺癌未来的治疗前景。
ABCC指南重磅更新,伊那利塞方案为乳腺癌一线治疗添新翼
ABCC指南汇集了中国权威专家组的宝贵临床经验,总结了国内外高质量循证医学证据,自发布以来获得临床广泛认可。随着时间的推移,距离上一版(2022版)指南的发布已过去两年,我们迎来了ABCC指南(2024版)[1]的又一次重磅更新。本次更新围绕晚期乳腺癌的诊疗问题,对晚期乳腺癌治疗的基本原则、HR+/HER2-乳腺癌、HER2+乳腺癌、三阴性乳腺癌(TNBC)的治疗原则、脑转移、支持治疗以及药物相关不良反应管理等多个章节进行了全面的修订,为中国晚期乳腺癌的临床实践提供了新的指导和参考依据。
在新版指南中,总体治疗原则部分特别强调了生物标志物检测的重要性,并指出,在相关靶向药物临床可及的情况下,建议明确PIK3CA等生物标志物以指导临床决策。

图1. ABCC指南(2024版)晚期乳腺癌治疗基本原则
此外,新版ABCC指南针对不同亚型乳腺癌均有治疗推荐的更新。特别值得关注的是,指南首次将伊那利塞+哌柏西利+氟维司群三联方案作为可选方案,用于对原发及继发内分泌耐药且携带PIK3CA突变HR+/HER2-晚期乳腺癌患者的一线治疗,为这部分患者带来了一线精准治疗新选择。
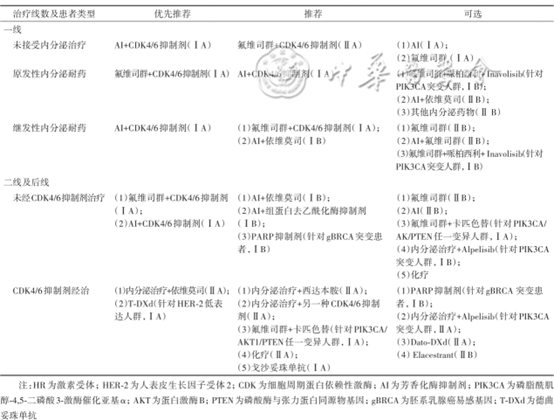
图2. ABCC指南(2024版)绝经后HR阳性HER-2阴性晚期乳腺癌患者的治疗方案
在新版指南的中国专家投票环节,51位专家根据辅助内分泌+CDK4/6i的进展情况进行了分层讨论,超过半数的专家支持根据PAM通路变异选择靶向治疗,进一步证实了生物标志物检测在指导治疗中的重要作用,也显示了包括伊那利塞在内的PAM通路抑制剂在临床应用中的巨大潜力。
PFS双倍获益,安全可控,伊那利塞三联方案再绘患者生命线
2024版ABCC指南将伊那利塞三联治疗方案纳入HR+/HER2-晚期乳腺癌一线治疗,主要是基于INAVO120研究的显著成果。INAVO120研究是一项全球多中心、随机、双盲、安慰剂对照的Ⅲ期研究,纳入原发内分泌耐药的PIK3CA突变、HR+/HER2-局部晚期或转移性乳腺癌患者,旨在探索一线伊那利塞或安慰剂+哌柏西利+氟维司群三联方案的疗效和安全性。
2023年SABCS大会公布的主要结果[2]显示,研究成功达到了主要终点PFS,伊那利塞组相较于对照组实现了超双倍的PFS获益(mPFS:15.0个月 vs 7.3个月,HR 0.43,P<0.0001),同时,伊那利塞组展现出可控的安全性和良好的耐受性,未发现新的安全信号。这一结果为伊那利塞三联治疗方案的临床应用提供了坚实的循证依据。
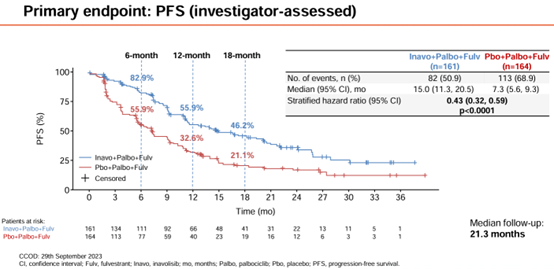
图3.INAVO120研究PFS结果
随后,2024年ASCO大会公布了附加分析结果[3],进一步证实了伊那利塞的远期生存获益,其中位PFS2(从随机化到下一线治疗结束或中止或任何原因死亡的时间)达到24.0个月,且TTFC(从随机化至首次开始后续化疗的时间)未达到,提示患者在出现疾病进展后仍能从伊那利塞方案中获益。此外,患者报告结局(PRO)数据显示,伊那利塞方案能够在不影响患者日常功能和生活质量、不增加治疗负担的前提下,将患者疼痛恶化的平均时间延长至30.9个月,显著提升患者的治疗体验。
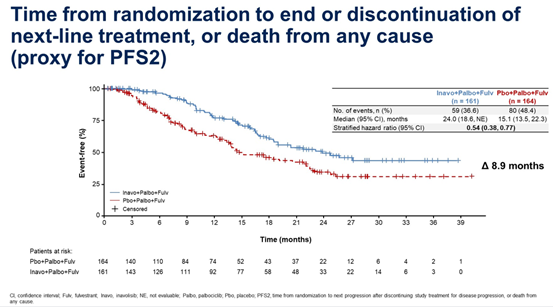
图4.INAVO120研究PFS2结果
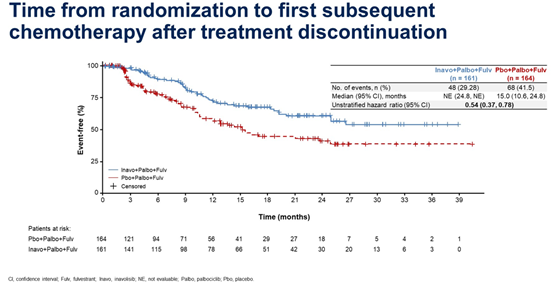
图5.INAVO120研究TTFC结果
2024年10月30日,INAVO120研究的成果被发表在国际顶尖医学期刊《新英格兰医学杂志》[4],标志着伊那利塞树立了一座乳腺癌PIK3CA突变靶向治疗的重要里程碑,为HR+/HER2-晚期乳腺癌患者带来了新的治疗希望。在今年的SABCS大会上,INAVO120研究还将报告伊那利塞组的长期安全性数据[5]。根据目前披露的信息,伊那利塞三联方案的治疗的长期安全性与既往报告一致,未发现新的不良事件。
综合INAVO120研究相关数据,我们可以看到,对于原发及继发内分泌耐药且携带PIK3CA突变HR+/HER2-晚期乳腺癌患者,伊那利塞+哌柏西利+氟维司群三联治疗方案展现出了卓越的抗肿瘤疗效。此次ABCC指南(2024版)将其纳入一线可选方案,不仅丰富了内分泌耐药患者的治疗选择,也体现了精准治疗理念在乳腺癌管理中的核心地位。
精准靶向新突破:伊那利塞助力HR+/HER2-晚期乳腺癌治疗新格局
一直以来,晚期HR+/HER2-乳腺癌的诊疗策略都是乳腺癌领域的热点议题,尤其是对于那些携带PIK3CA突变的原发内分泌耐药患者,其预后通常较差,对新型靶向治疗药物的需求显得尤为迫切。随着伊那利塞等新型靶向药物的不断涌现,本次指南对晚期HR+/HER2-乳腺癌的治疗方案做出了重要补充。作为一种新型口服、强效的高选择性PI3Kα抑制剂,伊那利塞在INAVO120研究中展现出了卓越的抗肿瘤疗效,为原发内分泌耐药的HR+/HER2-晚期乳腺癌患者带来了新的生存希望,为HR+/HER2-乳腺癌的精准治疗开辟了新的道路,有望改变HR+/HER2-晚期乳腺癌一线治疗的格局。
基于INAVO120研究的优异表现,2024年10月10日,美国食品药品监督管理局正式批准伊那利塞联合哌柏西利和氟维司群用于治疗在接受辅助内分泌治疗后复发的内分泌耐药、PIK3CA突变、HR+/HER2-的局部晚期或转移性乳腺癌成人患者。随后,NCCN指南(2024. v6)[6]将伊那利塞+哌柏西利+氟维司群方案纳入HR+/HER2-晚期乳腺癌患者一线治疗方案列表(Ⅰ类证据);本次更新的ABCC指南(2024版)也将该方案作为HR+/HER2-晚期乳腺癌患者一线治疗方案,这表明伊那利塞三联方案已获得国内外乳腺癌诊疗专家的一致认可。目前,伊那利塞在HR+/HER2-晚期乳腺癌领域的一线适应症已被国家药品监督管理局纳入优先审评,未来有望成为国内乳腺癌领域首个获批的PI3K抑制剂,填补PIK3CA突变HR+/HER2-晚期乳腺癌治疗空白,开启HR+精准治疗新时代。
从本次指南更新和乳腺癌总体发展趋势上来看,随着伊那利塞等新药物的加入,晚期乳腺癌尤其是HR+/HER2-乳腺癌的治疗趋势正朝着精准靶向治疗的方向发展。精准医疗的实施,将使得乳腺癌治疗更加个性化,能够针对患者的特定基因突变和生物标志物进行定制化治疗。这种治疗模式的转变,不仅能够提高治疗效果,还能减少不必要的不良反应,改善患者的生活质量。未来,我们期待有更多的靶向药物和个性化治疗方案出现,为患者带来更有效的治疗选择和更高的生活质量,让患者获益实现最大化!

