
马飞教授:一针守护!中国原研超长效止吐药磷罗拉匹坦帕洛诺司琼优化CINV全程管理
2025年5月29日,基于III期PROFIT研究成果,国家药品监督管理局(NMPA)正式批准注射用磷罗拉匹坦帕洛诺司琼(瑞坦宁)用于预防成人高度致吐性化疗(HEC)引起的急性和迟发性恶心和呕吐(CINV)。作为中国首个(截止至2025.5.29)超长效原研双靶点的止吐针剂,磷罗拉匹坦帕洛诺司琼在每个化疗周期内仅需注射一次,即可覆盖急性期(0-24小时)、延迟期(24-120小时)及超延迟期(120-168小时)CINV。其联合地塞米松在预防HEC-CINV方面非劣效于标准三联方案(福沙匹坦+帕洛诺司琼+地塞米松),在两周期化疗后,延迟期和超延迟期报告对日常生活无影响的患者比例更高[1]。该突破性数据已在国际著名肿瘤学期刊Journal of Clinical Oncology(JCO,IF=42.1)重磅发布[1],彰显了中国在CINV预防领域取得的重大进展,更为全球肿瘤学界贡献了重要的循证医学证据。
值此之际,医脉通特别邀请到中国医学科学院肿瘤医院马飞教授,就CINV管理的临床意义、瑞坦宁的创新作用机制及获批价值、以及如何优化CINV全程管理等重要话题进行深入探讨。此次分享旨在为临床医生提供更精准、更高效的CINV防治策略,推动中国肿瘤支持治疗领域的持续进步,助力患者跨越CINV难关,全身心投入抗癌之旅。
医脉通:CINV是肿瘤患者化疗过程中常见的不良反应。能否请您介绍下CINV对抗肿瘤治疗的影响?从肿瘤治疗全局视角来看,CINV 的有效控制对患者整体治疗效果、生存质量及预后有哪些重要意义?
马飞教授:
近年来,抗肿瘤方案及药物不断丰富,但治疗相关恶心呕吐仍是抗肿瘤临床实践中亟需规范化管理的常见不良反应。严重的恶心呕吐可能导致患者发生脱水、电解质紊乱、营养缺乏等,影响抗肿瘤治疗的实施及临床转归。有数据显示,相较于未发生和仅发生I/II级CINV的患者,发生更严重CINV(III/IV级)的患者病情更容易进展,生存时间也可能会缩短[2]。真实世界数据发现,高致吐风险化疗患者在CINV预防方面,指南依从率较低。提高止吐用药指南依从率,是当前CINV管理的重要任务。
从肿瘤治疗全局视角来看,CINV的有效控制对患者管理具有重要意义。首先,有效控制CINV,有助于化疗顺利进行,维持抗肿瘤治疗的有效性。其次,在抗肿瘤临床实践中,规范化管理CINV对提升患者生存质量具有积极影响,具体表现为改善机体功能状态、减轻疾病相关心理负担等。频繁的恶心呕吐还会给患者带来心理压力,产生焦虑、抑郁等不良情绪,影响心理健康。CINV得到有效控制后,患者心理负担减轻,能以更积极的心态面对疾病和治疗,有利于提高生活质量。此外,控制CINV可降低恶心呕吐导致的脱水、电解质紊乱、营养缺乏等并发症的发生风险,促进患者身体恢复,改善预后。
医脉通:近日,磷罗拉匹坦帕洛诺司琼获得NMPA批准用于预防成人高度致吐性化疗(HEC)引起的急性和迟发性恶心和呕吐。能否请您谈一谈,此次获批会对临床实践产生哪些积极影响?其对乳腺癌患者具有哪些重要意义?
马飞教授:
磷罗拉匹坦帕洛诺司琼的获批为中国肿瘤患者提供了一种强效便捷、安全性良好的CINV管理方案[1],有助于解决临床未满足的需求。化疗在乳腺癌不同治疗阶段发挥重要作用,但乳腺癌化疗患者中CINV发生率达60%-90%,延迟期恶心呕吐尤为突出[3]。在临床实践中,AC方案(含蒽环类、环磷酰胺的联合方案),以及一些含顺铂、卡铂(AUC≥4)的用药组合等均为HEC方案[4,5]。女性、年龄小于50岁等为CINV的高危人群[4],这些人群对恶心呕吐控制和生活质量有着迫切需求。
另外值得关注的是,目前相关指南/共识将ADC药物戈沙妥珠单抗、德曲妥珠单抗列为高度致吐风险药物,其引发的恶心呕吐不仅出现时间晚,且持续周期长。这种持续的恶心呕吐也会增加患者的总体负担。有研究显示[6],T-DXd的任何级别恶心发生率为55%-78%,呕吐发生率为25%-52%。SG在TROPiCS-02试验中恶心发生率为55%、呕吐发生率为19%。T-DXd的恶心中位发生时间为3天,持续10天;呕吐中位发生时间9.5天,持续3天。SG的恶心中位发生时间8天,持续5.5天;呕吐中位发生时间24.5天,持续1.5天。
磷罗拉匹坦帕洛诺司琼的获批对乳腺癌患者的管理具有重要意义。PROFIT研究显示[1],连续两个化疗周期,磷罗拉匹坦帕洛诺司琼急性期和超延迟期的CR率均达到90%以上(第一个化疗周期急性期CR率为91.2%,超延迟期CR率为90.3%;第二个化疗周期疗效更佳,急性期CR率为93.3%,超延迟期CR率为92.7%)。且连续两个化疗周期急性期以及超延迟期的无显著恶心率均达90%以上(第一个化疗周期急性期无显著恶心率为92.2%,超延迟期为92.2%;第二个化疗周期急性期为94.6%,超延迟期为95.5%),实现了止吐“双90”。这意味着该药物能持续、高效地保护乳腺癌患者在CINV风险期免受恶心呕吐的困扰,提升患者的生活质量和对抗肿瘤治疗的依从性,对改善乳腺癌患者预后具有积极意义。
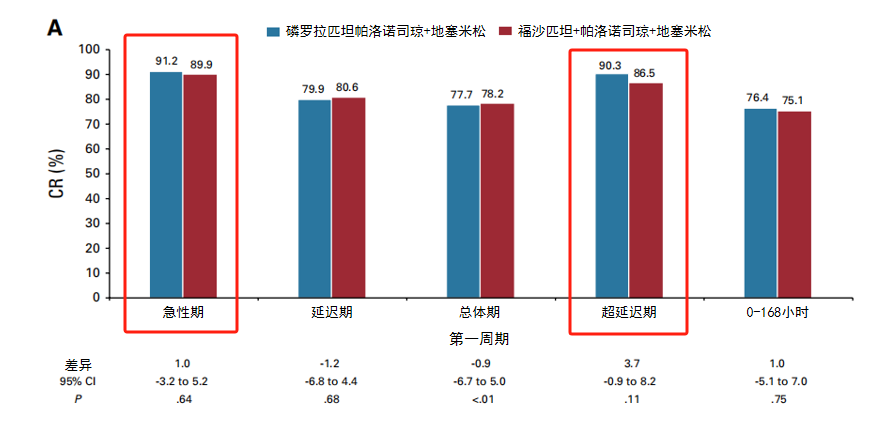
图1 第一个化疗周期的CR率
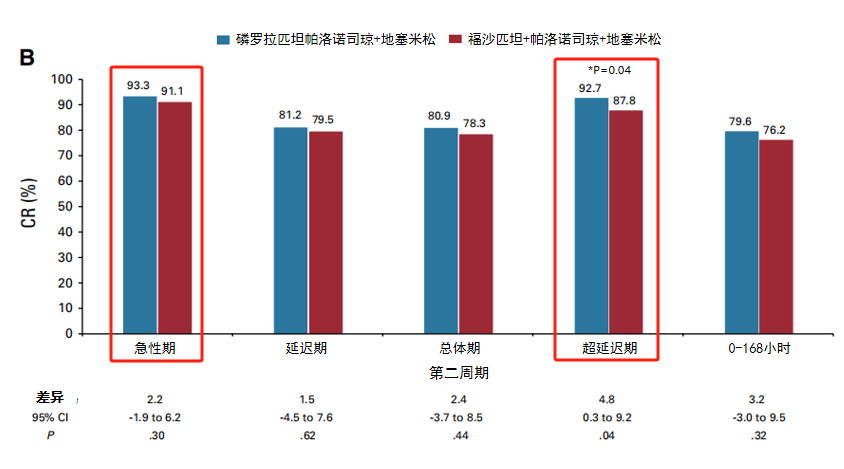
图2 第二个化疗周期的CR率
通常情况下乳腺癌患者需要化疗4-8个周期,甚至更长,每21天为一个周期,传统止吐药需多次给药,增加患者往返医院频率及用药管理负担。磷罗拉匹坦帕洛诺司琼凭借其长效——近8天(188小时*)的超长半衰期优势,每个化疗周期只需注射一次(可同时覆盖CINV急性期、延迟期及超延迟期),临床使用便捷,优化了用药管理,提高了乳腺癌患者的治疗依从性。此外,与其它止吐药物不同,磷罗拉匹坦帕洛诺司琼配伍后安全性更好。其不是CYP3A4酶的抑制剂或诱导剂,对经CYP3A4酶代谢抗癌药物(如乳腺癌治疗常涉及的紫杉醇、环磷酰胺等)以及激素的影响较小。
医脉通:磷罗拉匹坦帕洛诺司琼通过何种创新作用机制,突破传统CINV管理局限,重塑肿瘤治疗全程管理的策略与理念?在多学科协作治疗模式下,如何进一步优化 CINV 管理以推动肿瘤治疗高质量发展?
马飞教授:
传统CINV管理存在局限性。大部分肿瘤患者更关注急性期的CINV预防用药,而对延迟期的CINV管理关注较少,导致CINV全程管理不佳等。以往预防HEC引起的恶心和呕吐,可能需要多种药物联合、多次给药,患者用药依从性低、CINV预防用药指南依从率低。
磷罗拉匹坦帕洛诺司琼凭借创新机制,简化临床用药管理、提高患者生活质量。磷罗拉匹坦帕洛诺司琼是由新型超长效NK-1RA磷罗拉匹坦和目前唯一的二代5-HT3 RA帕洛诺司琼组成的双靶止吐药物,可同时拮抗NK-1受体和5-HT3受体,通过双通道抑制呕吐反射。在临床实践中,该药每化疗周期仅需注射1次,有助于简化肿瘤患者的临床用药管理,改善指南依从率。
当前肿瘤诊疗领域倡导“以患者为中心”的管理理念,而磷罗拉匹坦帕洛诺司琼的上市可有效改善患者生活质量,提升治疗体验和用药依从性,进而改善患者预后。未来,在多学科协作治疗模式下,可以通过加强各学科间的沟通与协作,优化止吐等影响患者生活质量的方案,并进一步关注患者个体差异开展全周期管理,同时加强研究与科普教育,进一步优化CINV管理,改善患者生活质量和延长生存期,从而推动肿瘤治疗进步。
*数据来源:PROFIT研究者手册

