
JASN 重磅综述 | 衰老细胞靶向治疗与再生策略有望延缓糖尿病肾病进展
前言
近年来,钠-葡萄糖 协同转运蛋白2抑制剂(SGLT2i)、胰高血糖素
协同转运蛋白2抑制剂(SGLT2i)、胰高血糖素 样肽-1受体激动剂(GLP-1RA)及非甾体盐皮质激素受体拮抗剂(nsMRA)等药物研发的重大突破,显著延缓了众多糖尿病肾病(DKD)患者的疾病进展。然而,DKD目前仍无法根治,每年仍有新增患者进展至肾衰竭
样肽-1受体激动剂(GLP-1RA)及非甾体盐皮质激素受体拮抗剂(nsMRA)等药物研发的重大突破,显著延缓了众多糖尿病肾病(DKD)患者的疾病进展。然而,DKD目前仍无法根治,每年仍有新增患者进展至肾衰竭 ,亟需新型治疗策略。
,亟需新型治疗策略。
近期,《JASN 》杂志发表了一项综述“Fortifying the Diabetic Kidney Disease Treatment Armamentarium——Multitarget Senotherapeutic and Regenerative Strategies”(IF=9.4),深入解析了衰老细胞靶向治疗与再生策略的作用机制与前景,有望为糖尿病肾病治疗带来革命性突破。

DKD是由多重复杂机制共同驱动的疾病,其进展需要多维度干预来阻断。慢性炎症和细胞衰老(衰老的核心生物学标志)作为相互关联的病理过程,共同促进并维持DKD的发展。细胞衰老是由高血糖、氧化应激及尿毒症 毒素等内外源性应激因素引发的不可逆细胞周期停滞,衰老失控状态会导致不良结局。具体而言,衰老细胞通过衰老相关分泌表型(SASP)释放促炎因子、促纤维化细胞因子、生长因子及基质降解酶,从而加速肾纤维化、肾小球硬化和肾小管功能障碍。
毒素等内外源性应激因素引发的不可逆细胞周期停滞,衰老失控状态会导致不良结局。具体而言,衰老细胞通过衰老相关分泌表型(SASP)释放促炎因子、促纤维化细胞因子、生长因子及基质降解酶,从而加速肾纤维化、肾小球硬化和肾小管功能障碍。
在DKD患者中,肾小管上皮细胞、足细胞、系膜细胞及内皮细胞均存在大量衰老细胞。研究表明,DKD患者的循环系统中,衰老标志物激活素A(activin A)水平显著升高,同时伴随抗衰老因子(如sirtuins和α-klotho)的功能障碍及表达缺失。值得注意的是,衰老细胞靶向治疗和再生治疗可特异性干预炎症与衰老过程,为DKD的临床治疗提供了新的策略。
DKD的衰老细胞靶向治疗策略
衰老细胞靶向治疗药物(senotherapeutics)主要分为两大类:衰老细胞清除剂(senolytics)和衰老表型调节剂(senomorphics)。这两类药物在延缓年龄相关疾病进展方面展现出显著疗效。
衰老细胞清除剂通过特异性抑制衰老细胞的抗凋亡通路,能够选择性清除30%-70%的衰老细胞,不过这类药物可能带来伤口愈合延迟等不良反应,通过组织特异性靶向和精准干预促炎表型可有效控制风险。另一方面,衰老表型调节剂采取不同机制,在不清除衰老细胞的前提下,特异性抑制SASP的产生。基于两类药物的作用特点,目前推荐采用联合治疗方案:间歇性使用衰老细胞清除剂进行"打击-撤离"式给药,同时持续应用衰老表型调节剂。这种组合策略既能有效清除衰老细胞,又可持续抑制SASP,从而获得最佳的风险获益比。
目前针对DKD的衰老细胞清除剂研究仍处于探索阶段。在DKD患者中开展的Ⅰ期临床试验已取得了重要突破:首次证实采用达沙替尼 (酪氨酸激酶抑制剂)联合槲皮素(D+Q)的3天短期给药方案,可有效清除脂肪组织中的衰老细胞。该方案不仅显著减少了脂肪组织巨噬细胞浸润,还降低了循环系统中多种SASP因子(包括IL-1α、IL-6、MMP-9和MMP-12)的水平。在机制研究方面,DKD小鼠模型实验显示,D+Q通过双重作用发挥肾脏保护效应:一方面激活PPARα介导的脂肪酸氧化,另一方面增强自噬功能,从而有效减轻氧化应激。值得注意的是,另一黄酮类化合物非瑟酮也展现出肾脏保护作用,其机制包括恢复自噬功能和抑制NLRP3炎症小体活化。然而,非瑟酮清除肾脏衰老细胞的作用目前仅在老年小鼠模型中得到验证,其在DKD中的疗效仍需进一步研究。
(酪氨酸激酶抑制剂)联合槲皮素(D+Q)的3天短期给药方案,可有效清除脂肪组织中的衰老细胞。该方案不仅显著减少了脂肪组织巨噬细胞浸润,还降低了循环系统中多种SASP因子(包括IL-1α、IL-6、MMP-9和MMP-12)的水平。在机制研究方面,DKD小鼠模型实验显示,D+Q通过双重作用发挥肾脏保护效应:一方面激活PPARα介导的脂肪酸氧化,另一方面增强自噬功能,从而有效减轻氧化应激。值得注意的是,另一黄酮类化合物非瑟酮也展现出肾脏保护作用,其机制包括恢复自噬功能和抑制NLRP3炎症小体活化。然而,非瑟酮清除肾脏衰老细胞的作用目前仅在老年小鼠模型中得到验证,其在DKD中的疗效仍需进一步研究。
近年来研究发现,包括二甲双胍 、雷帕霉素、雌激素
、雷帕霉素、雌激素 和白藜芦醇在内的多种衰老表型调节剂均表现出肾脏保护作用,但其在DKD中的抗衰老机制研究仍相对不足。动物实验
和白藜芦醇在内的多种衰老表型调节剂均表现出肾脏保护作用,但其在DKD中的抗衰老机制研究仍相对不足。动物实验 证实,这些药物在DKD模型中能够通过恢复Sirt1活性,显著减少肾小管和系膜细胞的衰老标志物表达。值得注意的是,近期研究发现SGLT2i和GLP-1RA等新型降糖药物可能通过间接途径发挥抗衰老作用,其机制可能涉及增强内源性免疫系统对衰老细胞的清除能力,以及模拟热量限制效应。
证实,这些药物在DKD模型中能够通过恢复Sirt1活性,显著减少肾小管和系膜细胞的衰老标志物表达。值得注意的是,近期研究发现SGLT2i和GLP-1RA等新型降糖药物可能通过间接途径发挥抗衰老作用,其机制可能涉及增强内源性免疫系统对衰老细胞的清除能力,以及模拟热量限制效应。
这些研究结果具有重要的临床意义:能够有效减轻DKD中细胞衰老负荷的靶向治疗药物,其获益可能不仅限于肾脏保护,还可能通过系统性地延缓衰老进程,改善多个器官功能,最终达到延长健康寿命的目的,为开发DKD的综合治疗方案提供了新的思路。
DKD的再生医学治疗策略
2024年12月,美国食品药品监督管理局(FDA)批准首个间充质干细胞疗法Ryoncil用于治疗儿童激素难治性急性移植物抗宿主病 ,这一突破性进展标志着细胞治疗领域的重要里程碑。在DKD治疗领域,基于细胞的再生疗法因其显著的抗炎和组织修复活性而备受关注。大量临床前研究表明,间充质干细胞(MSCs)、肾脏祖细胞及其分泌的细胞外囊泡在DKD动物模型中展现出多重肾脏保护作用,包括改善肾功能、减轻蛋白尿
,这一突破性进展标志着细胞治疗领域的重要里程碑。在DKD治疗领域,基于细胞的再生疗法因其显著的抗炎和组织修复活性而备受关注。大量临床前研究表明,间充质干细胞(MSCs)、肾脏祖细胞及其分泌的细胞外囊泡在DKD动物模型中展现出多重肾脏保护作用,包括改善肾功能、减轻蛋白尿 、抑制肾小球增大、减少纤维化形成,以及缓解炎症反应、细胞凋亡、上皮-间质转化和氧化应激等病理过程。其作用机制主要依赖于MSCs分泌组(包含细胞因子、趋化因子、生长因子和细胞外囊泡等生物活性物质)的旁分泌效应,通过免疫调节和促再生双重机制发挥作用。临床研究方面,近期一项采用抗CD362抗体筛选异体MSCs(ORBCEL-M)的随机安慰剂对照Ib/IIa期试验证实,该疗法可显著延缓DKD患者估算肾小球滤过率(eGFR)的下降速度。此外,多项针对DKD/慢性肾脏病(CKD)的早期临床试验也一致证明了细胞疗法的良好安全性和耐受性,为后续研究奠定了重要基础。细胞外囊泡作为DKD治疗的新兴选择,因其较活细胞治疗更低的致瘤性和免疫原性风险而备受关注。这类由细胞分泌的脂质双层囊泡通过转运蛋白质、mRNA和microRNA等生物活性物质,在细胞间通讯中发挥重要作用,进而产生肾脏保护效应。然而目前临床研究进展相对滞后,仅有一项关于细胞外囊泡治疗CKD的临床试验被报道。相比之下,美国研发的rilparencel(一种水凝胶包裹的自体肾脏祖细胞产品)已进入III期临床试验阶段,成为DKD再生医学领域的候选疗法。
、抑制肾小球增大、减少纤维化形成,以及缓解炎症反应、细胞凋亡、上皮-间质转化和氧化应激等病理过程。其作用机制主要依赖于MSCs分泌组(包含细胞因子、趋化因子、生长因子和细胞外囊泡等生物活性物质)的旁分泌效应,通过免疫调节和促再生双重机制发挥作用。临床研究方面,近期一项采用抗CD362抗体筛选异体MSCs(ORBCEL-M)的随机安慰剂对照Ib/IIa期试验证实,该疗法可显著延缓DKD患者估算肾小球滤过率(eGFR)的下降速度。此外,多项针对DKD/慢性肾脏病(CKD)的早期临床试验也一致证明了细胞疗法的良好安全性和耐受性,为后续研究奠定了重要基础。细胞外囊泡作为DKD治疗的新兴选择,因其较活细胞治疗更低的致瘤性和免疫原性风险而备受关注。这类由细胞分泌的脂质双层囊泡通过转运蛋白质、mRNA和microRNA等生物活性物质,在细胞间通讯中发挥重要作用,进而产生肾脏保护效应。然而目前临床研究进展相对滞后,仅有一项关于细胞外囊泡治疗CKD的临床试验被报道。相比之下,美国研发的rilparencel(一种水凝胶包裹的自体肾脏祖细胞产品)已进入III期临床试验阶段,成为DKD再生医学领域的候选疗法。
值得注意的是,最新研究发现MSCs及其分泌的细胞外囊泡不仅具有再生能力,还表现出显著的衰老细胞靶向治疗效应。在DKD动物模型中,MSCs能够有效降低肾小球和肾间质中衰老相关β-半乳糖苷酶 的表达水平。更重要的是,这些疗法通过其独特的抗炎和免疫调节特性,显著减少巨噬细胞和淋巴细胞浸润,同时降低循环系统中SASP因子的水平。这种与衰老表型调节剂相似的作用机制,为开发DKD的新型治疗策略提供了重要理论基础和临床转化前景。
的表达水平。更重要的是,这些疗法通过其独特的抗炎和免疫调节特性,显著减少巨噬细胞和淋巴细胞浸润,同时降低循环系统中SASP因子的水平。这种与衰老表型调节剂相似的作用机制,为开发DKD的新型治疗策略提供了重要理论基础和临床转化前景。
单独而言,再生疗法与抗衰老疗法或将成为延缓DKD进展的新型干预手段。最新跨领域研究揭示了二者联用可能产生的协同增效作用——这种组合策略有望重新定义DKD的治疗范式。本文列举了可转化应用于DKD的多种临床/临床前策略(图1):
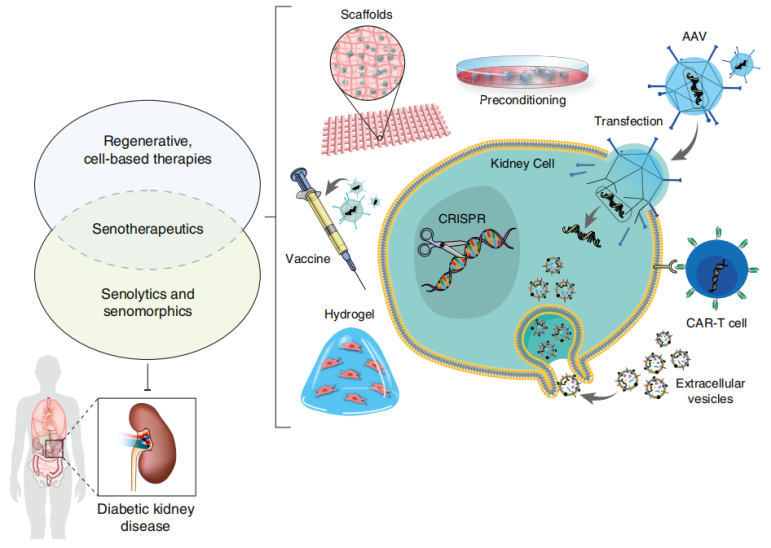
图1. 糖尿病肾病中衰老治疗、抗炎及再生效应的未来优化策略
AAV:腺相关病毒、CAR:嵌合抗原受体、CAR-T:嵌合抗原受体T细胞疗法、CRISPR:成簇规律间隔短回文重复序列、MSC:间充质干细胞
衰老药物预处理
类似低氧或干扰素-γ预激活方案,采用衰老治疗药物预处理可增强间充质干细胞及其胞外囊泡的修复效能与稳定性。
工程化胞外囊泡递药系统
装载衰老细胞清除剂(如D+Q)可解决药物生物利用度低与代谢过快的问题;通过聚乙二醇 化修饰或添加"衰老细胞靶向基团",能显著提升囊泡稳定性、延长循环半衰期,并实现肾脏靶向递送。
化修饰或添加"衰老细胞靶向基团",能显著提升囊泡稳定性、延长循环半衰期,并实现肾脏靶向递送。
生物材料载体技术
可包载保护衰老治疗药物、工程化胞外囊泡及MSCs/肾脏祖细胞。
-支架材料:胶原/壳聚糖/透明质酸等生物相容性聚合物构成的三维网络
-水凝胶:具有pH/温度/微环境响应性的交联聚合物网络,可实现可控降解与药物释放
生物材料肾脏植入技术可实现治疗药物的局部长效释放。例如,明胶甲基丙烯酰水凝胶能持续释放槲皮素纳米颗粒,显著促进伤口愈合。目前应用于DKD患者的Rilparencel(一种由肾脏祖细胞与生物材料复合而成的治疗产品)通过肾脏注射给药,已显示出良好的治疗效果。
衰老细胞转染与疫苗技术
可削弱衰老细胞的免疫逃逸和抗凋亡防御机制:
靶向CD153、衰老相关黏附分子1及糖蛋白非转移性黑色素瘤蛋白B等抗原的衰老细胞清除疫苗,能训练免疫系统特异性识别并清除衰老细胞;最新研究证实,腺相关病毒9型载体介导的G蛋白偶联受体124(Gpr124)肾脏实质递送,可减轻小鼠DKD模型中足细胞衰老。
嵌合抗原受体T细胞(CAR-T)疗法
通过靶向衰老细胞表面抗原(如自然杀伤细胞2D组配体)促进免疫清除;尿激酶型纤溶酶原激活物受体等衰老相关蛋白在非DKD模型中已证实有效性;衍生技术CAR受体修饰间充质干细胞可实现精准细胞靶向。
CRISPR基因编辑技术
通过精确上调Sirtuin 1、Klotho等肾脏保护基因表达;有效抑制衰老相关分泌表型驱动的炎症反应。
糖尿病肾病作为 2 型糖尿病(T2D)的常见微血管并发症,是全球慢性肾脏病 及终末期肾病的主要病因2。在中国,因T2D导致的CKD(CKD-T2D)已成为CKD首要病因,疾病负担沉重2。尽管当前糖尿病肾病的临床治疗已取得显著进展,但疾病进展的复杂性与患者对有效干预手段的迫切需求,仍凸显出未被满足的医疗缺口,亟需探索更具突破性的创新疗法来改写疾病管理格局。
及终末期肾病的主要病因2。在中国,因T2D导致的CKD(CKD-T2D)已成为CKD首要病因,疾病负担沉重2。尽管当前糖尿病肾病的临床治疗已取得显著进展,但疾病进展的复杂性与患者对有效干预手段的迫切需求,仍凸显出未被满足的医疗缺口,亟需探索更具突破性的创新疗法来改写疾病管理格局。
该研究通过创新性地联合再生医学与衰老细胞靶向治疗策略来减轻炎症和细胞衰老进程,有望为糖尿病肾病治疗带来革命性突破。然而,要实现这些前沿疗法的临床转化,仍需解决若干关键问题:首先需要系统评估治疗方案的安全性和耐受性,建立科学的风险获益评估体系;其次要精准识别最可能获益的目标人群(包括治疗失败高风险患者、不同分期的慢性肾病患者以及存在药物不耐受情况等特殊群体);最后还需开发有效的风险预测模型。值得注意的是,这些创新疗法的成功转化离不开多方协作,只有通过学术界的基础研究、产业界的研发投入、患者群体的积极参与以及监管机构的科学指导,形成完整的创新生态,才能最终实现DKD患者预后的显著改善。
点评专家:北京协和医院肾内科马杰教授
