
血液“加”速度 | 刘加军教授:Guadicitabine提高高危AML及MDS患者移植后无复发生存率
医脉通编辑整理,未经授权请勿转载。
去甲基化药物(HMA)阿扎胞苷 和地西他滨
和地西他滨 在临床中应用广泛,常被用作维持治疗以预防复发,或在异基因造血干细胞移植
在临床中应用广泛,常被用作维持治疗以预防复发,或在异基因造血干细胞移植 (allo-HSCT)后,用于急性髓系白血病
(allo-HSCT)后,用于急性髓系白血病 (AML)和骨髓增生异常综合征(MDS)患者的挽救性方案,用于治疗疾病复发。已有研究证实,HMA(联合或不联合供者淋巴细胞输注[DLI])在治疗移植后微小残留病(MRD)或明确复发方面具有疗效。Guadecitabine作为新一代HMA,其临床价值备受关注。为此,研究者报告了一项II期单中心临床试验(NCT06297629)的结果,该试验旨在探究Guadecitabine(联合或不联合DLI)在移植后不同阶段的AML和MDS患者中,分别作为维持治疗、抢先治疗及挽救治疗的应用效果。本期,中山大学附属第三医院刘加军教授为我们带来该研究的最新结果。
(AML)和骨髓增生异常综合征(MDS)患者的挽救性方案,用于治疗疾病复发。已有研究证实,HMA(联合或不联合供者淋巴细胞输注[DLI])在治疗移植后微小残留病(MRD)或明确复发方面具有疗效。Guadecitabine作为新一代HMA,其临床价值备受关注。为此,研究者报告了一项II期单中心临床试验(NCT06297629)的结果,该试验旨在探究Guadecitabine(联合或不联合DLI)在移植后不同阶段的AML和MDS患者中,分别作为维持治疗、抢先治疗及挽救治疗的应用效果。本期,中山大学附属第三医院刘加军教授为我们带来该研究的最新结果。
研究方法
研究纳入标准:年龄≥18 岁,接受过配型相关供者、无关供者或单抗原错配供者的allo-HSCT,美国东部肿瘤协作组(ECOG)体能状态评分为 0-2 分,且心、肝、肾功能良好的AML或MDS患者。根据移植后疾病状态,患者被分为三个治疗队列:队列1(n=13):移植后发生血液学复发的患者;队列2(n=18):移植后检出MRD阳性的患者;队列3(n=24):移植后100天内处于完全缓解且MRD阴性的患者。
队列1和队列2的患者接受Guadicitabine皮下注射治疗,初始剂量为40 mg/m²/天,连续注射5天,每28天为一个周期,最多治疗6个周期以评估疗效。队列3的患者接受Guadicitabine皮下注射治疗,剂量为30mg/m²/天,连续注射5天,每28天为一个周期,共治疗12个周期。
主要终点:队列1为达到完全缓解(CR);队列2实现MRD转阴;队列3为无复发生存期(RFS)。所有队列的次要终点为总生存期(OS)、缓解持续时间以及≥3级的不良事件(AE)的发生率。
研究结果
2016年8月至2020年8月期间,研究者前瞻性筛选并纳入了56例接受过allo-HSCT的成年AML和MDS患者。患者的人口统计学特征和基线资料详见表1。
表1
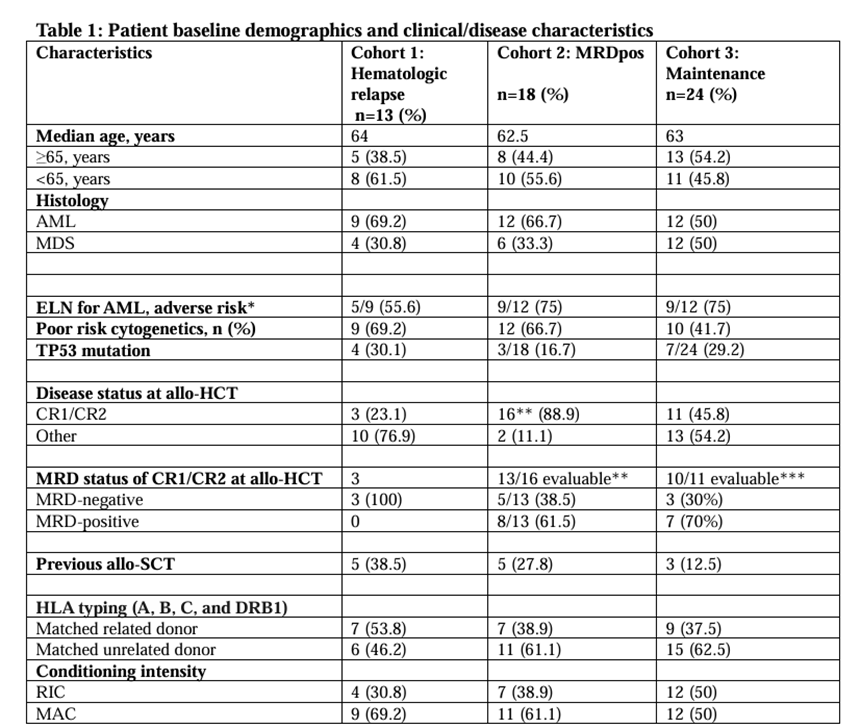
队列1的13例患者中,有3例经Guadicitabine治疗达到CR。
队列2共纳入18例处于形态学缓解但经证实存在MRD的患者。1例患者在第一个周期内停药,被排除在结局评估之外。在17例可评估患者中,8例(47.1%)在Guadicitabine治疗的前6个周期内实现MRD清除并达到应答(图1)。MRD检测后的2年RFS率和OS率分别为29.4%(95% CI,10.7%-51.2%)和35.3%(95% CI,18.5%-67.2%)。应答者的2年RFS率为62.5%(95% CI,22.9%-86.1%)。

图1
队列3纳入24例复发高危的MDS/AML患者,在移植后100天内启动Guadicitabine维持治疗。Guadicitabine维持治疗的中位周期数为7.5个(范围:1-12)。在存活患者中,中位随访时间为48个月(范围:35-70),2年RFS率和OS率分别为62.5%(95% CI:40.3%-78.4%)和66.7%(95% CI:44.3%-81.7%)(图2)。
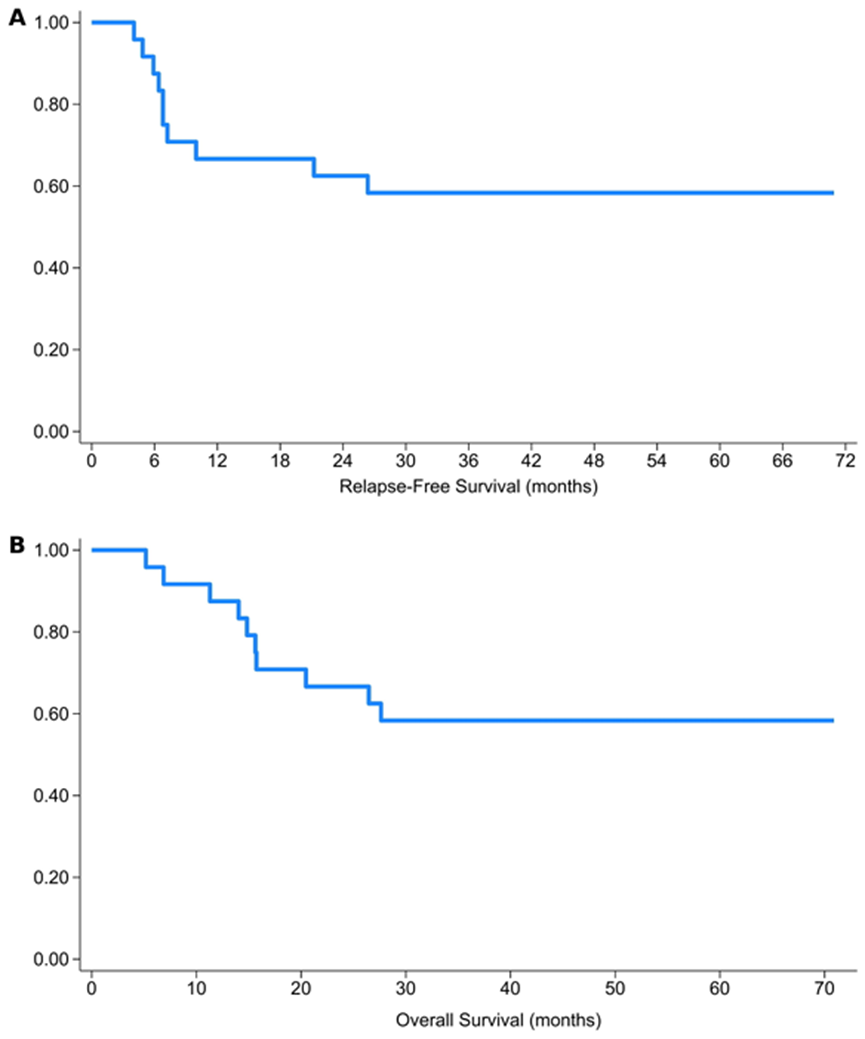
图2
本研究未观察到意外不良事件(AE)。在队列1和队列2中,每个队列各报告1例5级毒性反应(表2)。队列3(n=24)中,1例患者在第5个周期后出现II级迟发性急性GVHD,经治疗后病情缓解并完成了全部12个周期治疗;2例患者分别在第5和第6个周期后发生慢性GVHD,均经治疗成功控制,分别完成了9个和12个周期治疗。
表2
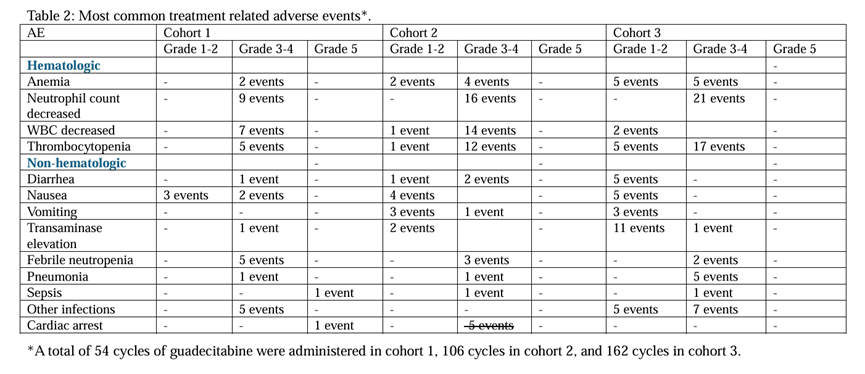
研究结论
研究表明,Guadicitabine在allo-HSCT后不同疾病状态的AML/MDS患者中均展现出良好的治疗效果和可接受的安全性,特别是对于MRD阳性患者具有显著的清除作用。这些结果为去甲基化药物在移植后维持治疗中的应用提供了新的循证依据,值得开展更大规模的随机对照研究加以验证。
专家点评
刘加军教授:
本研究采用疾病状态分层设计,针对allo-HSCT后三类不同风险患者(血液学复发、MRD阳性、预防性治疗)探索Guadicitabine的差异化应用策略,针对性设定治疗目标(队列 1 追求形态学完全缓解(CR)、队列 2 追求 MRD 清除、队列 3 追求延长无复发生存(RFS)),这种 "精准分层"的研究思路高度契合当前血液肿瘤的个体化治疗趋势。对于移植后复发(队列 1)和 MRD 阳性(队列 2)的高危患者,早期干预是降低进展风险的关键;对于移植后早期缓解但仍有潜在复发风险的患者(队列 3),通过巩固治疗延长 RFS,追求缓解后的持续维持。
队列2中MRD清除患者的2年RFS与预防组相当(均为62.5%),这一结果强烈提示: MRD阳性患者通过药物干预可能达到与自然缓解患者相似的生存获益,同时支持将"MRD清除"作为移植后干预的替代终点指标。
研究证实Guadicitabine未增加移植相关并发症(如GVHD、感染),未导致移植物失败,骨髓抑制可控,这种"高效低毒"的特性使其特别适合移植后免疫功能尚未完全重建的脆弱患者群体。
单中心、小样本(总例数55例)是本研究的主要局限,可能影响结果的普适性,需多中心研究进一步验证。同时研究缺乏随机对照设计,无法明确回答"是否优于现有HMA(如地西他滨)"另外,队列1的CR率偏低,提示对于已发生血液学复发的患者,单纯Guadicitabine可能疗效有限,未来需探索联合方案(如与供者淋巴细胞输注(DLI)、靶向药物等联合)以提高疗效。
专家简介

刘加军 教授
中山大学附属第三医院 血液内科主任
主任医师,教授,博士研究生导师,博士后合作导师
教育部“中国科技论文在线”特邀评审专家
教育部新世纪优秀人才
欧洲肿瘤内科协会抗癌分会会员
中国免疫学学会会员
中美医学科学与工程协会会员
广东省医疗行业协会血液病 分会主任委员
分会主任委员
广东省医师协会血液科医师分会副主任委员
广东省医疗安全协会血液学分会副主任委员
广东省健康管理学会血液病分会副主任委员
广州抗癌协会理事会常务理事
广东省医学会血液病学分会常员
广东省抗癌协会血液学分会常委
从事血液病学医教研工作30余年,目前担任教育部硕博士论文的评审专家,自2006年担任欧洲SCI杂志AntiCancer Drugs 常务编委,Ann Hematol 编委。目前已主持国家自然科学基金5项,省部级科研基金10余项,在国内外核心期刊发表论文200余篇,其中在Ann Oncol(IF>50)、American J Hematol. Blood 等杂志发表SCI收录论文50余篇。
