
案例实录:双靶序贯奈拉替尼强化辅助治疗,助力三阳性乳腺癌全程管理
近年来,≤35岁年轻乳腺癌 的全球发病率呈现上升趋势,其肿瘤生物学行为常表现为更高侵袭性、更高增殖活性(如Ki67指数偏高)和相对更差的预后特征[1];其中,三阳性乳腺癌作为一种特殊亚型,同时表达雌激素
的全球发病率呈现上升趋势,其肿瘤生物学行为常表现为更高侵袭性、更高增殖活性(如Ki67指数偏高)和相对更差的预后特征[1];其中,三阳性乳腺癌作为一种特殊亚型,同时表达雌激素 受体(ER)、孕激素
受体(ER)、孕激素 受体(PR)和人表皮生长因子受体2(HER2),约占所有乳腺癌的5-10%[2],这类肿瘤兼具激素驱动和HER2信号通路激活的双重特征,治疗需同步抑制激素通路与HER2靶点,策略复杂且需高度个体化调整[3]。
受体(PR)和人表皮生长因子受体2(HER2),约占所有乳腺癌的5-10%[2],这类肿瘤兼具激素驱动和HER2信号通路激活的双重特征,治疗需同步抑制激素通路与HER2靶点,策略复杂且需高度个体化调整[3]。
年轻三阳性乳腺癌患者面临多重治疗挑战:其一,肿瘤异质性强,HER2与激素通路的交互作用可能导致内分泌耐药或靶向治疗响应不足[4];其二,高复发风险,年轻患者淋巴结转移率高,远期复发(如脑转移)风险显著[5];其三,需在强化治疗的同时兼顾生育功能保留、卵巢保护及长期生活质量平衡[6]。目前,基于NeoSphere、APHINITY等研究[7-8],HP双靶方案(曲妥珠单抗 +帕妥珠单抗
+帕妥珠单抗 )联合化疗已成为HER2阳性乳腺癌的标准新辅助及辅助治疗,对于年轻TPBC患者,新辅助治疗既可实现肿瘤降期与保乳机会提升(使不可手术肿瘤转化为可手术,并提高病理完全缓解率),又可作为体内药敏测试,通过术后病理反应(如MP分级、RCB指数)动态评估治疗敏感性,从而指导后续辅助策略[9]。
)联合化疗已成为HER2阳性乳腺癌的标准新辅助及辅助治疗,对于年轻TPBC患者,新辅助治疗既可实现肿瘤降期与保乳机会提升(使不可手术肿瘤转化为可手术,并提高病理完全缓解率),又可作为体内药敏测试,通过术后病理反应(如MP分级、RCB指数)动态评估治疗敏感性,从而指导后续辅助策略[9]。
值得注意的是,即使患者通过新辅助治疗达到良好反应(如RCB-I级),存在的微小残留病灶(MRD)仍能导致疾病的复发。而奈拉替尼 作为一种口服泛HER酪氨酸激酶抑制剂,可不可逆抑制HER1/2/4靶点,能够突破耐药屏障(通过抑制HER2异源二聚体形成及下游PI3K/AKT等信号通路,克服曲妥珠单抗耐药)[10]、降低脑转移风险(凭借血脑屏障穿透能力,预防HER2阳性乳腺癌的中枢神经系统转移)[11]和远期生存获益(ExteNET研究[12]证实其可显著改善高危HER2阳性患者的5年无病生存率,尤其在激素受体阳性亚组中获益更显著)。
作为一种口服泛HER酪氨酸激酶抑制剂,可不可逆抑制HER1/2/4靶点,能够突破耐药屏障(通过抑制HER2异源二聚体形成及下游PI3K/AKT等信号通路,克服曲妥珠单抗耐药)[10]、降低脑转移风险(凭借血脑屏障穿透能力,预防HER2阳性乳腺癌的中枢神经系统转移)[11]和远期生存获益(ExteNET研究[12]证实其可显著改善高危HER2阳性患者的5年无病生存率,尤其在激素受体阳性亚组中获益更显著)。
综上所述,年轻三阳性乳腺癌的治疗需以“全程管理”为核心,整合新辅助化疗、双靶治疗、放疗及内分泌治疗,并基于治疗反应动态升级策略;奈拉替尼的辅助强化代表了对高危人群的精准干预,未来需进一步探索生物标志物(如ERBB2突变、TILs水平)以优化其应用时机与人群筛选,为实现年轻患者长期生存与生活质量提升提供新方向[13]。本文特别分享一例29岁绝经 前三阳性乳腺癌的治疗经历。入院时初诊左乳浸润性癌伴腋窝淋巴结转移,免疫组化提示三阳性特征(ER/PR阳性,HER2 3+,Ki67 30%)。术前予TCbHP方案新辅助化疗,并给予戈舍瑞林
前三阳性乳腺癌的治疗经历。入院时初诊左乳浸润性癌伴腋窝淋巴结转移,免疫组化提示三阳性特征(ER/PR阳性,HER2 3+,Ki67 30%)。术前予TCbHP方案新辅助化疗,并给予戈舍瑞林 保护卵巢,化疗后行保乳手术,术后病理接近完全缓解(MP 4级,RCB-Ⅰ级),随后予放疗、内分泌治疗及HP双靶维持,最终采用奈拉替尼辅助强化。病例体现了年轻三阳性乳腺癌的全程管理策略。
保护卵巢,化疗后行保乳手术,术后病理接近完全缓解(MP 4级,RCB-Ⅰ级),随后予放疗、内分泌治疗及HP双靶维持,最终采用奈拉替尼辅助强化。病例体现了年轻三阳性乳腺癌的全程管理策略。
许志宏 医生
南昌市人民医院 乳腺外三科
主治医师 医学硕士
中国抗癌协会会员

擅长乳腺良性肿瘤的微创治疗和乳腺癌的综合治疗。
主持省卫健委课题1项,参与学术论文发表3篇,其中以第一作者身份发表 SCI 论文2篇。
魏文嵩 教授
南昌市人民医院 乳腺外科
主任医师
江西省中医药学会乳腺病专业委员会常委
江西省康复养生协会乳腺疾病康复专业委员会常委
江西省妇幼保健与优生优育协会乳腺专业常委
江西省研究型学会乳腺肿瘤分会委员
病例介绍
患者:女,29岁,首次入院时间:2023.10.17
主诉:发现左乳肿块1周。
婚育月经史:已婚未育,12岁 7/30 2023年09月22日。
既往史及家族史:无高血压 、糖尿病
、糖尿病 等慢性病史;否认肿瘤家族史。
等慢性病史;否认肿瘤家族史。
查体:ECOG 1分,双乳基本对称,双乳头居同一水平线,左乳头凹陷。双乳皮肤无橘皮征、酒窝征。左乳内上象限距离乳头3cm处,可触及约4.0cm×2.5cm大小肿物,质硬,活动度差,边界不清,无压痛。右乳内未及明显肿块。左腋下可触及肿大淋巴结,2cm×1cm,质地硬,右侧腋下及双锁骨上下未触及肿大淋巴结。
影像学检查
2023年10月14日 乳腺彩超
左侧低回声区,建议完善相关检查,BI-RADS 4A类
左腋下淋巴结肿大
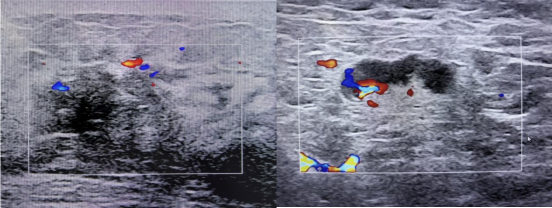
图1 双侧乳腺及双腋下锁骨上下彩超
2023年10月18日 乳腺磁共振
左乳内侧缘不规则团块状异常强化信号影 BI-RADS 6类
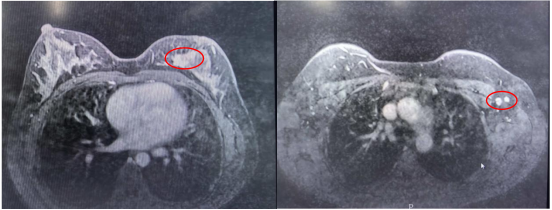
图2 磁共振所示左乳病灶及左腋下淋巴结
2023年10月17日 穿刺病理报告及免疫组化
(左乳)浸润性癌,见导管原位癌
(左腋窝淋巴结)转移性低分化癌,结合病史及免疫组化符合乳腺来源
(免疫组化)ER(约80%+,强),PR(约30%+,中),C-erbB-2(3+),Ki-67(5%)
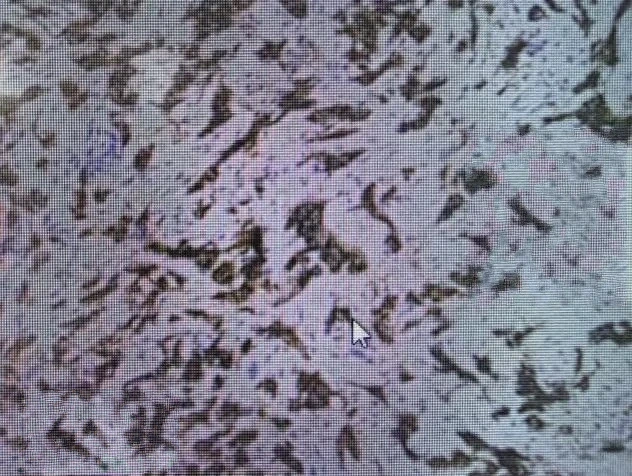
图3 HER2免疫组化染色
其他检查未见明显异常
初步诊断
左侧乳腺癌伴同侧腋窝淋巴结转移,cT2N1M0,IIB期,Her-2阳性型/Luminal B型
治疗经过及疗效评价
新辅助化疗
2023年10月-2024年02月:患者行TCbHP治疗,q3w × 6周期,具体为:多西他赛(75mg/m2,ivgtt)+卡铂(AUC 6,ivgtt)+ 曲妥珠单抗(首次8mg/kg,后续6mg/kg,ivgtt)+帕妥珠单抗(首次840mg,后续420mg,ivgtt)
新辅助化疗期间予戈舍瑞林保护卵巢
新辅助治疗后影像学复查结果如下:
疗效评价:PR
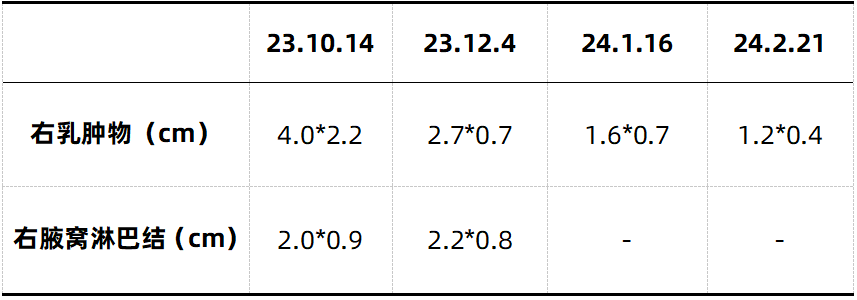
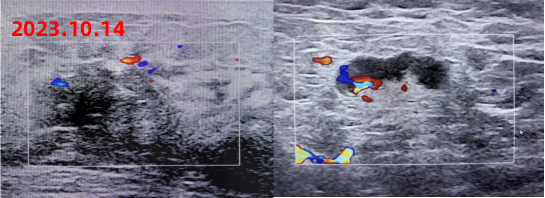
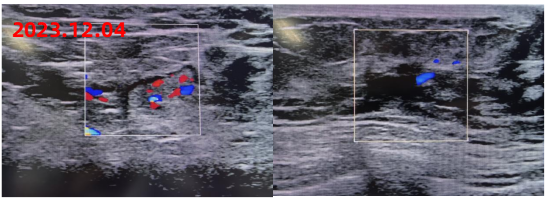
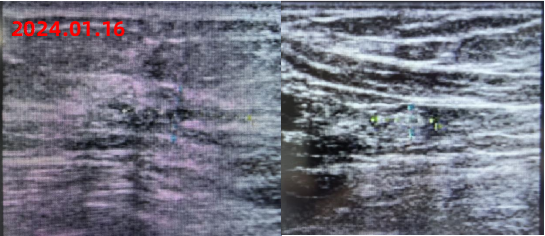
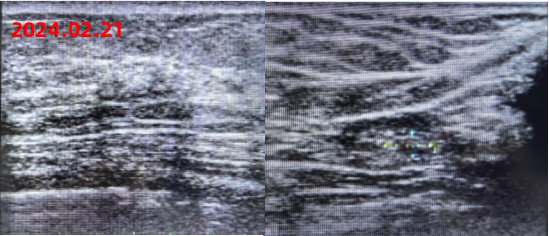
手术治疗
于2024年2月26日在全麻下行左乳癌保乳改良根治术,术后病理如下:
(左乳)浸润性导管癌,评分:3+2+1=6分,组织学II级,肿瘤约2.5 × 1mm大小,见少量导管原位癌(中级别),脉管(-)
区域淋巴结未见癌转移(0/16,其中4枚淋巴结见化疗反应),分组如下:腋窝淋巴结(0/11),腋尖淋巴结(0/5)。(左乳表面、上方、下方、内侧、外侧及基底切缘)均为阴性
新辅助治疗反应的评估: 残留癌负荷系统(RCB):RCB分值1.2333,RCB-I级。 Miller-Payne评分系统分级:4级
免疫组化:ER(约90%+,强),PR(约20%+,中),C-erbB-2(3+),Ki-67(2%)
后续治疗
1. 乳腺癌术后,予曲妥珠单抗+帕妥珠单抗双靶向治疗维持1年,于2024年10月结束静脉双靶向治疗
2. 乳腺癌术后,予戈舍瑞林联合依西美坦内分泌治疗
3. 2024年4月-5月期间,行辅助放疗,IMRT 6MV X线,患侧乳房+锁骨区+瘤床boost,放疗剂量Dt50Gy/25F+10Gy/5F,放疗技术IMRT
4. 静脉靶向治疗结束后予奈拉替尼(240mg po qd)辅助强化治疗至今。截至目前,未见肿瘤复发及转移征象。奈拉替尼治疗期间,相关不良反应轻微,主要表现为轻度腹泻,经对症处理后可控,整体安全性良好。
病例小结
该病例是一位非常年轻的局部晚期、三阳性的乳腺癌患者,符合新辅助化疗的适应症,按着指南的要求,给予TCbHP方案进行新辅助治疗,考虑患者已婚未育,在化疗期间予戈舍瑞林保护卵巢。新辅助化疗后肿瘤范围较前所缩小,患者成功完成了保乳手术,术后病理接近完全缓解(MP 4级,RCB-Ⅰ级)。到目前为止并无T-DM1优于HP双靶向治疗的阳性结果,所以该患者虽然未达到pCR,但考虑到双靶新辅助化疗后肿瘤退缩明显,后续仍予HP双靶维持治疗1年。基于乳腺癌复发模式的研究,三阳性的患者呈现出持续复发的风险;其次,多项研究(HERA、APHINITY、KATHERINE)结果表明基于大分子抗HER2单抗类药物的辅助治疗未降低脑转移的风险,而奈拉替尼在ExteNET研究中显示出降低脑转移的优势。该患者29岁,未来的累计复发风险高,双靶治疗结束之后继续给予了奈拉替尼强化治疗。该病例在治疗的全过程,既严格遵循指南的推荐,又落实了个体化治疗的理念,每个治疗节点方案的选择,均有充分的循证医学证据作支撑,治疗后随访至今,患者状态良好,无复发转移迹象。
专家点评
1. 新辅助治疗的精准响应评估指导后续策略
本例通过新辅助化疗后病理评估显示RCB-Ⅰ级(残留癌负荷指数1.2333)及免疫组化动态变化(Ki67从30%显著降至2%),证实了治疗方案的高度敏感性。这一发现与KATHERINE研究[14]的重要结论高度一致:即使是未达到病理学完全缓解(non-pCR)的患者,接受后续强化治疗(如T-DM1)仍可显著改善生存预后。RCB分级系统为此类患者提供了可靠的量化评估工具,其价值在于能够精确区分不同级别的治疗反应,从而指导临床医生制定个体化的后续治疗方案,有效避免治疗不足或过度治疗的问题。值得注意的是,本例中MP分级达到4级(接近完全缓解),进一步验证了新辅助治疗的显著效果。
2. 双靶向联合奈拉替尼强化覆盖全程风险
初始治疗采用HP双靶方案(曲妥珠单抗+帕妥珠单抗)是基于里程碑式的CLEOPATRA研究[15],该研究证实此方案可显著改善HER2阳性晚期乳腺癌患者的总生存期。后续奈拉替尼强化治疗则依据ExteNET研究[16]的循证医学证据:对于高危HER2阳性乳腺癌患者,奈拉替尼辅助治疗可降低27%的侵袭性疾病复发风险(HR=0.73),且在激素受体阳性亚组中获益更为显著(HR=0.60)。这种序贯靶向治疗策略实现了从外周至中枢神经系统的全程保护,特别针对年轻患者高发的脑转移风险。值得一提的是,奈拉替尼的血脑屏障穿透特性为其预防中枢神经系统转移提供了独特的药理优势。
3. 年轻患者个体化管理的多维平衡
病例中采用戈舍瑞林+依西美坦的内分泌治疗方案,体现了对年轻患者卵巢功能保护与治疗效果的双重考量。根据ESO-ESMO共识[17]推荐,年轻乳腺癌患者的生育力保存需要早期干预,使用GnRH类似物联合内分泌治疗可显著降低卵巢功能衰竭风险(绝对风险降低约15-20%),同时维持必要的治疗强度。这种个体化管理策略还需要综合考虑患者的生育需求、遗传风险评估(如BRCA基因检测)以及长期生活质量问题,体现了现代乳腺癌诊疗中"治疗效果与生活质量并重"的理念。
4. 生物标志物动态变化的临床意义
新辅助治疗后观察到的ER表达升高(60%→90%)、PR表达降低(60%→20%)的现象,反映了治疗压力下的肿瘤克隆筛选和演化过程。这种生物标志物的动态变化具有重要的临床意义:ER表达增加可能提示肿瘤对内分泌治疗的敏感性增强,而PR丢失往往与PI3K/AKT信号通路异常激活相关[18],可能导致内分泌治疗耐药。这种现象提示我们需要:①加强治疗过程中的生物标志物监测;②考虑采用CDK4/6抑制剂等联合治疗策略克服耐药;③未来探索针对PI3K/AKT通路的靶向药物(如alpelisib)与内分泌治疗的联合方案,为患者提供更加精准的治疗选择。
结语
本例展示了年轻三阳性乳腺癌的规范化治疗路径:基于新辅助治疗反应动态升级策略,融合化疗、靶向、内分泌及放疗的多模态管理,最终通过奈拉替尼强化实现风险控制。未来需关注生物标志物演变规律及耐药机制,进一步优化个体化治疗。
审校:Babel
排版:Babel
执行:Faline
本平台旨在为医疗卫生专业人士传递更多医学信息。本平台发布的内容,不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议。如该等信息被用于了解医学信息以外的目的,本平台不承担相关责任。本平台对发布的内容,并不代表同意其描述和观点。若涉及版权问题,烦请权利人与我们联系,我们将尽快处理。



