
菲常血液丨李菲教授:DEB研究赋能,为双表达弥漫大B细胞淋巴瘤患者提供可及新选择
目前,DE-DLBCL仍存在显著未满足的临床需求,尤其是传统化疗方案对此类患者的长期生存率提升有限,患者临床结局较差,5年总生存(OS)率仅30%左右2。DE-DLBCL患者具有异质性,目前尚无标准的治疗方案。表观遗传调控机制的探索为DLBCL治疗提供了新思路,其中组蛋白去乙酰化酶抑制剂(HDACi)西达本胺联合多柔比星已在临床前研究中显示可明显抑制DLBCL细胞生长,且探索性临床发现西达本胺单药治疗DLBCL有效、安全性可控。
在此背景下,研究者开展了一项III期随机对照试验——DEB研究(NCT04231448),通过严谨的设计验证了西达本胺+R-CHOP方案在DE-DLBCL中的临床价值2。全国共45家研究中心参与DEB研究,在2020年5月21日-2022年7月25日期间共纳入423例DE-DLBCL患者,入组患者按1:1比例随机分配至试验组(西达本胺+R-CHOP,211例)或安慰剂组(安慰剂+R-CHOP,212例),完成6周期诱导治疗后获得完全缓解(CR)的患者继续接受西达本胺或安慰剂维持治疗(最长24周)(图1)。其中试验组与安慰剂组分别有80.6%和77.8%患者完成了总计6个周期的联合治疗,64.0%和52.4%的患者接受了维持治疗。研究的主要终点为无事件生存期(EFS),关键次要终点为完全缓解率(CRR),其他次要终点包括无病生存期(DFS)、无进展生存期(PFS)、OS、不良事件(AEs)等。
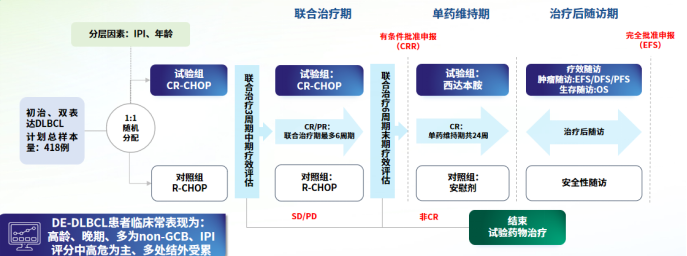
图1 研究设计
中位随访13.9个月时,对于研究的主要终点EFS,试验组中位EFS尚未达到,长于安慰剂组的18.3个月;24个月EFS率方面,试验组较安慰剂组显著提升12.7%(58.9% vs 46.2%,P=0.018)(图2)。
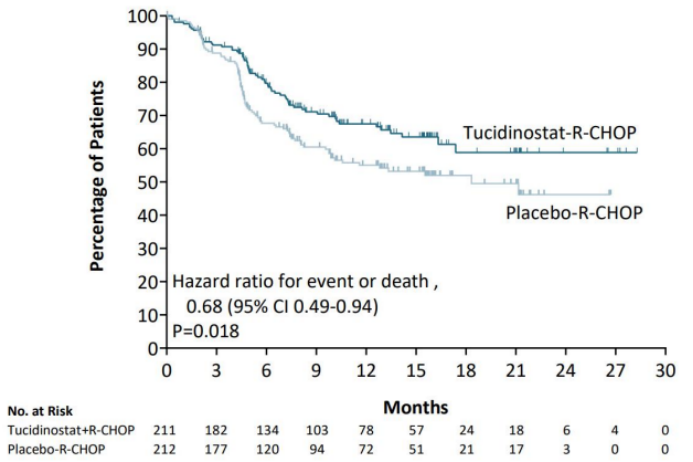
图2 ITT患者EFS情况
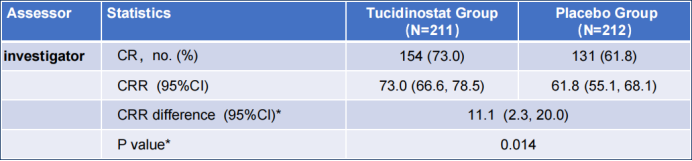
对于关键次要终点CRR,联合治疗结束时的试验组与安慰剂组CRR差异达11.1%,分别为73.0%和61.8%(P=0.014),提示西达本胺+R-CHOP方案可使更多患者实现深度缓解(表1)。研究显示对于EFS、CRR,在几乎所有亚组中(包括IPI评分为3-5 vs 2;年龄≤60岁 vs >60岁),试验组对比安慰剂组患者均获益更多。
表1 ITT患者CRR情况
试验组相比安慰剂组在PFS方面也呈现出积极趋势,24个月PFS率分别为67.3%和57.0%。两组24个月OS率分别为82.8%和76.5%,由于截至中期分析的截止日期时OS事件有限,目前无法确定趋势,需要更长时间的随访验证。
在安全性方面,两组安全性均符合预期,未发现新的安全性问题。尽管试验组3级血液学AEs的发生率普遍高于安慰剂组(表2),但大多数患者能够耐受并完成计划的治疗周期。两组均无观察到显著的心脏毒性、肝毒性和肾毒性。两组的非血液学AEs主要为低钾血症、肺炎,大多数严重AEs发生在联合治疗期间。
表2 两组联合治疗期间的血液学AEs
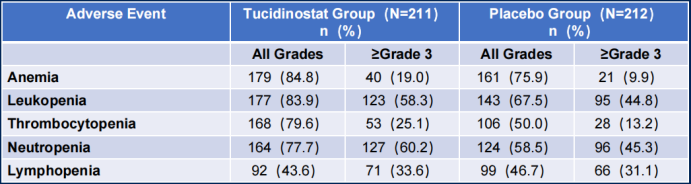
DEB研究结果显示,西达本胺+R-CHOP方案有效且耐受性良好,安全性可控,此方案可能成为DE-DLBCL患者新一线治疗方案。
李菲教授
DLBCL作为常见NHL之一,包含多种独特分子亚型。其中,存在MYC和BCL2双表达而无基因重排的DLBCL被称为DE-DLBCL,约占总体DLBCL的30%2。近年研究发现,与其他DLBCL患者相比,DE-DLBCL患者预后不佳,5年PFS率仅为27%-32%,5年OS率为30%-36%,即使使用强化疗方案,例如DA-EPOCH-R(剂量调整后的依托泊苷、泼尼松、长春新碱、环磷酰胺、多柔比星、利妥昔单抗)依然未观察到生存获益,DE-DLBCL患者亟待更有效的治疗手段3。
在针对DLBCL的多年探索中,研究者发现表观遗传失调通常与DLBCL的发病机制及发展密切相关,西达本胺作为一种选择性HDACi,其DEB研究结果表明,西达本胺联合方案的24个月EFS率显著高于对照组(HR=0.68,P=0.018),表明西达本胺联合方案可有效延缓疾病进展或复发;两组CRR差值为11.1%(P=0.014),实现CR则意味着患者有望获得更佳的生存获益2。在安全性方面,尽管西达本胺联合方案组的≥3级血液学AEs的发生率一般高于对照组,但大多数患者能够耐受并完成计划的治疗周期,表明西达本胺的联合方案总体耐受性较好,安全性可控。综上,西达本胺联合R-CHOP方案对于初治DE-DLBCL患者是一种可行且有效的方案。
在临床上,DLBCL的诊疗需以分子分型为核心,通过免疫组化及基因检测等明确MYC/BCL2双表达特征,结合IPI评分与影像学进行风险分层4。治疗中需关注血液学毒性管理,通过支持治疗、感染防控及多学科协作平衡方案的疗效与安全性。基于DEB研究等循证医学证据,R-CHOP联合表观遗传调节药物已成为一线治疗的重要选择之一。在最新发布的《CSCO淋巴瘤诊疗指南》(2025年版)中,对于初治DE-DLBCL患者,西达本胺联合R-CHOP方案被列为I级推荐(1A类证据)。此外,随着西达本胺联合R-CHOP方案首次进入2024版国家医保目录,其治疗可及性将进一步提高,惠及更多淋巴瘤患者。未来仍需依托精准医学优化分层,探索联合策略,并通过长期随访验证,最终实现从诊断到康复的全程化管理,改善患者生存质量与预后。
李菲 教授
南昌大学第一附属医院血液病中心主任医师、教授、博士生/博士后合作导师
江西省血液系统疾病重点实验室主任
江西省血液病临床医学研究中心主任
江西省血液病医疗质控中心主任
南昌大学淋巴肿瘤疾病研究所主任
中华血液学杂志通讯编委,临床血液学杂志、中国临床肿瘤杂志编委
中华医学会血液学分会常务委员
中华医学会血液学分会淋巴疾病学组委员
国家血液病质控中心专家委员会委员
江西省医学会血液学分会候任主委
中国CSCO骨髓瘤专家委员会副主任委员
中国CSCO抗淋巴瘤联盟委员
中国医药教育协会造血干细胞移植和免疫治疗分会副主任委员
中国抗癌协会血液肿瘤(肿瘤血液)专委会委员
中国慢淋专家组委员
中国噬血细胞综合征联盟专家组委员
中国女医师协会靶向专委会血小板病副组长
参考文献
1. Cai Z, et al. 2020;10:1007. doi:10.3389/fonc.2020.01007.
2. Weili Zhao et al. JCO 42, LBA7003-LBA7003(2024).
3. Chen X, et al. Ther Adv Hematol. 2024;15:20406207241292446.
4. 中华人民共和国国家卫生健康委员会. 中国肿瘤临床与康复,2023,30(3):135-158.



