
持续存在的肺结节?千万别落入惯性诊断的陷阱!这套评估思路可作参考
病例介绍
一位40岁女性患者,无吸烟史、无重大病史。因右侧胁腹痛到急诊科就诊,疑似肾结石 病。
病。
腹部和盆腔CT扫描(静脉注射对比剂)显示患者左侧有一颗3-4毫米的输尿管结石 ,伴有轻度肾积水;右下叶后基底段有一个2.4厘米的亚实性肺结节
,伴有轻度肾积水;右下叶后基底段有一个2.4厘米的亚实性肺结节 ,内含致密磨玻璃及部分实性衰减成分,所见其余肺野无异常发现(图1)。泌尿科医生在患者初次就诊后6周后安排的随访CT成像中,2.4厘米的亚实性肺结节持续存在,其大小及实性成分(测量至少8毫米)均未见明显变化(图2)。患者被转诊至肺结节门诊。
,内含致密磨玻璃及部分实性衰减成分,所见其余肺野无异常发现(图1)。泌尿科医生在患者初次就诊后6周后安排的随访CT成像中,2.4厘米的亚实性肺结节持续存在,其大小及实性成分(测量至少8毫米)均未见明显变化(图2)。患者被转诊至肺结节门诊。
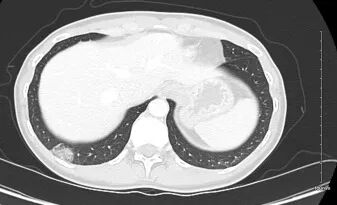
图1. 腹部盆腔增强CT扫描显示一个2.4厘米的亚实性肺结节,内含致密磨玻璃及部分实性衰减成分。图像以肺窗显示,层厚2.5毫米。
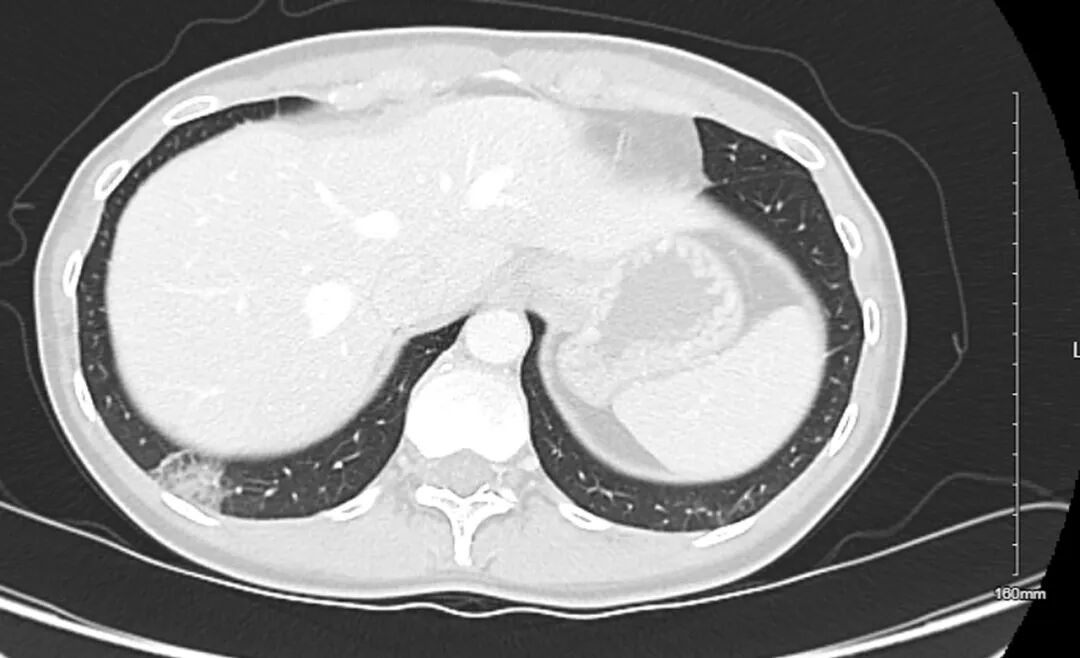
图2. 初次检查(图1)后6周复查的腹部盆腔增强CT扫描图像。结果显示,2.4厘米的亚实性肺结节持续存在,其大小及实性成分均未见明显变化。
门诊就诊时,患者一般状况良好,无不适。未服用任何药物;近期无咳嗽 、发热
、发热 或寒战;静息及活动时均无胸痛
或寒战;静息及活动时均无胸痛 或呼吸困难
或呼吸困难 ;无职业暴露史;无肺癌
;无职业暴露史;无肺癌 或其他肺部疾病家族史;无烟草使用史(包括被动吸烟或二手烟暴露);诊室肺量计检查结果正常。
或其他肺部疾病家族史;无烟草使用史(包括被动吸烟或二手烟暴露);诊室肺量计检查结果正常。
该持续存在的部分实性结节的初步鉴别诊断包括局灶性肺炎或其他感染性病因;但考虑到其无症状且持续存在长达6周,可能性被认为较低。同时考虑了肺栓塞 ,因为该结节的亚实性外观可能代表了缺血与进展性梗死的复合表现。鉴于其致密磨玻璃成分及部分实性衰减特征,也存在腺癌谱系恶性肿瘤的可能性。
,因为该结节的亚实性外观可能代表了缺血与进展性梗死的复合表现。鉴于其致密磨玻璃成分及部分实性衰减特征,也存在腺癌谱系恶性肿瘤的可能性。
电子计算机断层扫描(CT)/正电子发射计算机断层显像 (PET)扫描显示右下叶部分实性肺结节大小无变化,氟代脱氧葡萄糖
(PET)扫描显示右下叶部分实性肺结节大小无变化,氟代脱氧葡萄糖 摄取程度较低,最大标准化摄取值(SUVmax)为2.2(图3)。CT/PET扫描未发现异常淋巴结,也未发现肝脏或肾上腺病变。鉴于实性成分≥8毫米的亚实性结节往往具有更具侵袭性的特征,认为有必要进行进一步检查。与患者讨论了经胸壁穿刺活检、导航支气管镜以及电视辅助胸腔镜手术(VATS)活检等方案,患者最终选择了外科手术。
摄取程度较低,最大标准化摄取值(SUVmax)为2.2(图3)。CT/PET扫描未发现异常淋巴结,也未发现肝脏或肾上腺病变。鉴于实性成分≥8毫米的亚实性结节往往具有更具侵袭性的特征,认为有必要进行进一步检查。与患者讨论了经胸壁穿刺活检、导航支气管镜以及电视辅助胸腔镜手术(VATS)活检等方案,患者最终选择了外科手术。
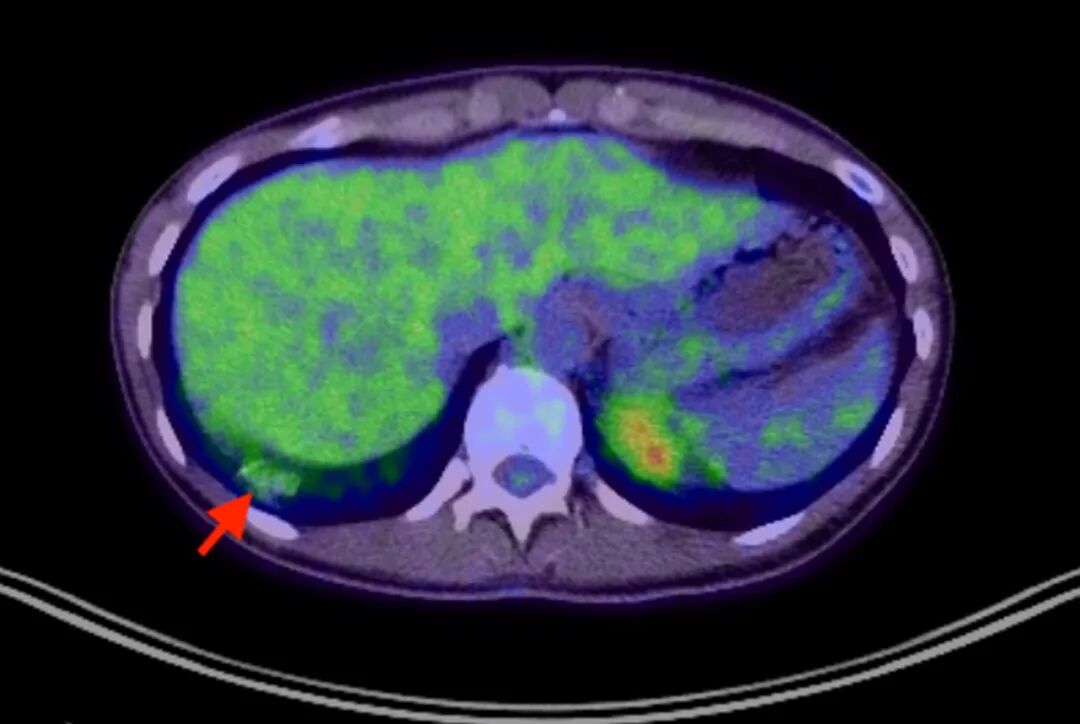
图3. CT/PET融合图像显示,右下叶部分实性结节存在轻度氟代脱氧葡萄糖摄取增高(红色箭头标示)。
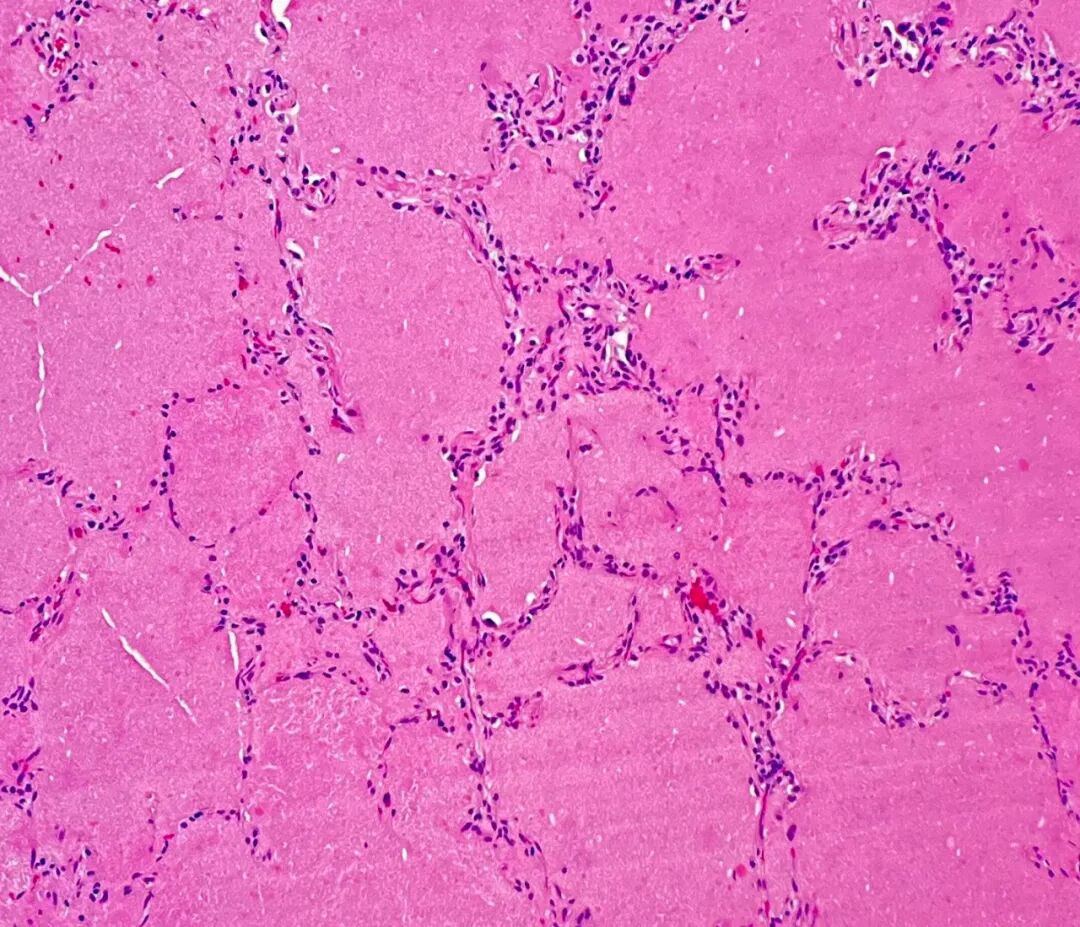
图4. 苏木精-伊红(H&E)染色显示,肺泡腔内充满弥漫性蛋白质样物质。
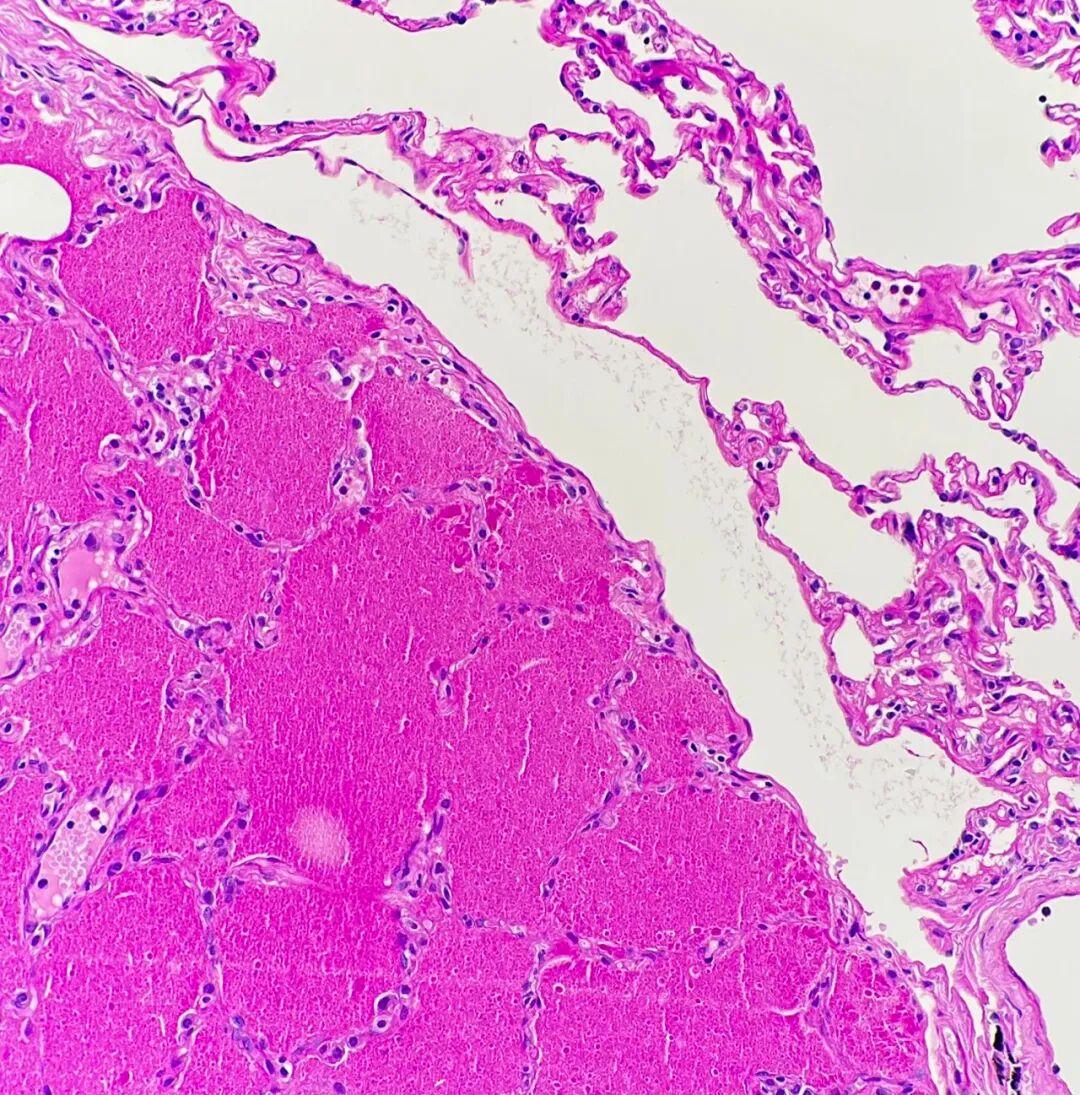
图5. 过碘酸雪夫(PAS)染色突出显示终末细支气管和肺泡腔内PAS阳性物质沉积的区域。图像右上方可见正常肺组织作为对照。
诊断:局灶性肺泡蛋白质沉积症(PAP)
讨论
影像学讨论
PAP典型的胸片表现为双肺浸润影,以肺门周围及基底部分布为主,肺中下野多见,不伴有胸腔积液 。虽类似于肺水肿
。虽类似于肺水肿 ,但缺乏胸腔积液及心脏扩大征象。初诊胸片发现异常后,通常进一步行高分辨率胸部CT(HRCT)检查,此为评估PAP的最佳影像学方法。HRCT典型表现为弥漫性磨玻璃影,伴小叶内间隔及小叶间隔增厚,后者可叠加于磨玻璃影之上,形成多边形结构,即所谓“铺路石征”。此征象虽提示PAP,但非特异性,亦可见于肺水肿、感染性肺炎(尤其是肺孢子菌肺炎
,但缺乏胸腔积液及心脏扩大征象。初诊胸片发现异常后,通常进一步行高分辨率胸部CT(HRCT)检查,此为评估PAP的最佳影像学方法。HRCT典型表现为弥漫性磨玻璃影,伴小叶内间隔及小叶间隔增厚,后者可叠加于磨玻璃影之上,形成多边形结构,即所谓“铺路石征”。此征象虽提示PAP,但非特异性,亦可见于肺水肿、感染性肺炎(尤其是肺孢子菌肺炎 )、弥漫性肺泡损伤、肺泡出血、过敏性肺炎
)、弥漫性肺泡损伤、肺泡出血、过敏性肺炎 及多种肺间质纤维化
及多种肺间质纤维化 。尽管影像学表现可能相当显著,但PAP的一个关键特点是患者的临床症状(通常相对轻微)与其影像学异常严重程度之间存在显著不符。本病例中,唯一的影像学发现仅为右下叶基底段一个2.4厘米的磨玻璃部分实性结节,这通常不会将PAP作为首要鉴别。由于异常区域相对局限,病变内部未见明确的铺路石征。若存在此征象,局灶性PAP或可纳入鉴别诊断范围。尽管患者缺乏肺癌的传统危险因素,但病灶的大小、部分实性成分及其在随访影像中的持续性,使得恶性肿瘤成为鉴别诊断中的重点考虑。病灶靠近膈肌的位置使得经皮穿刺活检的可行性降低。导航支气管镜虽为备选方案,但因病灶位置靠外周、气胸
。尽管影像学表现可能相当显著,但PAP的一个关键特点是患者的临床症状(通常相对轻微)与其影像学异常严重程度之间存在显著不符。本病例中,唯一的影像学发现仅为右下叶基底段一个2.4厘米的磨玻璃部分实性结节,这通常不会将PAP作为首要鉴别。由于异常区域相对局限,病变内部未见明确的铺路石征。若存在此征象,局灶性PAP或可纳入鉴别诊断范围。尽管患者缺乏肺癌的传统危险因素,但病灶的大小、部分实性成分及其在随访影像中的持续性,使得恶性肿瘤成为鉴别诊断中的重点考虑。病灶靠近膈肌的位置使得经皮穿刺活检的可行性降低。导航支气管镜虽为备选方案,但因病灶位置靠外周、气胸 风险较高、且靠近膈肌,实施存在限制。结合病灶尺寸较大及患者希望明确诊断的意愿,最终选择VATS活检。
风险较高、且靠近膈肌,实施存在限制。结合病灶尺寸较大及患者希望明确诊断的意愿,最终选择VATS活检。
CT/PET扫描在诊断弥漫性PAP中通常无明确作用。但有文献报道,在已经进行CT/PET检查的PAP病例中可观察到轻度氟代脱氧葡萄糖摄取。推测其机制可能与PAP发病过程中涉及的炎性细胞对葡萄糖的利用有关。
病理学讨论
病理学检查对PAP的诊断具有高度敏感性和特异性。组织学上,可见小动脉和细支气管结构基本保留,炎症反应轻微或缺如,可因II型肺泡上皮细胞增生致部分间隔增厚。最具特征性的改变是,终末细支气管及肺泡腔内充满大量脂蛋白样物质,PAS染色呈强阳性,提示含有大量多糖及黏液物质。此发现符合表面活性物质代谢异常导致其积聚的病理生理过程。图4(H&E染色)显示肺泡腔内弥漫分布的蛋白质样物质。图5(PAS染色)则清晰显示了填充于终末支气管及肺泡腔内的PAS阳性物质,与相邻的正常肺组织形成鲜明对比,充分展现了PAP病例病理学检查的独特性和诊断价值。此外,Grocott-Gomori六胺银染色结果为阴性,排除了肺孢子菌感染(此为PAP的一个重要鉴别诊断)。与本病例的影像学表现不同,其病理学特征完全符合典型的PAP表现,从而确立了诊断。
临床讨论
PAP属罕见病,当以局灶性分布出现时,临床几乎不予考虑。在更常见的弥漫性影像学表现的病例中,初始评估多因患者出现非特异性症状而启动,如活动后进行性呼吸困难、咳嗽、咳痰,查体可闻及爆裂音。肺功能检查 常用于评估呼吸功能损害程度,同时通过检测抗粒细胞-巨噬细胞集落刺激因子(GM-CSF)抗体水平、评估是否存在继发性病因的危险因素(如职业暴露、血液系统恶性肿瘤或异基因细胞移植史)。这些评估有助于将PAP分为以下三类:原发性(自身免疫性或遗传性)、继发性或先天性。在成人发病的PAP中,>90%的病例属于自身免疫性,患者体内可检测到抗GM-CSF抗体。GM-CSF作为巨噬细胞成熟和表面活性物质分解代谢不可或缺的介质的发现,是理解多数类型PAP发病机制的关键。肺泡巨噬细胞是清除表面活性物质降解产物的主要细胞。抗GM-CSF自身抗体降低了其生物利用度,从而损害肺泡巨噬细胞的正常功能,导致脂蛋白样物质在肺泡腔内积聚,并产生典型的影像学与病理学表现。
常用于评估呼吸功能损害程度,同时通过检测抗粒细胞-巨噬细胞集落刺激因子(GM-CSF)抗体水平、评估是否存在继发性病因的危险因素(如职业暴露、血液系统恶性肿瘤或异基因细胞移植史)。这些评估有助于将PAP分为以下三类:原发性(自身免疫性或遗传性)、继发性或先天性。在成人发病的PAP中,>90%的病例属于自身免疫性,患者体内可检测到抗GM-CSF抗体。GM-CSF作为巨噬细胞成熟和表面活性物质分解代谢不可或缺的介质的发现,是理解多数类型PAP发病机制的关键。肺泡巨噬细胞是清除表面活性物质降解产物的主要细胞。抗GM-CSF自身抗体降低了其生物利用度,从而损害肺泡巨噬细胞的正常功能,导致脂蛋白样物质在肺泡腔内积聚,并产生典型的影像学与病理学表现。
大约54%的PAP可通过HRCT联合支气管肺泡灌洗检查确诊,34%需要增加经支气管肺活检 ,仅7%需要外科手术活检。本病例中,临床及影像学均未怀疑PAP,为求确诊而采取了外科活检。该患者无任何呼吸系统症状,若非因其他原因进行CT检查,此异常将不会被发现。
,仅7%需要外科手术活检。本病例中,临床及影像学均未怀疑PAP,为求确诊而采取了外科活检。该患者无任何呼吸系统症状,若非因其他原因进行CT检查,此异常将不会被发现。
该患者的局灶性PAP病灶已通过楔形切除完全移除,随访影像学未见复发。本病例中一个遗留问题是患者是否存在复发(局灶性或弥漫性)的可能。至少有一项类似病例报告显示,一名46岁女性在初次切除局灶性PAP病灶后5年出现复发。尽管未检测本患者目前的抗GM-CSF抗体水平,但此举或可于现在或将来(尤其当出现呼吸系统症状时)予以考虑。鉴于此类病例的罕见性,目前尚无关于是否应追溯性检测患者抗GM-CSF抗体水平的正式建议。此外,在未出现任何肺部症状的情况下,进行影像学监测获益的可能性较低。
本病例突显了在处理肺结节,尤其是对于缺乏恶性肿瘤传统危险因素的患者中出现较大病灶时,保持广泛鉴别诊断的重要性。除局灶性PAP外,其他罕见疾病(如局灶性隐源性机化性肺炎、结节性硬化症 中的多灶性微小结节型肺泡上皮增生、局灶性肺泡出血、脂质性肺炎等)也需考虑鉴别。
中的多灶性微小结节型肺泡上皮增生、局灶性肺泡出血、脂质性肺炎等)也需考虑鉴别。
结论
该青年女性,因偶然发现右下叶基底段2.4厘米磨玻璃结节就诊。鉴别诊断广泛,首要考虑为腺癌谱系原发性肺癌。经全面评估后,进行VATS辅助下右下叶楔形切除术,术后病理确诊为局灶性PAP。对于持续存在且缺乏恶性肿瘤常见危险因素的肺结节,即使PAP(尤其是其局灶型)临床罕见,也应将其纳入鉴别诊断。
参考文献:Joseph V. Moran, Amar Mainra, Tian Sun, Eric R. Montgomery, Lauren A. Rome, Michael J. Walker,A 40-Year-Old Woman With an Incidentally Found Semisolid Pulmonary Nodule,CHEST Pulmonary,Volume 3, Issue 4,2025,100195,ISSN 2949-7892,https://doi.org/10.1016/j.chpulm.2025.100195.

